Повторение материала с целью актуализации знаний. Учащиеся на досках зарисовывают структуру твердых, жидких и газообразных веществ.
ФО:
— наблюдение и комментарии учителя;
— взаимооценивание по дескрипторам;
Садыкова Камшат Утепбергеновна
| Раздел: 6.2А. Вещества и материалы | Школа: | ||||||||||||
| Дата: | ФИО учителя: | ||||||||||||
| Класс: 6 | Количество присутствующих: | ||||||||||||
| Тема урока | Атомы и молекулы. Простые и сложные вещества | ||||||||||||
| Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу) | 6.3.1.1 различать атомы и молекулы, простые и сложные вещества | ||||||||||||
| Цели урока | Учащиеся могут:
| ||||||||||||
| Критерии оценивания | 1.Описывают атомы и молекулы; 2.Различают простые и сложные вещества. | ||||||||||||
| Языковые цели | Учащиеся могут:
Лексика и терминология, специфичная для предмета: атом, молекула, простые вещества, сложные вещества. Полезные выражения для диалогов и письма: Атом – это …. частица Молекулы состоят из …. Два или более атомов могут соединиться с образованием … Это вещество …, так как состоит из … | ||||||||||||
| Привитие ценностей | Данный урок направлен на развитие ценностей академической честности, сплоченности и умения работать в команде. Привитие ценностей осуществляется через организацию групповой и самостоятельной работы. | ||||||||||||
| План | |||||||||||||
| Запланированные этапы урока | Запланированная деятельность на уроке | Ресурсы | |||||||||||
| Начало урока 0-5 5-10 | 1. Повторение материала с целью актуализации знаний. Учащиеся на досках зарисовывают структуру твердых, жидких и газообразных веществ. ФО:
После обсуждения рисунков учитель объясняет, что древние греки выдвинули гипотезу о том, что материя состоит из частиц и мельчайшая частица вещества называется «атом». Обратите внимание учащихся на «теории атома», которую в наше время предложил Джон Дальтон (1805). Дает учащимся обратную связь. 2. Вызов.На стадии «Вызов» для ознакомления предложите учащимся информационные листки, содержащие данные об атомной теории Дальтона. — Как вы думаете, что такое «Атом»? — Как можно различить атомы и молекулы? — Если вещество состоит из одного только элемента, как он будет называться и почему? 3. Целеполагание. Совместно с учащимися определяются цели урока:
| Плакат Маркеры Мел доска карточка | |||||||||||
| Середина урока 10-15 15-20 20-22 22-32 32-37 | 4. Беседа с учащимися: В химии, кроме терминов «атом» и «молекула» часто применяется понятие «элемент». Вопрос: Какие сходства и различия есть между данными понятиями? Химический элемент- это определенный вид атомов. Например, атомы водорода – это элемент водорода; атомы кислорода и ртути – это элементы кислорода и ртути. O2, Cl 2. H2O, CO2 Вопрос:Как вы думаете чем отличаются молекулы кислорода и хлора от молекул углекислого газа и воды? Возможные ответы учащиеся: молекулы кислорода и хлора состоят из атомов одного вида. — Простые вещества. Углекислый газ и вода состоят из атомов разных видов. – Сложные вещества. Простые вещества – вещества, которые состоят из атомов одного вида. Ne, Ar, O2, Br2, I2, O3, P4, S8 Сложные вещества (химические соединения) вещества, которые состоят из атомов разных видов. H2O, C6H12O6, NaCl, KMnO4, CO2, CO 5. Заполнение диаграммы Венна. Опираясь на текст, определите сходства и различия между атомом и молекулой, простыми и сложными веществами. ФО:
6. Объяснение различий между простыми и сложными веществами. Учащимся предоставляется видеоролик. Изучив видеоролик, учащиеся объясняют различие между веществами.
7. Закрепление. С целью закрепления материала учащиеся выполняют задание на разделение веществ на простые и сложные. Задание .Распределите вещества на простые и сложные: SO2 K, Cu, N2, O2 , Cl2 , Al2O3 , H 2 , Br2 , NaCl, MgSO4 , KOH, Fe, Au, Ag, ZnO, LiI KF, Cr, SO3
Учитель дает обратную связь. | карточка Видеоролик «Атомы и молекулы. Простые и сложные вещества» | |||||||||||
| Конец урока: 37-40 | 8. Рефлексия Учитель возвращается к целям урока, обсуждая уровень их достижения. Учащиеся проводят рефлексию письменно дополняя предложения: -Я знаю … -Я умею … | карточка | |||||||||||
| Дифференциация – каким образом Вы планируете оказать больше поддержки? Какие задачи Вы планируете поставить перед более способными учащимися? | Оценивание – как Вы планируете проверить уровень усвоения материала учащимися? | Здоровье и соблюдение техники безопасности | |||||||||||
| На этапе повторения материала, учащиеся делятся на свое усмотрение, выбирая подходящий для него уровень воспроизведения учебной информации: знания, понимания и применения (рисунок), анализа (анализ и сравнение рисунков). На уроке используется учебная информация с учетом различных типов восприятия информации. На этапе закрепления менее способным учащимся предлагаются различные подмостки. | Формативное оценивание ранее полученных знаний по целям обучения предварительных знаний. Через диаграмму Венна оцениваются навыки сравненияпонятий простых и сложных веществ, а также атомов и молекул. | Соблюдение техники безопасности при передвижении учащихся по классу во время групповой работы. | |||||||||||
-75%
Сохранить у себя:

«В науке необходимо воображение. Она не исчерпывается целиком ни математикой, ни логикой, в ней есть что-то от красоты и поэзии.»
Мария Митчелл (American Astronomer, 1860 г.)
Эта глава не составляет неотъемлемой части курса. Включили мы ее по следующим причинам:
1) Материал позволяет провести ряд красивых опытов, причем некоторые из них могут быть осуществлены в домашних условиях. Сначала рекомендуется проделать опыты и оценить их красоту, а потом уже читать текст.
2) На примере этой главы видно, как происходит исследование определенной области явлений: сначала делаются наблюдения, которые затем интерпретируются, потом высказываются предположения и проверяются снова на опыте. В результате накапливаются полезные сведения и достигается научное понимание явлений.
3) Наряду с выяснением разнообразных практических вопросов (от образования мыльной пены до добычи золота) в главе рассказывается, как определяются размеры молекул, и это пригодится нам при последующем изучении атомов.
ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
Начнем исследование поверхностей жидкостей с наблюдения.
Общие наблюдения. Рассмотрите форму небольших капель:
Опыт 1. Капли, капающие из водопроводного крана.
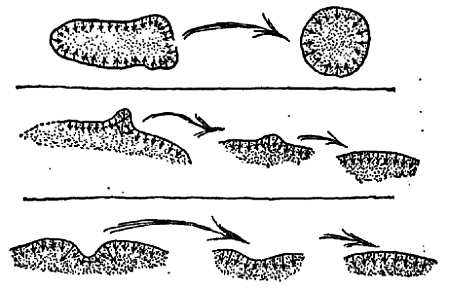
Опыт 2. Лужицы жидкости на столе: а) вода на чистом стекле; б) вода на стекле, покрытом воском; в) ртуть на стекле. Их форма грубо изображена на фиг. 110, б, однако следует, конечно, поступать мудро и наблюдать форму капель в реальных условиях; рисунки в книге годятся лишь для запоминания. Действительно ли слеза на щеке героини имеет ту форму, которая изображается на рисунках в романах?
Опыт 3. Капли дождя представляют собой идеальные шарики, но за ними непосредственно наблюдать очень трудно. Два источника позволяют получить косвенные доказательства: размер и положение которая появляется точно в том месте, где ей следует быть, лишь при условии, что капли дождя круглые (если бы капли имели неправильную форму, положение радуги смещалось бы), и форма свинцовой дроби, получаемой по старинному способу в дроболитейных башнях (фиг. 110, г): расплавленный свинец, разливаемый сквозь сито, падал в виде дождя в глубокий бак с водой и там превращался в круглые шарики.
Задача 1
Маленькая капелька дождя на рукаве шерстяного костюма имеет сферическую форму, а большая капля воды на натертом воском полу принимает более плоскую форму. Почему?
Специальные приборы. Следующий шаг — это применение в науке необходимых приборов или инструментов. С помощью проекционного фонаря понаблюдайте за каплями, изображенными на фиг. 110, а и б. (Если покажется, что вода движется слишком быстро, попробуйте нанести капли вязкого масла с помощью медицинской пипетки.)
Опыт 4. Если вы понаблюдали за всем семейством капель и лужиц разного размера, подобных тем, которые представлены на фиг. 110, д, то сможете вывести (путем индукции) несколько интересных правил. Определите свойства, общие для большинства капель.
Опыт 5. Устраните почти полностью влияние силы тяжести, используя для этого другую жидкость, например анилин (коричневая ядовитая жидкость немного тяжелее воды).
Из бюретки, погруженной в воду, капли анилина образуются очень медленно — сначала на конце трубки появляется и медленно растет «мешок» из анилина, затем появляется тонкая шейка и капля быстро отрывается, после чего шейка превращается в меньшую каплю, которая следует за первой (фиг. 110, е).[67] Если прибор встряхнуть, висящая капля начнет колебаться.
Опыт 6. Иногда на поверхности воды плавают небольшие предметы, которые, казалось бы, должны были бы потонуть, например слегка намазанные жиром иглы или лезвие бритвы, некоторые виды водяных жуков (фиг. 110, ж). Такое впечатление, что их поддерживают какие-то необычные силы.
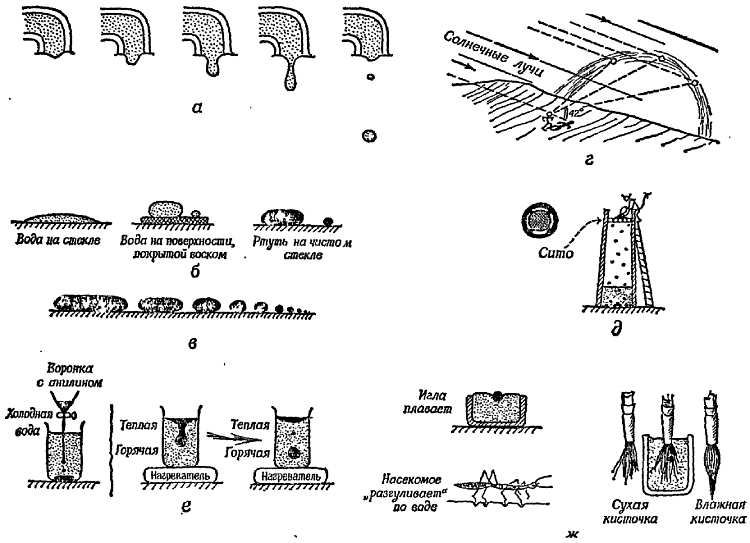
Фиг. 110. Поверхностное натяжение.
а — вытекание капли из очень узкого крана; б — небольшие лужицы жидкости на стекле; в — семейство капель на столе; г — радуга, созданная круглыми каплями дождя; д — старинная дроболитейная башня; е — образование капель анилина и воды; ж — примеры плотных тел, плавающих на поверхности жидкости.
Мыльные пленки. Поверхностные свойства жидкостей удобно наблюдать на мыльных пузырях и пленках, которые «состоят только из поверхности и не имеют внутренности» и вес которых слишком мал, чтобы он мог противостоять поверхностным силам. На фиг. 111 схематически изображены соответствующие опыты.
Опыт 7. Мыльный пузырь на воронке сжимается, задувая пламя свечи (фиг. 111, а).
Опыт 8. «Оконная штора». На проволочной рамке, нижний край которой подвижен, создается мыльная пленка. Ее растягивают, спуская за нить скользящую часть шторы вниз, а затем нить отпускают (фиг. 111, б).
Опыт 9. На квадратной проволочной рамке создают мыльную пленку. На пленку кладут шелковую нить, связанную в виде небольшой петли (фиг. 114, в). Затем пленку внутри петли разрывают.
Опыт 10. Опыт «оконная штора» повторяют с помощью рамки, имеющей подвижные стержни сверху и снизу (фиг. 111, г). Верхний стержень удерживается небольшой пружиной. Мыльная пленка создается между двумя стержнями, после чего нижний стержень двигают с помощью нити вверх и вниз.
Опыт 11. На концах Т-образной трубки выдувают два мыльных пузыря разного размера (фиг. 111, д). Затем конец, через который производили выдувание, закрывают, и оба пузыря остаются соединенными.
Фиг. 111. Мыльные пузыри.
Задача 2
Запишите ваши наблюдения о каждом из описанных опытов, а затем скажите, какие выводя можно сделать из них относительно мыльных пленок и их «поверхностного натяжения». (Замечание. Плоская фигура с максимальной площадью при заданном периметре есть круг.) Предупреждение. Важное следствие из опыта 8 исключает простейшее объяснение опыта 11.
Общие пояснения
Что говорят эти опыты о поверхностях жидкостей? Капли, образующиеся в водопроводном кране, выглядят так, как будто они заключены в резиновый мешок.
Взяв настоящую оболочку из тонкой резины, мы можем сделать большую искусственную «каплю», которая по мере того, как внутрь оболочки будет вливаться все больше воды, примет форму реальной капли; однако возрастающее натяжение резины помешает точной аналогии.
Капли дождя и лужицы жидкости на столе, по-видимому, стремятся принять круглую форму, что также наводит на мысль об оболочке, которая сжимает их и противодействует силе тяжести.
Обдумав эти наблюдения, можно сделать два вывода, расплывчатых и рискованных, но заслуживающих дальнейшей проверки.
А. Поверхности жидкостей ведут себя так, будто их удерживает эластичная оболочка, стремящаяся придать им круглую форму.
Б. «Эффект оболочки» более заметен при малых размерах (маленькие капли), чем при больших (лужи воды), но когда сила тяжести уравновешена другими силами, он проявляется и при больших размерах.
Классификация и терминология
Поверхностное натяжение. Все описанные явления называют «эффектами поверхностного натяжения» и говорят, что жидкость имеет поверхностное натяжение, подобное натяжению растянутой резиновой оболочки. Пока это просто удобное название, которое само по себе не может ничего доказать или объяснить. В лучшем случае оно стимулирует обсуждение и позволяет легко определить, о чем идет речь. В худшем случае — приводит людей к неправильной мысли о том, что на поверхности существует реальная пленка, которую можно содрать с капли, как шнурку с кролика.
Краевой угол. По своей форме лужицы жидкости на столе делятся на два типа.
1) Когда жидкость прилипает к столу и растекается, как на фиг. 112, а, говорят, что жидкость смачивает поверхность стола.
2) Когда жидкость собирается в округлую каплю вопреки действию силы тяжести, как показано на фиг. 112, б, говорят, что она не смачивает поверхности. Если стол наклонить, то такие капли будут скатываться.
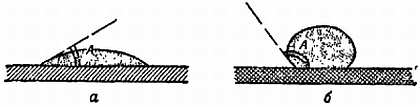
Фиг. 112. Краевой угол.
а — малый угол; б — большой угол.
Эти два случая различаются по углу А (угол внутри жидкости между поверхностью стола и поверхностью жидкости в месте их соприкосновения), который называют краевым углом. Тот же угол существует и на других границах раздела, например в том месте, где поверхность воды встречается со стенками стакана. Если угол А мал, жидкость смачивает твердую поверхность. Это снова только название. Выбрав этот угол и дав ему название, мы ничего не узнали и не объяснили, а лишь облегчили обсуждение[68].
Попытка построить теорию
Молекулы. Примем данное химиками определение молекул как мельчайших частиц вещества, из которых построены более крупные предметы, и приведем несколько рассуждений. Хотя такие предметы, как молекулы, видимо, существуют, их в обычный микроскоп не видно (впоследствии, правда, будут приведены убедительные косвенные доказательства их существования), поэтому они должны быть очень малы и многочисленны. Судя по тому, как жидкости льются, их молекулы, очевидно, легко скользят относительно друг друга. Жидкость трудно сжимается; это наводит на мысль, что молекулы в ней расположены тесно. Другие данные, с которыми вы познакомитесь позднее, позволяют думать, что молекулы жидкости постоянно находятся в быстром движении, сталкиваясь друг с другом, подобно людям в толпе, причем с повышением температуры движение это усиливается. Действительно, поведение жидкости можно имитировать с помощью стальных шариков или зерен песка, если эти большие «молекулы» заставить непрерывно вибрировать.
Молекулярные силы: притяжение и отталкивание. Рассмотрим жидкость с точки зрения такой молекулярной картины. Сразу же возникает мысль, что молекулы жидкости сопротивляются их растаскиванию в разные стороны, т, е. притягиваются друг к другу. Вода в наполовину полном кувшине не расширяется и не улетучивается в отличие от газа, который стремится заполнить весь сосуд и быстро улетучивается, или диффундирует. Если сосуд открыт, жидкость остается в сосуде и ее молекулы, по-видимому, притягивают друг друга. Пока мысль о притяжении является лишь смутной догадкой. Именно в поверхностном натяжении, как и в некоторых других явлениях, эта мысль находит основательное подтверждение. Тот факт, что жидкости сильно сопротивляются сжатию, говорит о сопротивлении молекул жидкости более тесному сближению; следовательно, они должны отталкивать друг друга. Таким же образом должны вести себя и молекулы газа при очень тесном сближении[69], и молекулы твердых тел[70]. Например, молекулы указательного и большого пальца отталкиваются при сжатии — какая другая причина могла бы помешать пальцам проникнуть один в другой? Но твердые вещества тоже сопротивляются попыткам растащить их в разные стороны; молекулы этих веществ должны притягивать друг друга. Мы представляем себе, что между молекулами твердых тел действуют два типа сил: силы отталкивания, которые, как показывает опыт, действуют только на очень малых расстояниях, т. е. короткодействующие силы, и силы притяжения, которые действуют на более далеких расстояниях, т. е. дальнодействующие силы. В обычном ненапряженном твердом теле каждая молекула занимает нейтральное положение, так что равнодействующая этих сил равна нулю. При сжатии твердого тела возрастающее отталкивание между молекулами оказывает сопротивление.
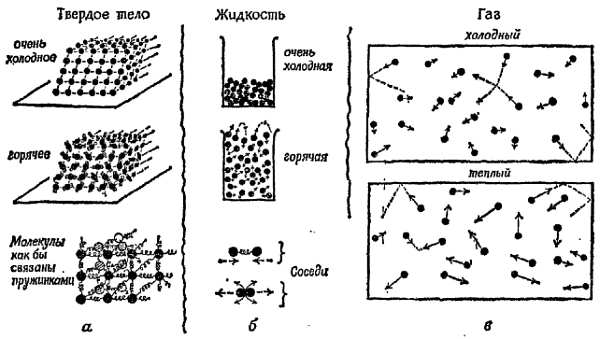
Фиг. 113. Молекулы в твердом теле, жидкости и газе.
а — в твердых телах молекулы образуют правильную систему; все истинно твердые тела — кристаллические. Молекулы сохраняют более или менее постоянное положение, но по мере нагревания тела они колеблются все больше и больше; б — в жидкостях молекулы расположены близко друг к другу, как в твердых телах, но свободно перемещаются среди своих соседей. Чем выше температура, тем быстрее движение и тем более бурно происходят столкновения молекул; в — в газах молекулы находятся далеко друг от друга и быстро движутся, время от времени сталкиваясь (чем выше температура, тем быстрее они движутся). Во время столкновений молекулы должны отталкиваться, в остальное время их действие друг на друга пренебрежимо мало.
При растяжении твердого тела отталкивание уменьшается больше, чем притяжение, и снова возникает напряжение, сопротивляющееся нашим усилиям. Опыты показывают, что притяжение действует не на очень больших расстояниях, а лишь на расстоянии одного или двух диаметров молекул.[71] Между молекулами жидкости, как мы полагаем, действуют подобные же силы: отталкивание на очень малых расстояниях (например, при столкновениях) и притяжение, распространяющееся более далеко. (Тут как будто возникает противоречие. Жидкости должны были бы хоть немного растягиваться при растяжении, на самом же деле при попытке растяжения они распадаются на части и в них образуются пузырьки пара. Однако если позаботиться о тщательном удалении растворенного воздуха, жидкость можно заставить выдержать растяжение и вести себя необычным образом. Например, вода или ртуть держатся в верхней части барометра намного выше «высоты атмосферного столба», а сифон может работать в вакууме! Жидкости оказываются «слабыми, как вода» только в результате вредного влияния маленьких пузырьков воздуха.)
Молекулярное объяснение поверхностного натяжения. Итак, тот факт, что жидкости сохраняют свой объем, мы «объяснили» наличием дальнодействующих сил притяжения. Посмотрим, не смогут ли эти силы объяснить существование поверхностного натяжения. Представим себе состояние молекулы А в середине сосуда с водой (фиг. 114). Со всех сторон ее толкают другие молекулы. Кроме того, со всех сторон ее притягивают ближайшие соседи — и равнодействующая сила притяжения равна нулю.
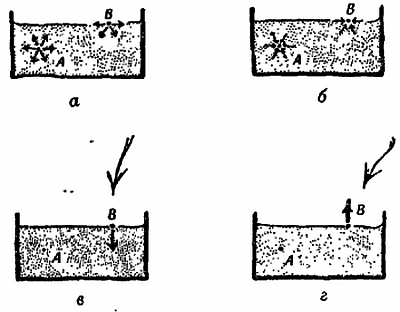
Фиг. 114. Силы, действующие на молекулы, в жидкости.
а — дальнодействующее притяжение ближайших соседей; б — короткодействующее отталкивание близких соседей при столкновении; в — равнодействующая притяжения (нуль для А, направлена вниз для В); г — равнодействующая отталкивания (нуль для А, направлена вверх для В).
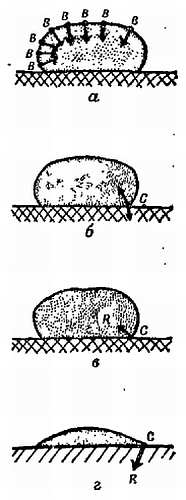
Теперь рассмотрим другую молекулу В, находящуюся на поверхности воды. Ее тоже толкают, но не со всех сторон, и тоже притягивают, но не во всех направлениях. В области действия сил притяжения у нее есть соседи снизу и с каждой стороны, но нет соседей сверху. Равнодействующая сил притяжения направлена внутрь жидкости и уравновешивается действием столкновений снизу. Таким образом, молекула В испытывает притяжение вниз, наподобие дополнительного веса. Во внутренних областях большой круглой капли молекулы будут, подобно молекуле А, испытывать равномерное притяжение со всех сторон. Молекулы на поверхности, подобно молекуле В, будут втягиваться внутрь. Так как такие молекулы В будут пытаться приблизиться к центру капли, поверхность будет стремиться сжаться; по существу создается впечатление, что капля имеет сжимающуюся оболочку. Очевидно, если на поверхности образуется гребень, молекулярное притяжение распрямит его, несмотря на мешающие возмущения (небольшое углубление на поверхности также исчезнет, хотя это менее очевидно); в результате притяжения молекул все неровности на поверхности будут сглаживаться (фиг. 115).
Фиг. 115. Поверхностные силы в небольшой капле жидкости.
Действующее на молекулы типа В притяжение соседей стремится придать массе жидкости сферическую форму. (Заметьте, что сфера имеет минимальную поверхность при заданном объеме.) Если на поверхности появляются небольшие неправильности, поверхностные силы стремятся устранить их.
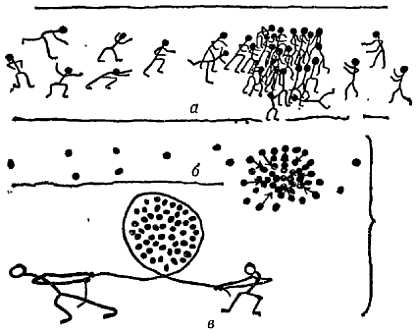
Чтобы представить себе общую картину, сравните заполненную молекулами каплю с толпой людей, привлеченных уличной дракой. На фиг. 116, б показан вид толпы с птичьего полета. Прибывает все больше и больше заинтересованных зевак. Опоздавшие плохо видят, что происходит, они напирают на впереди стоящих — их притягивает любопытство, но они напирали бы так же, если бы их притягивали просто стоящие впереди соседи. Как влияет это притяжение к центру на толпу в целом? Подвижная толпа стягивается в круг с минимальным внешним периметром. Круг имеет меньшую протяженность периметра, нежели любая другая фигура с той же общей площадью. Человек А, находящийся в глубине толпы, оказывается сжатым, и если ему позволяет рост, то видит, что его неприятные ощущения вызваны напирающими на него людьми, нажимающими внутрь. Он будет страдать точно тай же, если накинуть на толпу огромный пояс и затягивать его. Натянутый пояс будет влиять на внешнюю форму толпы и на тесноту внутри нее точно так же, как и стремление людей, находящихся снаружи, пробиться к середине.
Фиг. 116. Толпа.
а — толпа собирается; б, в — эффект одинаковый.
Поможет ли эта аналогия[72] понять, каким образом молекулярное притяжение оказывает то же действие, что и эластичная оболочка, растянутая по всей поверхности жидкости? С молекулярной точки зрения на поверхности жидкостей существует не реальная «шкурка», как у кролика, а особый слой внешних молекул.
Соотношение между поверхностными и объемными эффектами. Насекомые и поверхностное натяжение
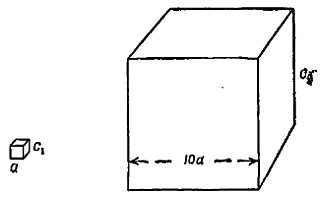
Почему эта «оболочка» превращает маленькие капли в совершенные по форме шарики вопреки действию силы тяжести и не может сделать этого с более крупными лужами? С молекулярной точки зрения (согласно нашей теории, если вам угодно) это обусловлено особым поведением молекул, расположенных на поверхности. Эти силы действуют на поверхности и не связаны с основной массой жидкости. Но сила тяжести действует на всю жидкость, равным образом на ее внешние и внутренние слои. Поверхностное натяжение — это «поверхностный эффект», а вес — «объемный эффект», и их относительная важность будет изменяться в зависимости от реального размера капли или лужи. Представим себе, что поверхностные силы возрастают прямо пропорционально величине поверхности[73], тогда как вес, конечно, возрастает пропорционально объему. Рассмотрим превращение небольшой капли в каплю, в 10 раз большую. Для простоты представим, что капли имеют вид кубиков[74]: маленького С1 (фиг. 117) с длиной ребра а и большого С2 с ребром 10а. Как соотносятся их поверхности?
Фиг. 117. Кубические «капли».
Сравнение поверхности и объема.
Каждый куб имеет шесть граней. Поверхность куба С1 равна 6a2, а куба С2 равна 6∙(10а)2, т. е. 600а2. Куб с десятикратными линейными размерами имеет в 102, или в 100 раз, большую поверхность. Как соотносятся объемы этих кубов? Они соответственно равны а3 и (10а)3, т. е. 1000а3. Объем одного куба превышает объем другого в 103, или в 1000 раз, и, следовательно, вес воды в нем будет в 1000 раз больше. При переходе от малого кубика к большому поверхностные эффекты возрастут только в 100 раз, но действие силы тяжести возрастет в 1000 раз; таким образом, ее относительное значение увеличится в 10 раз.
На самом же деле силы поверхностного натяжения растягивают каждую границу, или край, поверхности. Поэтому они возрастают пропорционально линейным размерам, т. е. пропорционально ребру или радиусу, и уменьшаются по сравнению с объемными силами еще более резко.
Для очень больших объемов сила тяжести во много раз превосходит влияние поверхностного натяжения; поэтому поверхность прудов плоская, а пролитое на пол ведро воды растекается под действием силы тяжести. На форму маленьких капель сильно влияет поверхностное натяжение, для очень маленьких капель это влияние становится определяющим. Для ныряющего в воду человека главную опасность представляет давление на него воды. Для крошечного клопа, ползущего по капле дождя, непреодолимы силы поверхностного натяжения. Теперь понятно, почему маленькие водяные насекомые могут бегать по поверхности пруда не проваливаясь? Они ничем не рискуют: большинство из них водой не смачивается и провалиться не может. Даже если их насильно затолкнуть под воду, они немедленно выскочат наружу, причем помогает им поверхностный слой. Для крошечных насекомых, тело которых имеет способность намокать, капля воды оказывается тюрьмой.
Частично смачиваемые водой насекомые могут держаться на ее поверхности, если они достаточно малы, но, погрузившись однажды в воду, случайно проскочив через упругую поверхность, они уже не смогут выбраться наружу. В жизни еще более мелких существ, например микробов, все определяется поверхностными силами; вес едва ли имеет для них какое-либо значение. Весь контакт с внешним миром они осуществляют через свою поверхность; через нее поступает пища, и, если они хотят двигаться, им надо изменять-форму своей поверхности. Не удивительно поэтому, что такие существа можно уничтожать с помощью ядов, которые покрывают их поверхность, подобно тому как краска наносится на волокна одежды.
Размышления завели нас далеко от экспериментальных фактов.
Некоторые из развитых идей подтверждаются последующими опытами, другие стоят лишь немногим более простой игры воображения, и их следует использовать только в той мере, в какой они приводят к плодотворным предположениям.
Краевой угол с молекулярной точки зрения
Все же мы можем развить дальше молекулярную картину и обсудить, как жидкости соприкасаются с твердыми телами, т. е. обсудить вопросы смачивания и водоотталкивания.
Возвращаясь к небольшим лужицам на столе и к классификации по краевым углам, нарисуем каплю, поверхность которой принимает выпуклую форму под влиянием поверхностных сил, действующих на молекулы (фиг. 118).
Фиг. 118. Поверхностное натяжение и краевой угол с молекулярной точки зрения.
а — притяжение поверхностных молекул В со стороны соседей создает эффекты оболочки; б, в — угловые молекулы С притягиваются соседями в жидкости и молекулами стола, R — равнодействующая сил притяжения; г — молекула С притягивается столом сильнее, чем соседями в жидкости.
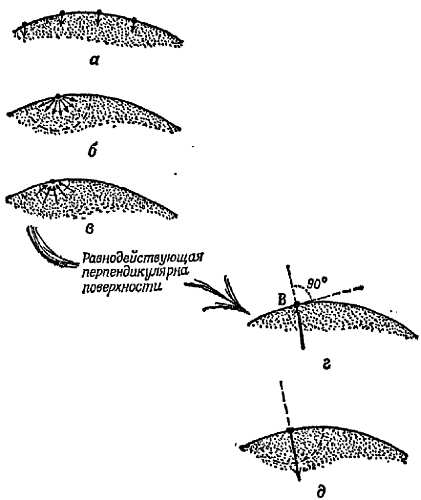
В том месте, где лужица соприкасается со столом, угловые молекулы должны также притягиваться столом. Совместное притяжение стола и жидкости и определяет краевой угол. Складывая силы притяжения как векторы, получаем равнодействующую R сил притяжения со стороны соседних молекул как жидкости, так и стола. Для поверхности жидкости эта равнодействующая играет роль «вертикали», и поверхность расположится перпендикулярно к ней, точно так же, как поверхность большой лужи принимает горизонтальное положение, перпендикулярно силе тяжести. Итак, краевой угол определяется направлением равнодействующей сил притяжения R; прежде чем продолжить обсуждение, рассмотрим подробнее силы, которые определяют форму поверхности.
Молекулярные силы и поверхность жидкости
Чтобы понять, почему поверхность жидкости располагается перпендикулярно равнодействующей сил притяжения R, вернемся к обсуждению сил, действующих на молекулу. На молекулы действуют:
дальнодействующие силы:
а) сила тяжести;
б) притяжение соседей (только в пределах нескольких диаметров молекул);
короткодействующие силы:
в) сильное отталкивание во время столкновений с соседями (на расстоянии долей диаметра молекулы).
Для описания поведения молекул вряд ли стоит применять термин «равновесие», но все же можно сказать, что в покоящейся жидкости каждая молекула в среднем находится в равновесии.
Фиг. 119. Коротко- и дальнодействующие силы.
а — силы тяготения (очень малы); б — дальнодействующее притяжение соседей; в — короткодействующее отталкивание ори столкновении; г — равнодействующая 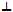
равнодействующей дальнодействующих сил притяжения.
На любую молекулу на поверхности жидкости короткодействующие силы действуют со всех сторон и снизу, поэтому равнодействующая будут перпендикулярна поверхности. Равнодействующая дальнодействующих сил, которая уравновешивает эти короткодействующие силы, должна иметь противоположное направление, а следовательно, она также будет перпендикулярна поверхности. Из последнего утверждения следует и обратное — поверхность должна быть перпендикулярна равнодействующей сил притяжения, в противном случае все силы перемещали бы поверхность, пока она не приняла бы этого положения. (Конечно, в молекулярном масштабе сама поверхность исчезает в хаосе беспорядочных движений, подобно границе толпы. Она представляется гладкой, только когда ее рассматривают издалека.) Две из названных сил действуют на поверхность и меняют свое направление, когда поверхность изгибается. Это — короткодействующее отталкивание и дальнодействующее притяжение соседей. Третья сила — земное притяжение — всегда направлена вертикально вниз. В большом пруду основное направление задается силой тяжести, которая превращает всю поверхность в горизонтальную плоскость; поэтому две другие силы также вертикальны. На молекулы же, расположенные вблизи твердой стенки или на поверхности небольшой искривленной капли, притяжение соседей влияет намного больше, чем сила тяжести. Поэтому для объяснения искривленного мениска или краевого угла силой тяжести можно пренебречь. Просто говорят: «Поверхность располагается перпендикулярно равнодействующей сил притяжения, которые действуют на молекулу, находящуюся на поверхности».
Краевой угол и молекулярные силы
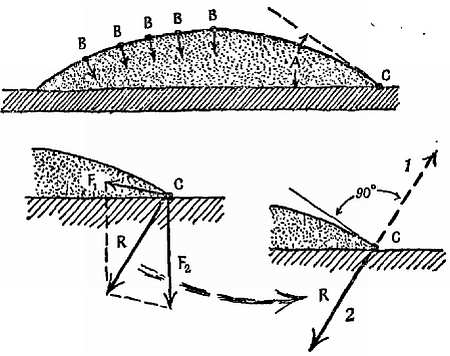
Чтобы объяснить природу краевого угла с точки зрения молекулярных сил, рассмотрим силы притяжения, действующие на молекулу С, которая находится в том месте, где лужица жидкости соприкасается с твердым столом (фиг. 120).
Фиг. 120. Силы, действующие на молекулу, находящуюся на краю небольшой лужицы жидкости.
Лужица находится на столе, который сильно притягивает молекулы жидкости. 1 — короткодействующие силы; 2 — дальнодействующее притяжение.
Во-первых, на нее действует притяжение соседей, находящихся внутри слоя жидкости; равнодействующая этих сил равна F1 и направлена по биссектрисе угла клина (направление подсказано симметрией). Во-вторых, ее притягивают молекулы твердого стола с равнодействующей F2, которая перпендикулярна столу (снова по соображениям симметрии).
Векторное сложение сил F1 и F2 и дает их равнодействующую R; поверхность жидкости должна расположиться перпендикулярно R.
Это схематически изображено на фиг. 120, где F1 дано намного меньше F2, чтобы показать, что молекула С притягивается своими собратьями меньше, чем столом. В таком случае краевой угол невелик и жидкость смачивает стол. Можно сказать, что сильно притягивающий стол побуждает жидкость растекаться. Таким образом, смачивание зависит от относительной силы молекулярного притяжения. Если молекулы жидкости притягиваются молекулами твердого тела сильнее, чем соседними молекулами самой жидкости, жидкость будет смачивать стол и растекаться.
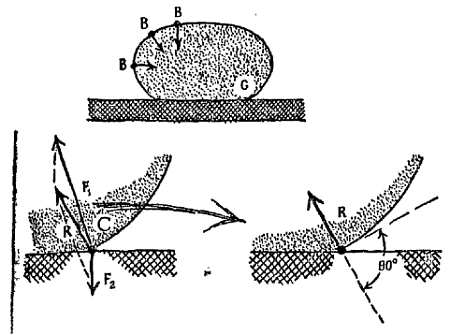
С другой стороны, если молекула жидкости предпочитает своих собратьев молекулам стола, силу F1 следует нарисовать больше F2 и картина примет такой вид, как на фиг. 121, где показан большой краевой угол. Для «водоотталкивания», по-видимому, требуется, чтобы молекулы жидкости испытывали со стороны соседних молекул стола меньшее притяжение, чем со стороны соседних молекул жидкости.
Фиг. 121. Силы, действующие на молекулу, находящуюся на краю небольшой лужицы жидкости.
Лужица находится на столе, который слабо притягивает молекулы жидкости.
Водоотталкивание и смачивание
Таково молекулярное объяснение смачивания и краевого угла.
Объяснение? Разве это не просто волшебная сказка, выдуманная для того, чтобы свести концы с концами? Нет, это объяснение совсем не так плохо, поскольку оно основано на молекулярных представлениях, которые используются в других областях физики и химии. Кроме того, оно позволяет сделать полезные рекомендации:
1) Для улучшения смачивания (мечта прачек) надо сделать F2 больше, чем F1, т. е. надо, чтобы молекулы жидкости притягивались твердым телом сильнее, чем своими соседями. Это можно осуществить, применяя молекулы-посредники, которыми на практике являются молекулы мыла. Таким образом, мы раскрыли секрет мыла и указали путь к созданию новых синтетических моющих средств.
2) Чтобы увеличить краевой угол (надежда изготовителей плащей), надо покрыть текстильное волокно каким-либо веществом, для которого F2 мало по сравнению с F1. На вопрос: «Какой толщины должно быть покрытие?» (еще одна забота изготовителей плащей) — примечание на стр. 195 отвечает, что достаточно очень тонкого слоя, толщиной в несколько молекул. (На вопрос: «Какова толщина молекулы?» — дан ответ в этой главе.)
3) В тех случаях, когда роль поверхностных сил велика, жидкость с небольшим краевым углом (F2 больше F1) будет расползаться вдоль твердой поверхности, даже карабкаясь вверх. Это особенно заметно, когда жидкости поднимаются в очень узких трубках; «капиллярность» — полезное свойство жидкостей, и мы сейчас его разберем.
Капиллярность
ДЕМОНСТРАЦИОННЫЙ ОПЫТ
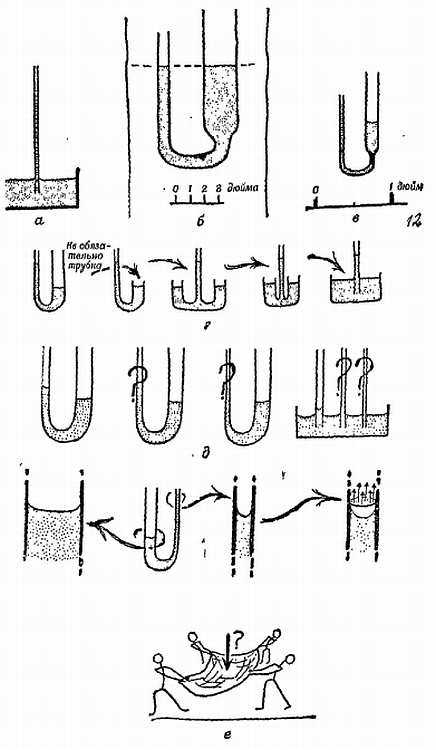
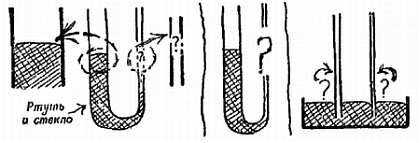
Опыт 12. Нагрейте кусок стеклянной трубки, растяните его в очень тонкую трубку и опустите один ее конец в чернила (фиг. 122, а). Окрашенная вода поднимается вверх вопреки силе тяжести, опровергая правило: «вода в сообщающихся сосудах устанавливается на одном уровне». Однако в U-образной трубке с колонами разного сечения жидкость все же устанавливается на одном уровне (фиг. 122, б). Если вспомнить обсуждение относительной роли поверхностных и объемных эффектов, можно догадаться, что влияние поверхностного натяжения будет более заметно в приборах малых размеров; например, в небольшой U-образной трубке (фиг. 122, в). Конечно, это то же самое, что мы уже видели при погружении тонкой трубки в чернила.
Наброски, представленные на фиг. 122, г, помогают понять переход от одного опыта к другому. Если жидкость поднимается в тонких трубках, то в еще более тонких она должна подняться еще выше. Проверьте это (см. фиг. 122, д).
Фиг. 122. Капиллярные явления.
Поскольку это следствие поверхностного натяжения проявляется в трубках, «тонких, как волос», оно получило название от латинского слова «волос» — capilla. Таким образом, капиллярность — это старое название поверхностного натяжения, которое еще применяется, чтобы охарактеризовать поведение жидкостей в тонких трубках. Это красивое название, но оно не объясняет подъема жидкости. Сказать, что вода поднимается по тонкой трубке вследствие капиллярности, по существу то же, что сказать «вследствие поведения тонких трубок». Рассматривая через увеличительное стекло мениск (поверхность жидкости) в тонкой трубке, мы увидим, что он висит, как прикрепленный к стеклу изогнутый мешок, весьма похожий на одеяло пожарников, которые ловят выбрасывающегося из окна горящего дома тяжелого мужчину (фиг. 122, е).
Снова возникает мысль о резиновой оболочке. Если измерить силы, удерживающие оболочку, то видно, что эти же силы определяют форму маленьких капель. Можно даже говорить, что оболочка удерживает поднимающуюся по трубке жидкость[75], но более реально говорить о молекулах, которые вскарабкиваются по внутренней поверхности трубки и образуют изогнутый мениск.
Жидкости поднимаются не только в круглом стеклянном капилляре. Капиллярность проявляется в любом узком пространстве.
Когда вода стекает между щетинками малярной кисти или увлажняет в ванне ваши волосы, то она заполняет не полые волоски, а узкие промежутки между отдельными волосками. На таком поведении жидкостей основано всасывание масла в ламповый фитиль, воды в банное полотенце и т. д.
Задача 3 (трудная). Формула капиллярности
Допустим, что подъем жидкости в капилляре определяется разностью давлений по обе стороны мениска. Вернитесь к опыту с двумя соединенными друг с другом мыльными пузырями (см. фиг. 111, д). Какой вывод только из этого опыта можно сделать о соотношении между высотой подъема в капилляре и его диаметром?
Задача 4. Капиллярность в несмачиваемой трубке
Возьмем жидкость, которая образует со стенками трубки большой краевой угол. На фиг. 123 показана, например, ртуть в стеклянной трубке.
Фиг. 123. К задаче 4.
Уровень ртути в широкой трубке показан, но рисунки не закончены. Набросайте в тетради все эти рисунки и закончите их.
Применения капиллярности
Чтобы жидкость втягивалась в капилляр, а не только поднималась вверх, и вообще проникала в поры, необходим малый краевой угол между жидкостью и стенками пор. При большой величине краевого угла предметы будут оставаться сухими. Ниже приведены примеры, которые демонстрируют роль капиллярности и смачивания в природе и в быту.
1) Системы, где нужен малый краевой угол (желательно при большом поверхностном натяжении)
Вода на волокнах банных полотенец и т. д.
Чернила на конце пера (щель на конце пера подает чернила на бумагу вследствие капиллярности; стальные перья, применявшиеся прежде, когда они бывали новыми, имели большой краевой угол, и для улучшения работы перья следовало смочить слюной).
Чернила на бумаге (но поры в бумаге должны быть закрыты).
Кровь на бинтах.
Капли от насморка на слизистой оболочке носа.
Припой на металле (для уменьшения краевого угла применяют флюс).
? Слюна на пище.
Растворитель для краски на сухом порошке красителя.
Жидкая краска на окрашиваемых поверхностях (с этим связан ряд вопросов в технике живописи).
Мыльная вода при стирке грязной одежды.
? Вода на стеклах очков (здесь нет узких промежутков, но при небольшом краевом угле конденсирующаяся на стекле вода создает плоскую пленку, а не туман из капелек).
2) Системы, где нужен большой краевой угол
Вода на спине утки, на тканях для палаток и зонтов.
? Блинное тесто на сковороде.
Вода на полу в ванной.
? Вода на стеклах очков (мелкие капли быстрее испаряются).
Важную роль капиллярность играет в садоводстве. Вода проникает в тонкие промежутки между частицами почвы. Разрыхление и вскапывание изменяет размеры этих промежутков и затрудняет доступ воды из глубины почвы к поверхности, предотвращая тем самым ее испарение.
Кирпичи пористы. Кирпичные дома на высоте 30 см или более от поверхности земли должны иметь изоляцию от влаги из непористого материала.
Объяснение капиллярности с молекулярной точки зрения
По всей трубке вверх поднимается очень тонкий слой жидкости, возможно, толщиной в одну молекулу, а за ним ползет основная масса жидкости, образуя искривленный мениск. Силы F1 и F2 для случаев малого и большого краевого угла схематически изображены на фиг. 124.
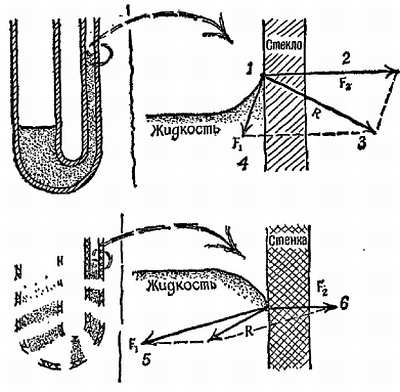
Фиг. 124. Молекулярные силы, краевой угол и капиллярность.
1 — рассматриваемая молекула; 2 — притяжение стекла; 3 — равнодействующая сил притяжения; 4, 5 — притяжение соседей в жидкости; 6 — притяжение стенки.
Поверхность жидкости располагается перпендикулярно равнодействующей R сил притяжения, действующих на ее молекулы. Это является результатом короткодействующих сил, которые проявляются при столкновениях с другими молекулами. Когда краевой угол равен нулю, стеклянная стенка, вероятно, на всем протяжении покрыта тонким слоем жидкости толщиной в несколько молекул. Мениск всползает по этому слою жидкости.
Рисунки весьма упрощены, так как на них не учтена сила тяжести.
Вещества, облегчающие смачивание: мыла и моющие средства
Очень часто, когда нужен малый краевой угол, природа дает нам большой. Овечья шерсть, например, не смачивается водой; это мешает обработке отары растворами при дезинсекции. С обеденной посуды вода скатывается, как со спины утки, и даже на чайных стаканах порой остаются несмачиваемые отпечатки пальцев. А новые посудные полотенца, поступающие со склада с ужасной восковой отделкой! Нам необходимы молекулы-посредники, которые образовывали бы промежуточный слой и уменьшали бы краевой угол между водой и жирными тарелками, покрытыми воском волокнами одежды и т. д. Сейчас эту роль выполняют моющие средства, предшественником которых было мыло. Мыло действует на жир с помощью поверхностного натяжения, помогая воде заползать под жир и отрывать его частички, которые смываются в виде эмульсии (скопление мелких частиц жира, взвешенных в воде). Один конец молекулы мыла имеет сродство к воде вследствие химического или электрического притяжения[76], а другой конец инертен к воде, но легко присоединяется к жиру. В то время как «жирные» концы образуют облако вокруг частиц жира, «водяные» концы выступают наружу и притягивают воду. Современные синтетические мыла или стиральные порошки обычно облегчают смачивание. Их молекулы действуют как посредники и уменьшают краевой угол. Они проникают в любую щель между жиром и тарелкой, облегчая попадание туда воды.
Вообразим себя в роли физиков-судомоек, которые приходят к группе химиков и говорят: «Пожалуйста, разработайте и пустите в производство вещество, которое было бы пригодно в качестве моющего средства. Оно должно иметь следующие свойства:
1) его молекулы должны притягиваться к жиру (или, для других целей, — к текстильным волокнам);
2) его молекулы должны также притягиваться к воде;
3) оно должно довольно легко растворяться в воде, чтобы его молекулы могли плавать и достигать границы вода/жир, где необходима их помощь.
P. S. Производство этого средства должно быть недорогим».
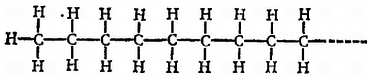
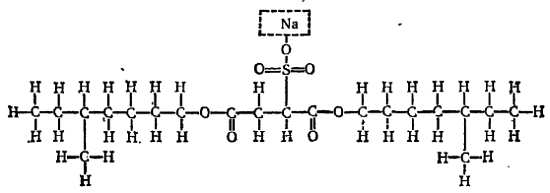
Современные химики-органики ответят: «Это легко сделать». Чтобы прицепиться к воску или к жиру, молекулы должны иметь длинную углеводородную цепь, подобную следующей[77]»:
но не слишком длинную, иначе она не будет растворяться в воде.
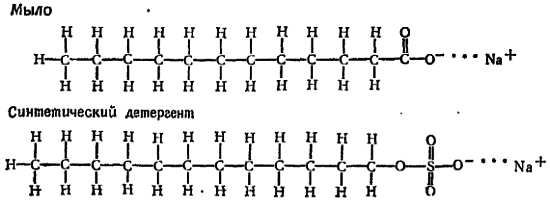
Воски и жиры имеют аналогичную цепную структуру, и они должны притягивать такие цепи. Затем это вещество на одном из концов должно иметь нечто обладающее сродством к воде, например атом натрия. Годится любая группа, которая будет отделяться в воде, освобождая электрический заряд, поскольку молекулы воды несут на концах заряды + и — и будут скапливаться вокруг других зарядов.
Такого рода молекулы были сконструированы и изготовлены, и сейчас мы покупаем их в больших количествах в хозяйственных магазинах. Ниже приведены примеры обычного мыла и синтетического стирального порошка подобной структуры[78]).
К числу таких веществ относится также применяемый в фотографии и исследовательской работе аэрозоль. Его молекула представляет собой длинную цепь с воскообразными концами и «притягивающим воду» атомом натрия в середине:
ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
Опыт 13. На покрытое воском стекло наносят каплю чистой воды (фиг. 125). Концом спички добавляют раствор моющего средства и следят за изменением краевого угла.
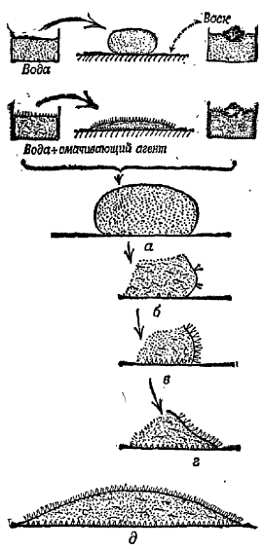
Фиг. 125. Действие смачивающего агента.
Длинные молекулы показаны линией с точкой, которая обозначает группу, имеющую сродство к воде. Молекулы смачивающего агента аэрозоля показаны не в масштабе, а увеличены во много раз. а — на столе, покрытом воском, образуется небольшая лужица; б — добавляется смачивающий агент; в — молекулы смачивающего агента собираются на поверхности инертными концами наружу; г — капля воды покрыта молекулами смачивающего агента и испытывает сильное притяжение к покрытому воском столу; д — краевой угол сильно уменьшается, и вода растекается по столу.
Опыт 14. Новое посудное полотенце с воскообразной поверхностью разрезают на два куска и растягивают на наклонном столе. На один кусок выливают крепкий раствор красителя. Краситель впитывается с трудом, большая его часть стекает. Затем на другой кусок выливают остаток красителя, к которому добавлено небольшое количество моющего средства.
Действие мыла и моющих средств. Когда раствор моющего средства попадает на покрытую воском поверхность, его молекулы скапливаются вокруг воска, причем их «жирные» концы направлены в сторону воска, а «водяные» — наружу. Эти внешние концы создают оболочку, которая притягивает воду, и этим облегчают смачивание. (Аэрозоль, молекула которого имеет удвоенную длину, прикрепляется к воску, жиру или целлюлозе обоими концами и поднимает имеющую сродство к воде середину, подобно выгнувшей спину гусенице; выпяченные «спины» создают притягивающую воду оболочку.)
Мытье посуды. Молекулы большинства моющих средств и мыла имеют на одном конце группу, обладающую сродством к воде. Действие этих веществ при мытье посуды схематически изображено на фиг. 126.
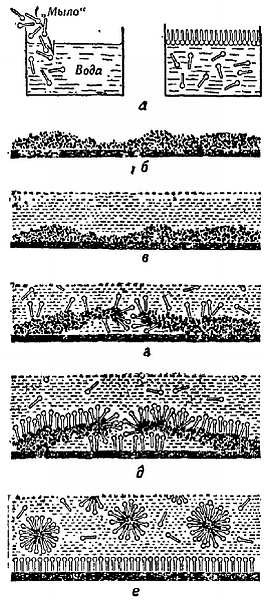
Фиг. 126. Действие моющего вещества (натурального или синтетического).
а — к воде добавляют молекулы «мыла»; б — моющее действие (тарелка, покрытая частицами жирной грязи); в — добавленная вода не может удалить грязь; г — добавлен детергент; инертные воскоподобные концы его молекул притягиваются к границе между водой и грязью; в — инертные концы скапливаются на грязи, которую теперь можно удалить проточной водой или мочалкой; е — грязь удерживается во взвешенном состоянии, так как молекулы детергента образуют защитный слой на очищенной тарелке и вокруг комков грязи.
Мыльные пузыри. Мыльные пузыри на вид достаточно прочны; если их ударить, они подскакивают и, если испарения нет, сохраняются довольно долго. Происходит это по следующим причинам:
1) Молекулы мыла собираются с обеих сторон пленки, причем их концы, имеющие сродство к воде, направлены внутрь, а инертные — наружу, создавая нейтральную поверхностную оболочку[79] которая ни к чему не прилипает.
2) Мыльный раствор представляет собой неоднородную смесь, образующую пленку со слегка изменяющимся поверхностным натяжением; это позволяет пленке выдерживать нагрузку и восстанавливать свою первоначальную форму. В то же время чистая жидкость редко образует устойчивые пузырьки или пену, поэтому остерегайтесь пить воду из прудов, на поверхности которых бывает пена.
Водонепроницаемость. Чтобы плащ не пропускал воду, поверхностное натяжение не должно позволять воде проникать в поры. Для этого поры не закрывают, а покрывают волокна воском, чтобы создать большой краевой угол при контакте с водой. Тогда, если поры малы, вода в них не проникает, а задерживается выпяченной поверхностной пленкой.
Опыт 15. На фиг. 127 схематически изображена вода, политая на волокна, имеющие покрытие, — увеличенная схема зонта или палатки под дождем. Схему можно показать через проекционный фонарь; тот же эффект можно продемонстрировать на небольшом решете с металлической сеткой. Если проволочки решета покрыть парафином, чтобы они сделались несмачиваемыми, решето будет удерживать осторожно налитую на него воду. Но стоит снизу к решету прикоснуться влажным пальцем, как оболочка воды разрушится и начнется дождь. Таким же образом палатка начинает протекать, если кто-нибудь из любопытства прикоснется изнутри к полотнищу мокрой головой.
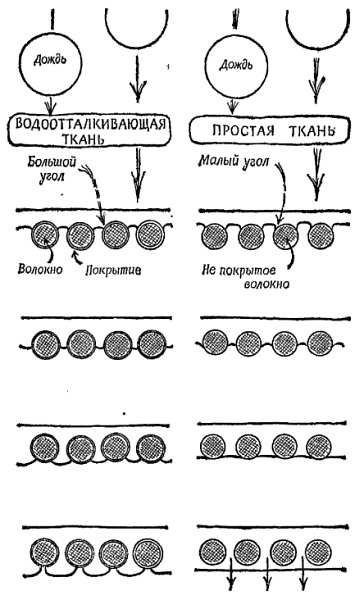
Фиг. 127. Водонепроницаемость и смачивание.
В сильно увеличенном виде показаны в разрезе волокна ткани для зонтов или брезента для палаток с налитой на них водой. Поры не закрыты, но когда на волокна нанесено покрытие, создающее большой краевой угол (между водой и покрытием), вода выпячивается между волокнами и удерживается поверхностным натяжением.
Химия поверхностных явлений и чудеса в горном деле
Химия веществ, изменяющих краевой угол, творит поистине чудеса в технике и в быту. Моющие средства помогают прачкам, протирщикам окон и мойщикам овец. Ничтожные добавки к каплям от насморка позволят им проникнуть в носу пациента сквозь барьер, созданный волосками слизистой. Водоотталкивающие вещества делают непромокаемыми плащи и промышленные фильтры. Наконец, избирательные смачивающие вещества отделяют ценные минералы от бесполезной породы. Для этого породу, содержащую металлическую руду, размалывают, а затем полученную пыль размешивают в чане с водой. В воду добавляют соответствующее вещество, которое покрывает частички руды, делает их несмачиваемыми и позволяет им легко «плавать»[80], тогда как бесполезный песок намокает и опускается на дно в виде грязи, которую затем удаляют. Поверхность соприкосновения воды с открытым воздухом слишком мала, чтобы на ней могли собраться все несмачиваемые водой частицы руды, поэтому через взвесь продувают пузырьки воздуха, которые создают пену и поднимают руду кверху, где ее и собирают. Такая схема «пенной флотации» отнюдь не бесполезная игрушка. Этот процесс успешно применяется в горной промышленности, и с его помощью разделяют миллионы тонн руды в день. Подбор веществ, которые будут охватывать руду защитной оболочкой и не будут защищать песок, требует от химиков большого искусства. Более того, некоторые вещества даже отделяют в смешанных рудах один металл от другого; для этого требуется еще более тонкая химия. Сейчас пенная флотация находит много новых применений, например отделение грибка спорыньи от спелого зерна, сортировка гороха для консервирования, улавливание потерянных частичек каучука, но основное ее применение — это разделение свинца, цинка, серебра и т. д., которое выросло в мощную промышленность, где главным работником служит поверхностное натяжение.
Амебы и поверхностное натяжение
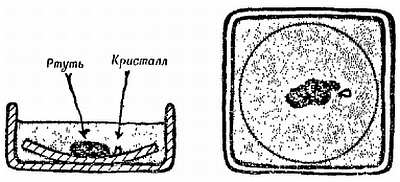
Каким образом мелкие простейшие организмы, живущие в воде, передвигаются и находят пищу? Некоторое представление об этом можно получить с помощью грубых химических моделей, вроде движущейся зигзагами «лодки» из камфары или искусственной ртутной «амебы» (фиг. 128).
Фиг. 128. «Амеба» из ртути.
На небольшую лужицу ртути на часовом стекле в блюдце наливают разбавленную азотную кислоту. Около ртути помещают кристалл бихромата калия. Ртуть начинает двигаться подобно амебе; ее перемещения вызваны изменениями поверхностного натяжения вследствие химических или электрических эффектов.
Настоящая амеба тоже образует такие неправильные выступы и впадины, возможно также используя изменения поверхностного натяжения.
ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
Изменение свойств поверхностной оболочки воды. Здесь приведены некоторые красивые опыты, демонстрирующие изменения поверхностного натяжения.
Опыт 16. Швейную иглу или тонкий листочек металла можно заставить плавать в блюдце с водой. Если поверхностное натяжение уменьшить, предмет потонет. Попробуйте добавить к воде спирт или мыло.
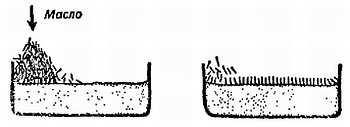
Опыт 17. Посыпьте поверхность чистой воды несмачиваемым порошком (сажей, тальком или ликоподием). По движению порошка можно обнаружить ослабление поверхностного натяжения. Если на поверхность нанести капли спирта, порошок разбежится в стороны (фиг. 129).
Фиг. 129. Капли спирта падают на воду, которая посыпана порошком.
Обычное объяснение таково: спирт образует слабую оболочку, и порошок растаскивается в стороны прочной оболочкой чистой воды. Но иногда предпочитают говорить, что молекулы спирта, растекаясь, создают «поверхностное давление» и расталкивают порошок. Хотя эти взгляды различны, любой из них полезен для объяснения опытов.
Опыт 18. На посыпанную порошком чистую поверхность воды нанесите оливковое масло. Его требуется так мало, что достаточно погрузить в масло спичку и затем вытереть ее насухо. Даже палец, потертый о волосы, соберет достаточное количество природного жира. В предыдущем опыте после действии спирта поверхность восстанавливается, но влияние жира остается, поэтому этот опыт требует очень чистых, свободных от жира приспособлений. Мыло и слюна действуют подобно спирту.
Личинки москитов живут в прудах и просовывают наружу расположенные в хвосте дыхательные трубки. Масло, нанесенное на поверхность, проникает в эти трубки и убивает личинку. Прежнее объяснение, согласно которому масло настолько ослабляет поверхностную пленку, что личинки не могут висеть на ней и дышать, следует отбросить.
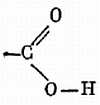
Опыт 19. Небольшая капля масла, помещенная в большое блюдо со слегка припудренной чистой водой, очень быстро растекается в большое круглое пятно, которое потом сохраняет свои размеры. Так ведут себя растительные масла; они являются «жирными кислотами», и у них один конец, кислотный, имеет сродство к воде:
(Молекулы минерального масла, у которых инертны оба конца, видимому, располагаются по поверхности воды и движутся подобно двумерному газу, растекаясь случайным образом.) Кажется, что пленка масла сверху «давит» на поверхность раздела.
Такое объяснение представляется более правильным, чем «ослабление поверхностного натяжения воды». Сейчас это внешнее давление измеряют с помощью точных весов, которые взвешивают давление пленки масла на подвижную перекладину.
Применение длинных молекул масла
Смазывание. При смазывании высокоскоростных подшипников молекулы растительного масла присоединяются к металлу (металл вытесняет водород из кислотного конца молекулы масла), и масло образует мономолекулярные бархатистые «ковры», инертные внешние слои которых удобно скользят друг по другу. (К смазке добавляют также минеральные масла, чтобы между этими «коврами» получить инертные масляные «ролики».) При крайне небрежном обращении с металла сдираются даже бархатистые монослои; тогда движущиеся металлические детали с большой силой прилипают друг к другу («схватываются»), и это чревато неприятными последствиями.
Ланолиновый жир пристает к коже и проникает в нее, перенося с собой необходимые медикаменты, тогда как инертные минеральные масла беспорядочно распределяются на коже в виде жирных комков; поэтому избегайте мазей, изготовленных не на ланолине, а на минеральных маслах.
К коже пристают и молекулы хорошей ваксы, а парафин (разновидность минерального масла с более длинной цепью) образует беспорядочные пятна[81]. Полировка обуви щеткой облегчает прилипание и распределяет молекулы по поверхности более равномерно.
Укрощение штормов в море. Укрощение бурных морей с помощью масла — отнюдь не сказка. Достаточно вылить за борт совсем немного подходящего масла, чтобы оно распространилось по большой поверхности. Ветер пытается создать большие волны, раскачивая небольшую рябь, масло сдувается в лужи неправильной формы, и различие поверхностного натяжения помешает действию ветра, создав своего рода поверхностное трение. Поэтому в таком месте образуется меньше больших волн. А волны, приходящие издалека, не смогут по крайней мере создать разрушительных гребней. Поверхностное натяжение играет важную роль при образовании вспененных гребней, и масло может помешать их образованию.
ДЕМОНСТРАЦИОННЫЕ ОПЫТЫ
Опыт 20. Как изменится поверхностное натяжение при повышении температуры? Попробуйте нагреть припудренную поверхность воды, поднося к ней раскаленную докрасна кочергу.
Опыт 21. Распылите по чистой воде камфару. Каждая частица совершает беспорядочные движения. Это происходит потому, что камфара медленно растворяется в воде, ослабляя поверхностную оболочку. Каждую частицу вперед тянет чистая вода, а назад — слабее вода с камфарой, поэтому частица плывет вперед, подобно лодке, крутясь и поворачиваясь из-за своей неправильной формы. Попробуйте добавить еще немного масла. Движение камфары сразу прекратится. Не правда ли, это красивый несложный опыт, немного похожий на детскую забаву? Однако эта забава играет важную роль в одном из великих экспериментов атомной физики — в измерении размеров молекулы.
Размер молекулы
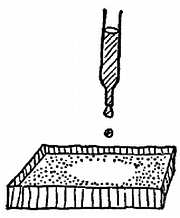
Шестьдесят лет назад лорд Рэлей наблюдал за растеканием масла по воде. В то время, когда ученые строили различные предположения о размерах молекул, он догадался, что самый тонкий слой масла, который может полностью покрыть водную поверхность, будет иметь толщину как раз в одну молекулу, и решил определить эту толщину. Рэлей представил себе растекание капли масла как хаотическое движение молекул, карабкающихся друг на друга и сваливающихся назад, пока каждая не достигнет поверхности воды и не сможет прицепиться к воде (эти масла состоят из молекул с длинной цепью, на одном конце которых находится химическая группа, имеющая сродство к воде). Как только все молекулы масла расположатся таким способом, они будут держаться в виде мономолекулярного покрова и перестанут стремиться к дальнейшему растеканию (фиг. 130).
Фиг. 130. Масло на воде.
Капля масла, нанесенная на чистую поверхность воды, растекается и покрывает ее слоем толщиной в одну молекулу. Молекулы масла, вероятно, стоят «дыбом» подобно ворсу на ковре.
Если масла как раз достаточно для данной поверхности воды, слой будет иметь толщину в одну молекулу, и все молекулы будут плотно упакованы по вертикали, подобно ворсинкам бархата. При меньшем количестве масла останутся участки открытой воды. Если масла будет
…???… супе)[82].
Лорд Рэлей вымыл и заполнил водой круглый большой таз, имевший 82 см в поперечнике. На поверхность воды он поместил взвешенную каплю масла и наблюдал, как оно растекается и закрывает всю поверхность. Затем он опять взял чистую воду и каплю меньшего размера, затем еще меньшую, пока не дошел до такой капли, которая уже не могла полностью закрыть всю поверхность. Как же он обнаружил, что закрыта не вся поверхность?
Если перед опытом распылить на поверхности порошок, можно изменить свойства поверхности. Поэтому Рэлей после масла распылял камфару (помните детскую забаву?). Пока поверхность воды была полностью покрыта маслом, камфара не находила чистой воды, по которой она могла бы танцевать, но когда капля масла была мала, на поверхности открывались участки чистой воды.
Условия приведенной ниже задачи 5 следуют за ходом вычислений Рэлея. Используя результаты его измерений, определите размеры молекул масла.
Задача 5. Измерение размеров молекулы
Рэлей наносил каплю оливкового масла на чистую воду в большом сосуде. Для простоты примем, что сосуд был прямоугольным с размером зеркала воды 0,55 м х 1,00 м (это даст ту же площадь, что и в круглом тазу, взятом Рэлеем).
Движение камфары показало, что масла как раз достаточно для покрытия всей поверхности (капля масла весит 8/10 мг, или 0,00000080 кг). Плотность масла равна 900 кг/м3 (что составляет 0,90 от плотности воды). Предположим, что плотность остается такой же и в очень тонкой пленке.
(Помните, что поскольку масло менее плотно, чем вода, его объем должен быть больше объема той же массы воды.)
а) Определите толщину масляной пленки, образующейся при растекании капли по воде.
б) Допустим, что Релей был прав и пленка, достаточная для остановки движений камфары, имеет толщину в одну молекулу. Поверим химикам, что это масло имеет «длинные» молекулы, один конец которых сильно притягивается водой. Какой вывод можно сделать из вопроса (а) относительно размеров молекул?
Длина молекул очень мала; чтобы образовать линию в 1 см их требуются миллионы. В те времена, когда Рэлей производил свои измерения, ученые делали грубые, поспешные предположения о размере и массе молекул; их косвенные догадки основывались на трении в газах, на рассеянии солнечного света в небе молекулами и на некоторых сомнительных электрических аргументах. Здесь же был поразительно простой эксперимент и, вероятно, надежный.
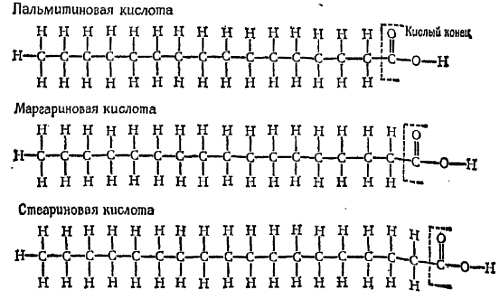
С тех пор метод был улучшен и обобщен многими, особенно Ленгмюром в США. Оливковое масло, которое применял Рэлей, было неопределенной смесью маслянистых веществ. Позднейшие исследователи применяли чистые химические соединения, часто используя несколько членов «гомологического ряда» (или, иначе, химической семьи). Например, Ленгмюр применял «жирные кислоты». Их получают из природных жиров и масел, и они дают мыло, соединяясь с натрием или калием. Они имеют длинные молекулы с одним инертным, а другим «кислым» концом, который притягивается водой. Существует целый ряд таких соединений, причем молекула каждого представителя этого ряда больше своего предшественника на один атом углерода и два атома водорода. Очень давно химики изобразили молекулы различных членов этих рядов структурными формулами, подобными трем приведенным на стр. 222.
Это были лишь догадки, основанные на химических данных, но они наводили на мысль о длинных цепных молекулах, удлиняющихся на группу СН3 при переходе от одного члена семьи к другому.
Задача 6 основана на усовершенствовании метода Рэлея, осуществленном Ленгмюром, Адамом и другими.
Задача 6. Точное измерение размеров молекул
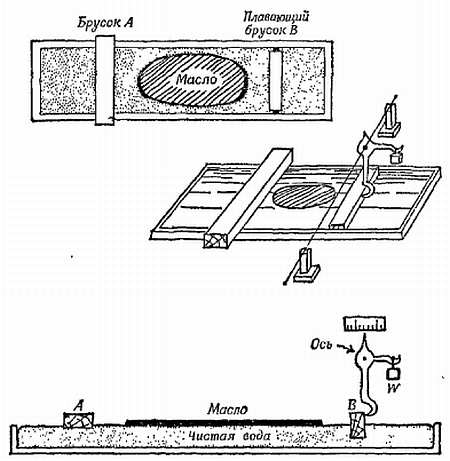
Адам использовал прямоугольную ванну шириной 0,14 м и длиной 0,5 м. Ванна была наполнена водой до краев; исследуемая область ограничивалась положенными сверху на расстоянии около 0,4 м друг от друга брусками А и В (фиг. 131).
Фиг. 131. Упрощенный рисунок прибора Адама.
Пленка масла ограничена брусками А и В.
Брусок В был подвижен; он свободно плавал по воде и был соединен с измерительным устройством, которое имело пружину или грузик и позволяло обнаружить любое горизонтальное смещение бруска, а также предотвращало его случайные движения. Брусок А клали поперек ванны, он имел выступающие края и его можно было перемещать рукой. Ванну и бруски покрывали воском, чтобы уровень воды мог подниматься немного выше краев, так что бруски А и В отсекали центральную часть поверхности.
Располагая сначала брусок А далеко от бруска В, Адам помещал на водную поверхность между брусками небольшое измеренное количество пальмитиновой кислоты. Брусок В не смещался. Затем передвигался брусок А, собирая пленку масла на все меньшей и меньшей площади, пока вдруг брусок В не испытывал заметного толчка; это позволяло думать, что молекулы вобрались в сплошной слой. (В реальных экспериментах толкающее усилие не возрастало абсолютно резко от нуля до полного значения. Оно появлялось при определенной величине поверхности и быстро росло при дальнейшем перемещении, достигая постоянной величины, после которой дальнейшее сближение, вероятно, заставляло «слой» изгибаться. По графику легко было найти момент, в который появляется значительное усилие.)
Для нанесения жирных кислот на поверхность вода Адам растворял их в бензоле и наносил несколько капель раствора. Бензол быстро испарялся.
Вот типичные результаты измерений (это не подлинные данные Адама, но они основаны на его записях):
Бензольный раствор. Состав: 4 г пальмитиновой кислоты растворены в 996 г бензола. Следовательно, каждый килограмм раствора содержит 0,004 кг пальмитиновой кислоты.
Размер капель. В сосуд капают 100 капель раствора и сосуд взвешивают.
Масса 100 капель раствора равна 0,33 г, или 0,00033 кг.
Основной опыт. На воду наносят 5 капель раствора. Когда бензол испаряется (остается невидимая нерастворимая поверхностная пленка пальмитиновой кислоты), брусок А двигают по направлению к бруску В. Последний испытывает сильный толчок, когда расстояние между А и В составляет 0,23 м. В этот момент поверхность воды между брусками составляет 0,23 м в длину и 0,14 м в ширину.
Плотность пальмитиновой кислоты (в виде жидкости) составляет 850 кз/м3, (0,85 по сравнению с водой).
Задание: предполагая, что пленка пальмитиновой кислоты имеет ту же плотность, с помощью приведенной ниже инструкции определите размеры ее молекул.
1) Рассчитайте длину молекул, используя снова предположение Ралея.
[Примечание. Даже одна арифметическая ошибка может превратить решение этой задачи в бессмыслицу. Расчет объема взятого масла (пальмитиновой кислоты) является простой задачей на дроби, подобно расчету рецепта теста для пирога или разбавления соков. Он требует знания элементарных арифметических правил и уверенности. Чтобы избежать ошибок, лучше производить его по стадиям, например, по количеству раствора (5 капель), нанесенного на воду, рассчитать:
а) массу нанесенного на воду раствора;
б) массу пальмитиновой кислоты, содержащейся в этом количестве раствора;
в) объем, который займет эта масса пальмитиновой кислоты (850 кг занимают 1 м3, следовательно…).]
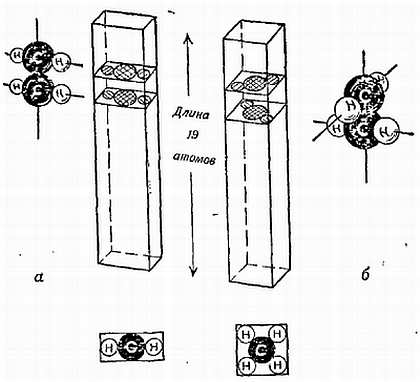
2) Оцените ширину молекул с помощью следующего рассуждения. Цепная формула изображает молекулу в 19 атомов длиной и только несколько атомов шириной. Трудно догадаться о форме поперечного сечения молекулы; атомы Н должны быть меньше, чем атомы С в цепи. Возможно, что поперечное сечение содержит 3 атома в ширину и один в толщину, либо чередующиеся связи могут колебаться в разные стороны, делая поперечное сечение квадратом, скажем, со сторонами по 3 атома.
В качестве грубого предположения[83], допустим, что поперечное сечение является квадратом со стороной от 1,5 до 3 атомов. Забывая, что разные атомы имеют разные размеры, мы заключаем, что ширина молекулы должна быть где-то между 1/10 и 1/5 ее 19-атомной длины. Глупо было бы пытаться сузить эти пределы (фиг. 132).
Фиг. 132. Схема к рассуждению о форме молекулы пальмитиновой кислоты.
Современные химики, группируя атомы углерода и водорода в молекулы, приписывают им четкие размеры, причем углероду намного больше, чем водороду. Здесь показаны ранние предположения о размерах атомов, и атом С изображен лишь немного больше атома Н. Каково поперечное сечение: «продолговатое» (а) или «квадратное» (б)?
Рассчитайте объем молекулы пальмитиновой кислоты, для этого возьмите длину, полученную в п. 1, и считайте поперечное сечение квадратом со стороной, равной 1/10 длины. Повторите вычисление с другим пределом — 1/5 длины.
3) Принимая плотность равной 850 кг/м3, рассчитайте массу одной молекулы на основе каждого предположения (1/10 и 1/5). (Если 850 кг занимают 1 м3, то…)
4) Простые химические измерения (анализ путем сжигания и взвешивания и т. д.) говорят, что масса молекулы пальмитиновой кислоты в 256 раз больше массы атома водорода. (Химические опыты не могут дать действительных значений масс отдельных атомов и молекул, но позволяют легко определить их относительные величины.) На основании полученного вами результата рассчитайте массу одного атома водорода (при каждом предположении — 1/10 и 1/5).
5) На основании п. 4 скажите приблизительно, сколько атомов должно быть в 1 кг водорода (около 11 м3 при атмосферном давлении).
6) Сейчас существуют совершенно другие способы определения массы атома водорода (косвенные, но надежные, использующие электрический заряд электрона или некоторые измерения радиоактивности). Они дают:
МАССА АТОМА ВОДОРОДА = 1,66∙10-27 кг.
Предположите, что правильно это значение, и проделайте вычисление в обратном порядке. Что теперь можно сказать о форме молекулы пальмитиновой кислоты? Были ли допущения 1/10 и 1/5 близки к истине?
(Примечание. Проделать детально всю работу в обратном порядке может оказаться утомительным. Можно ограничиться сокращенными выкладками.)
Задача 7. Цепные молекулы
Измерения с помощью бруска и весов, подобные описанным в задаче 6, дают следующие оценки для длины молекул нескольких членов ряда жирных кислот. Длина дается в специальных единицах (часто используемые в атомной физике единицы Ангстрема, равные 10-10 м).
(Примечание. Указанное число групп включает первый атом углерода с тремя атомами водорода.)
Подтверждают ли эти опыты идею о цепных молекулах? Проанализируйте их о помощью графика.
Физическая проверка химической картины
Только плохой преподаватель льстит себя надеждой, что способен объяснить, что такое молекулы масла, с помощью одних разговоров о «цепях связей» или «ворсе бархата» в тонких пленках. Однако если после вычислений, подобных приведенным выше, у вас появилось чувство, что вы что-то понимаете, то вы делаете гениальные успехи в науке. Использованные нами структурные формулы были остроумными догадками, сделанными по косвенным химическим соображениям. Они оставались совершенно непроверенными, пока метод Рэлея не дал в высшей степени удовлетворительное подтверждение существования длинных тонких молекул с одинаковым увеличением длины на каждую группу СН2.
Все же рассуждения Рэлея допускали определенный риск; были желательны независимые измерения. В наше время еще более тонким средством измерения размеров молекул стали рентгеновские лучи. Превращая масла в воски путем замораживания, мы можем заставить слои молекул в кристаллах отражать рентгеновские лучи и по отражению рентгеновских лучей можем определить расстояние между слоями (или размер молекул), подобно тому как физики во времена Рэлея могли определить расстояние между жилками на крыльях бабочки по цветам отраженного света[84].
Некоторое понятие об этих «эффектах дифракционной решетки» будет дано в последующих главах. Рентгеновские измерения с удовлетворительной точностью подтвердили догадку Рэлея и дали дополнительные сведения о размерах и строении молекул.
Если теперь вернуться к вопросам смачивания и водонепроницаемости, то можно оценить количества веществ, требуемые для придания материалу нужных свойств. Вероятно, достаточен слой толщиной в одну молекулу, поэтому потребные количества минимальны. О мономолекулярных слоях уже думают как о реальных, знакомых вещах. Они слишком тонки, чтобы их видеть с помощью обычного света, хотя их можно обнаружить с помощью рентгеновских лучей или дифракции электронов. Однако Блоджетт разработал метод, в котором наносится слой за слоем на стеклянную пластинку, причем осаждаются сразу по два слоя, когда пластинку погружают в воду с плавающим мономолекулярным слоем. Погружение повторяют до тех пор, пока толщина не может быть измерена обычными приборами, которыми измеряют толщину бумаги, и не будут осуществлены, наконец, прямые измерения. (Такие пленки представляют собой ранний способ, нанесения на стекла покрытий, уничтожающих блики, — просветление оптики. Линзы современных фотоаппаратов имеют покрытие, нанесенное другим методом — испарением в вакууме.)
Эту главу мы начали с простых наблюдений и ввели некоторые наименования, затем позаимствовали идеи о молекулах и сделали некоторые предварительные предположения. Потом провели дополнительные опыты и пришли к разнообразным результатам, простирающимся от сугубо практических вещей, вроде мыльной пены и чистки обуви, до измерения длины молекулы.
Сейчас физика и химия поверхностей образуют самостоятельную отрасль науки.
Все мы знаем, что если надуть пластиковую бутылку горячим воздухом, крепко-накрепко закрыть крышкой, а потом охладить, то бутылка сожмётся. Причина этого лежит в физике 8-го класса, или, если точнее, в законе Гей-Люссака, утверждающем, что отношение объёмов при разных температурах равно отношению абсолютных температур. То есть ещё со школьных времён (а может и раньше) нам всем известно, что при нагревании некоторого количества газа его объём увеличивается, а при охлаждении — уменьшается.
А что насчёт того, из чего этот газ состоит? Увеличивается ли объём самих частичек газа, то есть размер атомов и молекул? Банальный ответ на этот банальный вопрос под катом.

Ха-ха, попались!
Ответ на этот вопрос весьма прост: как мы определим
объём
размер частиц (что такое размер атома/молекулы в зависимости от температуры), такой ответ мы и получим. Поскольку атомы по-своей сути — это одноатомные молекулы, то дальше мы будем называть все эти частицы единым термином «молекула«.
Если взять бутылку с газом, и из этой бутылки взять одну единственную молекулу, то окажется, что для неё не возможно (по-честному) даже принципиально измерить температуру. Частица находится в каком-то конкретном (квантовом) состоянии, которое мы можем определить и измерить, но при этом мы не сможем засунуть
ей в
в неё термометр и узнать сколько там у неё градусов. Связанно это с тем, что «температура» — это свойство макроскопических (т.е. больших) систем, состоящих из большого числа частиц. А значит если молекул в системе мало, то и измерять у этой системы нечего. «Большое число частиц», конечно, это плавающее понятие, но обычно оно измеряется в молях, или в числах Авогадро (), поэтому очевидно, что одна молекула горааааздо меньше этого порядка величин, а значит само понятие температуры не применимо к одной, двум, да даже десяти молекулам.
Что такое температура?
Но что вообще такое температура? Ещё со школы мы знаем, что есть т.н. абсолютная температура T, измеряемая в градусах Кельвина. Именно она стоит во всех газовых законах, в частности в уравнении Менделеева-Клайперона.
Для забывших, как выглядит уравнение Менделеева-Клайперона
Это уравнение имеет вид , где P — давление, V — объём, n — количество вещества (в молях), R = 8.314 Дж/(моль · К) — универсальная газовая постоянная, а T — абсолютная температура в Кельвинах (К).
Абсолютная температура связанна с относительной температурой t, измеряемой в градусах Цельсия, как , и абсолютный ноль (T=0, или же
) — это недостижимая величина. Ещё всем в голову вбивают мантру:
абсолютная температура является мерой средней кинетической энергии молекул.
Но эта мантра не объясняет, что же именно из себя представляет температура.
Попробуем разобраться. Начнём с простого примера. Закроем глаза и представим себе Африку: жаркую, солнечную, заполненную равнинными саваннами, и с горой Килиманджаро торчащей посередине. А ещё там есть слоны.
Каждый слон имеет определённую (большую) массу, и поэтому любое поднятие своей туши из равнинной местности в горную — это большая затрата энергии.
Представим, что слоны голодные, поэтому энергии у них мало. Будучи слоном, я бы в таком состоянии не попёрся бы в гору, а тусовался бы в саванне. В горы бы я ходил только по очень-очень большой нужде. В результате, если бы мы сняли фотографию Африки со спутника, она бы выглядела примерно так, как показано на картинке ниже: много-много слонов на равнине, и очень мало смелых и отчаянных в горах, причём, чем выше — меньше вероятность найти слона.

А теперь представим, что слоны хорошенько поели, да ещё какой-нибудь [Роскомнадзор] ещё для скорости им в еду подсыпали, так что энергии у слонов много. В этом случае, что равнина, что гора, слоны будут туда переться без особой устали, поэтому теперь вероятность отыскать слона на равнине и в горах будет отличаться уже меньше, чем в предыдущем примере (см. картинку ниже), хотя всё ещё будет сохраняться правило: чем выше на гору — тем меньше слонов.

Эти два примера весьма точно иллюстрируют случаи газа с низкой (первый) и высокой (второй) температурой. У каждой молекулы (слона) есть какая-то своя энергия, в нашем примере — это гравитационная энергия , где m — масса, g = 9.8 м/c2 — ускорение свободного падения, а h — высота над равниной. Из энергии каждой конкретной частицы (места, где нашли слона) мы не можем ничего сказать о том, как всех слонов покормили
в целом
, но именно то, сколько на всех выделили еды, или другими словами, сколько энергии вкачали в среднем во всю систему, даст нам распределение слонов по ландшафту Африки. Собственно, температура в наших примерах — это общая величина накормленности всех слонов во всей Африке. Именно поэтому мантра из школьного курса физики и оказывается верна — температура — это то, сколько в среднем энергии (причем, как кинетической, так и потенциальной) имеет каждая молекула, или, что в данном случае эквивалентно, какова вероятность найти частицу с очень большой энергией. Но более точно, температура — это параметр распределения Больцмана (или Гиббса) — распределения частиц по состояниям с различной энергией. Это распределение говорит нам, что чем выше температура, тем больше высокоэнергетических молекул относительно числа низкоэнергетических мы имеем.
Распределение Больцмана
Собственно, распределение Больцмана имеет вид:
где n(E) — это число частиц с энергией E, R — универсальная газовая постоянная (см. предыдущий спойлер), а T, само собой, температура.
В примере же со слонами мы иллюстрировали т.н. барометрическую формулу: частный случай распределения Больцмана, показывающий как меняется давление газа с увеличением высоты:
где P(h) — это давление на высоте h, , а M — это молярная масса газа.
Растут ли атомы от температуры?
Теперь, собственно, можно перейти к вопросу: а растут ли, например, атомы при росте температуры. Само собой, каждый конкретный атом находится в каком-то квантовом состоянии, поэтому от температуры его размер не зависит, но вот средний размер всех атомов в сосуде с газом от той самой температуры зависеть уже будет.
Представим себе, например, атом водорода: тяжёлый протон, а вокруг него летает электрон. Поскольку протон положительный, а электрон отрицательный, то один притягивает другой по закону Кулона, который выглядит точно так же как ньютоновская гравитация, поэтому в этом смысле атом вполне себе напоминает, например, Солнце и Землю, летающую вокруг него. Только, как говорит нам (далеко не полностью удачная, см. например, тут) атомная модель Бора, в отличие от системы «звезда + планета», электрон летает вокруг ядра только по орбитам определённого радиуса.
Так или иначе, чем больше энергии мы закачиваем в атом водорода, тем более широкая орбита будет доступна электрону для полёта вокруг ядра. Естественно, если мы возьмём один конкретный атом, мы можем узнать его орбиту, и она ничего нам о температуре всех атомов не скажет. Но вот если мы измерим радиусы у множества атомов, а потом усредним полученные величины, то у нас действительно возникнет зависимость от температуры для этого среднего числа. В результате получится что-то типа такой картинки:

Из неё видно, что чтобы начать замечать хоть какие-то изменения в размере электронной оболочки, нужно ооочень сильно нагреть атом (в данном случае до более 10000 градусов). Это в целом общий тренд.
Как была посчитана эта зависимость
Подробнее о формулах можно узнать в этом посте.
Если кратко, то радиус орбиты (R) в зависимости от главного квантового числа n=1,2,3… — это
где R0=5.3×10−11 метра − это боровский радиус. Энергия (E) же орбиты имеет вид
где Eh= 4.3597447222071(85)×10−18 Джоулей − это энергия Хартри.
Далее используя распределение Больцмана для одной частицы, мы можем посчитать среднее значение радиуса от температуры как
Знаменатель у нас появляется из-за того, что полная вероятность всех исходов измерений должна быть равна единице.
Иными словами,
ответ на вопрос поста: да, при нагревании электронные оболочки атомов (и молекул) в среднем расширяются
. Но, это увеличение очень маленькое, и требует нагрева до очень высоких температур, к которым мы в обыденной жизни не привыкли.
Растут ли молекулы от температуры?
Теперь зададимся вопросом: а что если наша молекула составлена не из одного, а из двух, трёх или более атомов? Можем ли мы что-то сказать о межатомных расстояниях в ней, как ведут они себя при повышении температуры? Для простоты, естественно, ограничимся двухатомными молекулами, кои, в частности, составляют как минимум 98.7 % нашей атмосферы (азот и кислород).
У нас есть один атом, у нас есть второй атом: ммммм, и расстояние между ними, обозначим его как R. Как ведёт себя потенциальная энергия взаимодействия этих атомов в зависимости от R?
- Если мы разведём атомы оооочень далеко друг от друга, то химическая связь между ними давно будет разорвана. Поэтому особой разницы от того, что расстояние мы увеличим от «очень много» до «очень много и ещё чуть-чуть», мы не заметим. Иными словами при R → ∞ у нас должна быть горизонтальная асимптота.
- Если же, наоборот, мы будем пытаться впихнуть один атом в другой (R → 0), то в какой-то момент мы выгоним из пространства между этими атомами все электроны, ибо те не идиоты, чтобы тусоваться в токсичной высокоэнергетической атмосфере, и у нас останутся два голых положительно заряженных ядра, отталкивающиеся друг от друга через Кулоновскую силу. Т.е. при R → 0 у нас будет вертикальная асимптота, стремящая потенциальную энергию взаимодействия атомов в высокоэнергетическую бесконечность.
- Ну и, логично, что не будь какого-то минимума на этой потенциальной кривой между R=0 и R → ∞, то самих молекул о которых мы говорим, не существовало бы.
В итоге мы понимаем, что кривая потенциальной энергии взаимодействия имеет следующий вид:

Атомы в молекуле всегда колеблются, даже при абсолютном нуле, когда никакой лишней энергии не осталось. Из-за принципа неопределённости они не могут просто скатиться в минимальную по энергии точку на потенциале и
сдохнуть
лежать, свернувшись калачиком: им приходится совершать т.н. нулевые колебания. Если же энергия у них выше, то и колеблются они с большей амплитудой. Поэтому возникает вопрос: а как конкретно колеблются атомы?
Если бы слева и справа от точки минимума потенциал был одинаков, как, например, в случае закона Гука, то атомы во время колебаний отклонялись бы в область малых значений межатомных расстояний ровно то же количество времени, сколько и в область больших значений. В этом случае бы среднее значение межатомного расстояния при любой температуре было бы равно значению расстояния в точке минимума. Иными словами, если бы мы взяли газ, и в любой момент времени сфоткали все молекулы, а потом посчитали бы среднее значение для всех расстояний между атомами, то в итоге получили бы расстояние в точке минимума.
Но реальность у нас другая: слева от точки минимума (при R → 0) у молекулы стоит жёсткая стенка, а справа (при R → ∞) — мягкий диван. Вопрос: где будет больше времени проводить молекула: долбиться о стенку, или валяться на диване? Правильно: конечно на диване. Иными словами, распределение расстояний в молекуле, что при абсолютном нуле, что при какой-то температуре, будет несимметричным, поэтому среднее значение расстояний будет сдвинуто в сторону больших расстояний относительно минимального. Мало того, при повышении температуры, т.е. когда мы будем закачивать больше кинетической энергии в систему, увеличивая амплитуду колебаний, молекула будет видеть гораздо более жёсткую стенку, и гораздо более мягкий диван. Поэтому среднее значение межатомных расстояний будет расти с ростом температуры, а значит и средний размер молекул, причём всех, не только двухатомных, будет увеличиваться.
К сожалению, чтобы посчитать этот рост среднего расстояния, потребуется много больше усилий, чем в случае атома водорода. Но можно пойти другим путём, и поискать, а не исследовался ли этот вопрос в экспериментах?
И порывшись на просторах этих наших Интернетов, можно набрести на следующую работу: J. Chem. Phys. 79, 170 (1983). В ней делали эксперимент буквально описанный выше:
- брали кучу молекул углекислого газа (CO2) и нагревали их до разных температур, в диапазоне температур от комнатной (300 K ≈ 25oC) до «ай как горячо» (1000 К ≈ 730oC ),
- при каждой выбранной температуре делали «фотку» всех молекул при помощи электронов (этот метод зовётся газовой электронографией, о нём можно немного почитать здесь),
- ну а дальше буквально измеряли средние значения для межатомных расстояний на каждой фотке.
В результате они, в частности, получили следующую зависимость средней длины двойной связи C=O в молекуле углекислого газа (O=C=O):

Из графика видно, что при нагреве от комнатной температуры до 1000 градусов К это среднее значение выросло почти на 0.004 Å (1 ангстрем, Å, = 10—10 метров). Конечно, в наших привычных величинах это очень мало, но сама длина связи C=O в этой молекуле составляет 1.2 Å, так что это рост на почти 0.3 %! Вполне себе заметная величина при нагреве, достижимом привычными средствами (например, газовой плитой).
Зачем это вообще знать?
Да хотя бы просто ради любопытства. Разве не прикольно поспорить с коллегой на чашку кофе, что при нагреве контейнера с едой в микроволновке помимо объёма газа увеличится и размер частиц газа? Ну и в практическом смысле это тоже важно. Все эти температурные расширения/уменьшения всяких макроскопических объектов, таких как рельсы, провода линий электропередач, да даже крышки банки под горячей водой, работают ровно по тому же механизму, что и для молекул газа: средние межатомные расстояния увеличиваются, т.к. в систему при увеличении температуры закачивается больше энергии движения частиц. И по-моему, осознание того, что за такими обыденными явлениями стоят такие нетривиальные процессы, вдохновляет на новые подвиги и свершения.
Всех благ, и да пребудет с Вами межатомная сила.
Все мы дышим воздухом, который в основном состоит из молекул азота и кислорода с небольшими добавками других элементов. Следовательно, кислород — один из важнейших химических элементов. Кроме того, его молекулы существуют в огромном разнообразии химических соединений, используемых в повседневной жизни. Сотни страниц будет недостаточно, чтобы описать все свойства этого элемента, поэтому мы ограничимся основными фактами рассказа, а также основными характеристиками элемента: валентностью и степенью окисления кислорода, удельным весом, применение, основные физические свойства.
История открытия химического элемента
Официальная дата открытия химического элемента «кислород» — 1 августа 1774 года. Именно в этот день британский химик Дж. Пристли завершил свой эксперимент по разложению оксида ртути в герметично закрытом сосуде. В конце эксперимента ученый получил газ, поддерживающий горение. Однако это открытие осталось незамеченным даже самим ученым. Мистер Пристли думал, что ему удалось выделить не новый элемент, а составную часть воздуха. Джозеф Пристли поделился своими открытиями с известным французским ученым и химиком Антуаном Лавуазье, который смог понять, чего не смогли сделать англичане. В 1775 году Лавуазье смог установить, что образовавшаяся «составляющая воздуха» на самом деле является независимым химическим элементом, и назвал его кислородом, что по-гречески означает «образование кислот». Затем Лавуазье считал, что кислород содержится во всех кислотах. Впоследствии были выведены формулы кислот, не содержащих атомов кислорода, но название осталось.
Кислород – особенности строения молекулы
Этот химический элемент представляет собой газ без цвета, запаха и вкуса. Химическая формула — O2. Химики называют обычный двухатомный кислород «атмосферным кислородом» или «дикислородом».
Валентность и степень окисления кислорода
Валентность химического элемента означает его способность связывать с собой определенное количество атомов другого химического элемента. Атом кислорода имеет валентность два. Валентность молекулы кислорода также равна двум, поскольку два атома соединены друг с другом и обладают способностью присоединять к своей структуре другой атом другого соединения, то есть образовывать с ним ковалентную связь. Например, молекула воды H2O образуется в результате образования ковалентной связи между атомом кислорода и двумя атомами водорода.
Кислород содержится во многих известных химических соединениях. Есть даже отдельный вид химических соединений — оксиды. Это вещества, полученные при соединении с кислородом практически всех химических элементов. Степень окисления кислорода в оксидах -2. Однако в некоторых соединениях этот показатель может быть другим. Более подробно это будет описано ниже.
Физические свойства кислорода
Обычный двухатомный кислород — это бесцветный газ без запаха и вкуса. В нормальном состоянии его плотность составляет 1,42897 кг / м3. Вес 1 литра вещества чуть меньше 1,5 грамма, то есть в чистом виде кислород тяжелее воздуха. При нагревании молекула распадается на атомы.
Когда температура среды падает до -189,2 ° C, кислород меняет свою структуру с газообразной на жидкую. При этом происходит закипание. При понижении температуры до -218,35 ° С наблюдается изменение структуры от жидкой к кристаллической. При этой температуре кислород находится в виде голубоватых кристаллов.
При комнатной температуре кислород плохо растворяется в воде: на литр его приходится 31 миллилитр кислорода. Растворимость с другими веществами: 220 мл на 1 л этанола, 231 мл на 1 л ацетона.
Химические свойства кислорода
О химических свойствах кислорода можно написать целый талмуд. Важнейшее свойство кислорода — окисление. Это вещество — очень сильный окислитель. Кислород способен взаимодействовать практически со всеми известными элементами таблицы Менделеева. В результате этого взаимодействия образуются оксиды, о которых говорилось выше. Степень окисления кислорода в соединениях с другими элементами обычно составляет -2. Примером таких соединений является вода (H2O), диоксид углерода (CO2), оксид кальция, оксид лития и т.д. Но есть определенная категория оксидов, называемых пероксидами или пероксидами. Их характеристика состоит в том, что эти соединения имеют пероксидную группу «-OO-». Эта группа снижает окислительные свойства O2, поэтому степень окисления кислорода в пероксиде равна -1.
В сочетании с активными щелочными металлами кислород образует супероксиды или суперпероксиды. Пример таких образований:
- супероксид калия (KO2);
- супероксид рубидия (RbO2).
Их характеристика состоит в том, что степень окисления кислорода в супероксидах составляет -1/2.
В сочетании с наиболее активным химическим элементом фтором получаются фториды. О них речь пойдет ниже.
Высшая степень окисления кислорода в соединениях
В зависимости от вещества, с которым взаимодействует кислород, различают семь степеней окисления кислорода:
- -2 — в оксидах и органических соединениях.
- -1 — в пероксидах.
- -1/2 — в супероксидах.
- -1/3 — в неорганических озонидах (справедливо для трехатомного кислорода — озона).
- +1/2 — в солях катиона кислорода.
- +1 — в монофтористом кислороде.
- +2 — в дифторид кислорода.
Как видите, самая высокая степень окисления кислорода получается у оксидов и органических соединений, а у фторидов она даже имеет положительную степень. Не все виды взаимодействия могут быть выполнены естественным путем. Для образования некоторых соединений требуются особые условия, например: высокое давление, высокая температура, воздействие редких соединений, которые практически не встречаются в природе. Рассмотрим основные соединения кислорода с другими химическими элементами — оксидами, пероксидами и фторидами.
Классификация оксидов по кислотно-основным свойствам
Есть четыре типа оксидов:
- кислота;
- нейтральный;
- амфотерный.
- базовый;
Степени окисления кислорода в соединениях этих разновидностей равны -2.
- Кислотные оксиды — это неметаллические оксиды с высокой степенью окисления. При добавлении воды образуется кислота.
- Нейтральные оксиды — это соединения, которые не вступают в реакцию ни с кислотами, ни с основаниями.
- Амфотерные оксиды — это соединения с металлами, которые имеют низкое значение электроотрицательности. Они, в зависимости от обстоятельств, проявляют свойства как кислотных, так и основных оксидов.
- Основные оксиды состоят из металлов с низкой степенью окисления. Обычно при взаимодействии с кислотами получают соответствующую соль и воду.
Пероксиды, степень окисления кислорода в пероксиде водорода и других соединениях
Пероксиды — это соединения кислорода с щелочными металлами. Их получают путем сжигания этих металлов в кислороде. Органические пероксиды чрезвычайно взрывоопасны. Их также можно получить абсорбцией из оксидов кислорода. Примеры пероксидов:
- перекись водорода (H2O2);
- перекись натрия (Na2O2).
- пероксид бария (BaO2);
Все они объединены тем, что содержат кислородную группу -OO-. Следовательно, степень окисления кислорода в пероксидах равна -1. 
Другие типы пероксидов:
- супероксиды (супероксиды, в которых кислород окислен -1/2);
- органические озониды (соединения, имеющие в своей структуре связь -OOO-).
- неорганические озониды (крайне нестабильные соединения, содержащие в своей структуре анион озона);
Фториды, степень окисления кислорода в OF2
Фтор — самый активный элемент, известный сегодня. Поэтому при взаимодействии кислорода с фтором получаются не оксиды, а фториды. Названы они так потому, что в этом соединении окислителем является не кислород, а фтор. Фториды не могут быть получены естественным путем. Их только синтезируют, экстрагируют путем ассоциации фтора с водным раствором КОН. Фториды кислорода делятся на:
- дифторид кислорода (OF2);
- монофторид кислорода (O2F2).
Давайте подробнее рассмотрим каждое из соединений. Дифторид кислорода по своей структуре представляет собой бесцветный газ с ярко выраженным неприятным запахом. По мере охлаждения он конденсируется в желтоватую жидкость. В жидком состоянии плохо смешивается с водой, но хорошо сочетается с воздухом, фтором и озоном. По химическим свойствам дифторид кислорода является очень сильным окислителем. Степень окисления кислорода в OF2 равна +1, то есть в этом соединении фтор является окислителем, а кислород — восстановителем. OF2 очень токсичен, по токсичности превосходит чистый фтор и приближается к фосгену. Основное применение этого соединения — окислитель ракетного топлива, поскольку дифторид кислорода не взрывоопасен.
Монофторид кислорода обычно представляет собой твердое вещество желтоватого цвета. При растворении образует красную жидкость. Это мощный окислитель, чрезвычайно взрывоопасный при взаимодействии с органическими соединениями. В этом соединении кислород показывает степени окисления, равные +2, то есть в этом соединении фтора кислород действует как восстановитель, а фтор как окислитель.
Озон и его соединения
Озон — это молекула, в которой три атома кислорода связаны вместе. Обычно это голубой газ. После охлаждения он образует темно-синюю жидкость, близкую к индиго. В твердом состоянии это кристаллы темно-синего цвета. Озон имеет резкий запах, в природе его можно почувствовать в воздухе после сильной бури.
Озон, как и обычный кислород, является очень сильным окислителем. По химическим свойствам он близок к сильным кислотам. Под воздействием оксидов озон увеличивает степень их окисления с выделением кислорода. Но при этом степень окисления кислорода снижается. В озоне химические связи не такие сильные, как в O2, поэтому в нормальных условиях, без приложения усилий, он может разлагаться на кислород с выделением тепловой энергии. При повышении температуры воздействия на молекулу озона и понижении давления процесс разложения на двухатомный кислород с выделением тепла ускоряется. Также при большом содержании озона в космосе этот процесс может сопровождаться взрывом.
Поскольку озон является очень сильным окислителем и практически во всех процессах с его участием выделяется большое количество O2, озон является чрезвычайно токсичным веществом. Однако в верхних слоях атмосферы озоновый слой действует как отражатель ультрафиолетового излучения солнечных лучей.
Органические и неорганические озониды создаются из озона с помощью лабораторных инструментов. Эти вещества очень нестабильны по своей структуре, поэтому их создание в естественных условиях невозможно. Озониды хранятся только при низких температурах, так как при обычных температурах они чрезвычайно взрывоопасны и токсичны.
Применение кислорода и его соединений в промышленности
В связи с тем, что ученые однажды узнали, какова степень окисления кислорода при взаимодействии с другими элементами, он и его соединения широко используются в промышленности. Особенно после изобретения турбодетандеров в середине двадцатого века, устройств, способных преобразовывать потенциальную энергию кислорода в механическую энергию. 
В химической промышленности кислород используется в качестве окислителя углеводородов в кислотосодержащих соединениях, таких как спирты, кислоты и т.д. В медицине он используется при пониженном давлении для лечения пациентов с проблемами легких, чтобы поддерживать жизненно важные функции организма. В сельском хозяйстве небольшие дозы чистого кислорода используются для выращивания рыбы в прудах, увеличения удельного веса скота и т.д.
Кислород – мощный окислитель, без которого невозможно существование
Выше было много написано о том, какой кислород проявляет степень окисления при взаимодействии с различными соединениями и элементами, какие типы кислородных соединений существуют, какие типы опасны для жизни, а какие нет. Одно может остаться неясным: каким образом кислород при всей его токсичности и высокой степени окисления является одним из элементов, без которого невозможна жизнь на Земле? Дело в том, что наша планета представляет собой очень уравновешенный организм, который адаптировался именно к тем веществам, которые содержатся в атмосферном слое. Он участвует в цикле, который выглядит следующим образом: люди и все другие животные потребляют кислород и производят углекислый газ, в то время как растения в подавляющем большинстве потребляют углекислый газ и производят кислород. Все в мире взаимосвязано, и потеря одного звена в этой цепочке может привести к разрыву всей цепочки. Нельзя забывать об этом и заботиться о жизни на планете в целом, а не только о ее отдельных представителях.
Инфоурок
›
Физика
›Презентации›Повторительно-обобщающий урок по теме «Первоначальные сведения о строении вещества» в 7а классе

Описание презентации по отдельным слайдам:
-
1 слайд

Описание слайда:
« Сведения о веществе»
Автор: Партиспанян К. Р. –
учитель физики
МБОУ ВСОШ №2 , г. Владикавказа -
2 слайд

Описание слайда:
Домашнее задание:
Повторить § 6-12, составить сказку про приключение молекулы в телах различных агрегатных состояний. Подготовиться к зачету.
-
3 слайд

-
4 слайд

-
5 слайд

Описание слайда:
« Сведения о
веществе» -
6 слайд

Описание слайда:
Оценка за урок:
-
7 слайд

Описание слайда:
Физическое тело
Вещество
Молекулы
атомы -
8 слайд

Описание слайда:
1745 год
Михаил Васильевич Ломоносов разграничил понятия атом и молекула.
Молекулы состоят из атомов.
Молекула – наименьшая частица вещества.
Атом – мельчайшая частица химического элемента
По современной терминологии -
9 слайд

Описание слайда:
«Необыкновенное путешествие мир молекул»
-
10 слайд

Описание слайда:
Релэй Джонсон
Жан Батист Перрен
Роберт Броун -
11 слайд

Описание слайда:
Диффузия
-
12 слайд

Описание слайда:
Основные положения
молекулярно-кинетической теории
строения вещества.
Все вещества состоят из мельчайших частиц: молекул и атомов.
Частицы вещества непрерывно и хаотически движутся.
Частицы вещества взаимодействуют друг с другом. -
13 слайд

Описание слайда:
Встретились три молекулы газа, жидкости и твердого тела. Известно, что первая молекула была не из твердого тела. Вторая молекула хвасталась подругам, что она любит свободу и не признает никаких ограничений. А вот третья подруга похвасталась, что она ценит верность и преданность и предпочитает, чтобы друзья были всегда рядом. На что вторая молекула сказала, а я ценю и свободу, и дружбу и еще могу менять свою форму. На что первая молекула возразила, а я тоже могу менять не только форму, но еще и объем. Определите, к какому агрегатному состоянию принадлежит каждая
-
14 слайд

-
15 слайд

-
16 слайд

Описание слайда:
Физкультминутка
-
17 слайд

Описание слайда:
С детства окружают нас тела,
Состоят они из вещества.
Всех веществ не знаем мы,
Но водою все окружены.
В атмосфере, в реках и в морях,
В супе, в чашке чая, в сухарях,
Даже в теле человека есть вода-
От неё не деться никуда!
В агрегатных состояниях вода
Свойства разные покажет нам всегда. -
18 слайд

Описание слайда:
Не одна вода в природе: Оглянись кругом. Про другие вещества Вы поверите с трудом:
Здесь написана не сказка, Это правда, а не ложь. Объясняется всё просто, Да ты сам сейчас поймёшь.
твердый кислород,
газообразная ртуть.
жидкий алмаз, -
19 слайд

Описание слайда:
Сталь тверда, но при нагреве Станет жидкой, как вода. Даже пар стальной над нею Наблюдается тогда.
При обычных условиях сталь – твердое вещество
При температуре 15350С сталь становится жидкой -
20 слайд

Описание слайда:
Кислород бывает твердым, Жидким тоже может быть. Но на практике, поверьте, Это нам не получить.
При обычной температуре кислород бывает газообразным.
При -1930С кислород становится жидким.
При -2190С кислород превращается в твердое тело. -
21 слайд

Описание слайда:
Задачки от тетушки совы
-
22 слайд

-
23 слайд

Описание слайда:
Молекулы
Пусть молекул не видим
В микромире их скрытом,
Пусть беззвучен их маленький мир,
Во Вселенной огромной
Из частичек тех скромных
Состоит из молекул весь мир!Припев:
Познаем мы мир молекул,
И расскажем всем друзьям,
Что состоим мы из частичек,
Знаем точно ты и я!
Нам волшебник не нужен,
Мы с учебником дружим,
Нам расскажет учебник про всё.
Про молекулы все же
Нам не скажет прохожий,
На уроках мы все узнаем.Припев.
-
24 слайд

Описание слайда:
Оценка за урок:
-
25 слайд

Описание слайда:
Ребята ! Я очень прошу взять меня в 7 «А» класс МБОУ ВСОШ №2. Обещаю делать все уроки! И не буду гусем. Только вам решать с вами или нет! Если согласны и все поняли на уроке нарисуйте цветочек на доске, а если нет то напишите «не согласен»
-
26 слайд

Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с
сайта, Вы можете оставить жалобу на материал.
Пожаловаться на материал

- Сейчас обучается 939 человек из 79 регионов

- Сейчас обучается 68 человек из 26 регионов

- Курс добавлен 18.11.2021
- Сейчас обучается 44 человека из 25 регионов
Найдите материал к любому уроку,
указав свой предмет (категорию), класс, учебник и тему:
также Вы можете выбрать тип материала:
-
Все материалы
-
Статьи
-
Научные работы
-
Видеоуроки
-
Презентации
-
Конспекты
-
Тесты
-
Рабочие программы
-
Другие методич. материалы
Проверен экспертом
Общая информация
Учебник:
«Физика», Перышкин А.В.
Тема:
Глава 1. Первоначальные сведения о строении вещества
Похожие материалы
-
Повторительно-обобщающий урок по теме «Первоначальные сведения о строении вещества» в 7а классе
-
Презентация по физике на тему «Фотоэффект»
-
Конспект урока по физике на тему «Простые механизмы» (7 класс)
-
Зачётная работа по теме «Ядерная физика»
-
Анализ ВПР по физике в 8 классе
-
Урок » Закон Ома »
-
Презентация к уроку по теме «Энергия»
-
Презентация к уроку по теме «Солнце и звезды»
-
Не нашли то что искали?
Воспользуйтесь поиском по нашей базе из
5453351 материал.
Вам будут интересны эти курсы:
-
Курс повышения квалификации «Информационные технологии в деятельности учителя физики»
-
Курс профессиональной переподготовки «Физика: теория и методика преподавания в образовательной организации»
-
Курс повышения квалификации «Организация научно-исследовательской работы студентов в соответствии с требованиями ФГОС»
-
Курс повышения квалификации «Основы управления проектами в условиях реализации ФГОС»
-
Курс повышения квалификации «Введение в сетевые технологии»
-
Курс повышения квалификации «Экономика: инструменты контроллинга»
-
Курс профессиональной переподготовки «Организация менеджмента в туризме»
-
Курс повышения квалификации «Финансы предприятия: актуальные аспекты в оценке стоимости бизнеса»
-
Курс повышения квалификации «ЕГЭ по физике: методика решения задач»
-
Курс повышения квалификации «Психодинамический подход в консультировании»
-
Курс профессиональной переподготовки «Организация процесса страхования (перестрахования)»
-
Курс профессиональной переподготовки «Организация маркетинговой деятельности»