30.01.13
Псевдомоноз «Pseudomonas aeruginosa».
Псевдомоноз (pseudomonosis) – инфекционное заболевание молодняка сельскохозяйственных животных, характеризующееся пневмониями, диареей, артритами. У взрослых животных – маститами, вагинитами и эндометритами.
Ежегодно ФГБУ «Ставропольская межобластная ветеринарная лаборатория» выделяет в исследуемом материале (вода, земля, почва, смывы с влагалища сельскохозяйственных животных, аборт плоды, сперма и препуциальные смывы быков производителей) псевдомоноз «Pseudomonas aeruginosa».
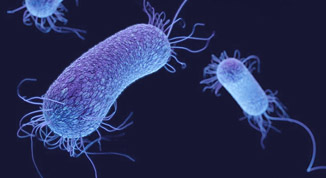
Pseudomona saeruginosa (синегнойная палочка) – это грамотрицательная подвижная бактерия палочковидной формы, является облигаторным (строгим) аэробом. Широко распространена в природе: встречается в почве, в воде, на растениях, в желудочно-кишечном тракте человека и животных. Способна не только длительное время сохраняться в окружающей среде (влажной атмосфере или воде), но и успешно размножаться. Оптимальная температура для развития 37 оC, но может расти и при 42 оС. Для своей жизнедеятельности может использовать широкий спектр биологических материалов. Причем синегнойная палочка является одним из самых подвижных микроорганизмов, наблюдаемых в образцах воды из природных источников. Выделенный микроорганизм ранее считался слабопатогенным, в настоящее время приобретает ведущее этиологическое значение в инфекционной патологии. Микроорганизмы семейства псевдомонад (Pseudomonadaceae), включая и синегнойную палочку (Pseudomonas aeruginosa), распространены в почве, в воде, на поверхности растений. Они могут также присутствовать на коже, в носоглотке и в кишечнике здорового человека и животного, не вызывая заболевания. Чрезвычайно устойчива к большинству антибиотиков за счет барьера, создаваемого липосахаридами внешней мембраны, а также частого присутствия в толще биопленки, тоже выполняющей защитную роль. Существуют штаммы, на которые практически не действуют никакие из известных антибиотиков. Что касается дезинфицирующих средств, то синегнойная палочка чувствительна к 0,5% раствору хлорамина, 3% раствору перекиси водорода 2% раствору фенола (карболовой кислоты). Эпизоотологические данные. Наиболее восприимчив молодняк. Источником возбудителя инфекции являются больные и бактерионосители. Во внешнюю среду возбудитель выделяется с мочой, фекалиями, молоком, носовой слизью, спермой, истечениями из влагалища. Заражение происходит воздушно-капельным, алиментарным и половым путями. Болезнь, как правило, носит очаговый характер и протекает энзоотически.
Для псевдомоноза свойственна сезонность: пик заболеваемости приходится на осенне-зимний период, а наименьшее выделение возбудителя отмечали в августе. Развитию заболевания способствуют факторы, снижающие резистентность животных, в первую очередь нарушения кормления, условий содержания и техногенные стрессы. Наиболее подвержен заболеванию молодняк и беременные животные, у которых регистрируются нарушения минерального и витаминного обменов (уровень каротина ниже нормы витамина А, резервной щелочности, цинка, йода). Чаще заболевание регистрируется при низком санитарном состоянии животноводческих помещений, общая микробная загрязненность воздуха родильных отделений. Наиболее часто синегнойную палочку выделяли в ассоциациях с E.coli, Proteus ssp, различными стрептококками и стафилококками.
Течение эпизоотического процесса при псевдомонозе у крупного рогатого скота. У молодняка развивается диарея, они быстро отстают в росте. Шерстный покров тусклый цвет. Каловые массы серо-зеленого цвета, иногда с примесью крови. Энзоотия протекает остро. Температура тела в начале болезни повышается на 0,5-1,5 °С а затем снижается до 37,5-38 °С, снижается или полностью отсутствует аппетит, развивается катарально-гнойный конъюнктивит, ринит. При токсической форме болезни у животных проявляются судороги, парезы, повышенную возбудимость. Заболеваемость телят в хозяйствах составляла 40-90. При патологоанатомических исследованиях у павших животных отмечается набухание, брыжеечные, средостенные, заглоточные лимфоузлы увеличены с кровоизлияниями. Регистрируются кровоизлияния на эпи- и миокарде, под капсулой почек и на селезенке. Отмечаются отеки слизистой оболочки желудка, острое геморрагическое воспаление слизистой оболочки желудка и кишечника с кровоизлияниями, дистрофические и застойные процессы в печени, почках и сердечной мышце, отеки в легких, сосуды коры головного мозга инъецированы.
У коров, искусственно осемененных спермой, содержащей инвазивные штаммы P.aeruginosa уже на 4 – 5 день отмечаются появление слизисто-гнойных истечений из половых органов. Псевдомоноз проявлялся в форме абортов во второй половине стельности, мертворождений, маститов, метритов, агалактии.
У производителей достаточно широко распространено носительство P.aeruginosa, клинические признаки заболевания проявляются редко. Из спермы и препуциальных смывов быков-производителей выделяется синегнойная палочка. При этом отмечается снижение половой активности, быки не охотно идут на чучело, объем эякулята меньше, чем обычно. Качество спермы по показателям загрязненности и активности спермиев низкий.
Течение эпизоотического процесса при псевдомонозе у свиней. Псевдомоноз регистрируется у поросят сосунов (5-25 дневного возраста), отъемного и после отъемного возраста (35-60дней). Инкубационный период от 2 до 7 дней. У поросят снижается аппетит, наблюдался отказ от корма, вялость, температура тела повышалась на 1,5-2,0◦ С, диарея, часто с примесью крови и слизи. Через 3-4 дня после начала заболевания регистрируется поражение ЦНС, мышечная дрожь, кашель, одышка, рвота с пенистыми кровянистыми выделениями, у животных старшего возраста развивалась серозно-катаральная и катарально-гнойная бронхопневмония. За день до гибели отмечается снижение температуры тела до 37 -37, ◦С, у отдельных животных развивался гомеостаз, характеризующийся геморрагическим инфильтратом подкожной клетчатки в области промежности, внутренней поверхности конечностей. Основные пути передачи P. аeruginosa у свиней – алиментарный и половой, с контаминированной возбудителем спермой. Контаминированная P. aeruginosa сперма хряков-производителей является причиной ранней гибели плодов и рождению гипотрофичных, инфицированных синегнойной палочкой поросят, заболеваемости свиноматок эндометритами и маститами. Псевдомоноз животных и птиц, независимо от природно-географических условий регистрируется во всех регионах России. Наибольшая инфицированность возбудителем псевдомоноза отмечается в хозяйствах с интенсивными технологиями и с нарушениями ветеринарно-санитарных правил ведения животноводства.
ПО ВОПРОСАМ ПРОФИЛАКТИИКИ, ДИАГНОСТИКИ ОБРАЩАТЬСЯ ПО АДРЕСУ:
ФГБУ «СТАВРОПОЛЬСКАЯ МЕЖОБЛАСТНАЯ ВЕТЕРИНАРНАЯ ЛАБОРАТОРИЯ»
г. Ставрополь, Старомарьевское шоссе,34 Тел. (8652) 28-16-53 , Бактериологический отдел.
Что такое Синегнойная инфекция у детей —
Синегнойная инфекция (известна также как пиоцианозы) – это инфекционные заболевания, которые вызываются условно-патогенными микроорганизмами из рода Pseudomonas, и которые протекают схоже с пневмонией, менингитом, поражением ЖКТ, различными нагноительными процессами и сепсисом.
Эпидемиология. Синегнойная палочка имеет широкое распространение в природе, но на разных материках и в разных странах распределена неравномерно. Она «хранится» в организмах растений, насекомых, теплокровных животных и человека. В 90% проб сточных вод обнаруживают синегнойную палочку.
Распространяют возбудитель заболевания больные люди, независимо от формы инфекции, а также здоровые носители. Носительство означает, что в организме человека есть синегнойная палочка, но симптомы заболевания не проявляются, человек выглядит здоровым. Опасны в плане заражения загрязненные возбудителем медикаменты, медаппаратура, антисептические растворы, предметы ухода за больными, санитарно-техническое оборудование.
Во внешней среде палочки устойчивы, сложно убить их большинством антибактериальных средств и дезинфицирующих растворов. На сегодняшний день появилось множество штаммов госпитальной инфекции.
Пути передачи синегнойной палочки:
- контактно-бытовой
- пищевой
- аэрозольный (воздушно-капельный).
В стационарах можно заразиться через перевязочный материал, постельное болье, лекарственные мази и растворы, руки врачей, нянек и пр., медицинскую аппаратуру. К синегнойной инфекции высокую восприимчивость имеют дети, ослабленные из-за перенесенных прежде болезней, с ожогами, иммунодефицитами, хроническими инфекционными заболеваниями, а также в группе риска находятся новорожденные.
Болезнь фиксируется круглогодично, сезонность не выражена. Среди детей большая часть заболеваний случается в раннем возрасте. Не смотря на то, что фиксируются спорадические случаи синегнойной инфекции, в стационарах и в отделениях для новорожденных могут быть вспышки лиоцианозов, с довольно большим числом заболевших.
Что провоцирует / Причины Синегнойной инфекции у детей:
Синегнойная палочка Pseudomonas aeruginosa относится к семейству Pseudomonadaeeae и роду Pseudomonas. Она представляет собой грамотрицательный подвижный аэробный микроорганизм, размер которого составляет 0,5—0,6×1,5мкм. Форма: палочка со жгутиком, без выраженной капсулы. В спецлитературе зафиксировано 200 штаммов синегнойной палочки. Лучше всего она развивается во влажной среде, но высушенные палочки могут выживать и накапливаться, к примеру, в больницах при недостаточной уборке (в пыли).
Штаммы P. aeruginosa природно резистентный к широкому спектру антибактериальных препаратов. Синегнойную палочку нельзя убить нашатырным спиртом, фурацилином, танином. Она чувствительна к борной и муравьиной кислотам, перманганату калия.
Синегнойная палочка оказывает патогенное действие с помощью ферментов, пегментов и токсинов. Она выделяет такие токсигены как экзотоксин А, эндотоксин, экзоэнзим. Вредят организму также такие агрессивные продукты как гемолизин, нейраминидаза, внеклеточная слизь, фосфолипаза, протеолитические ферменты. У P. aeruginosa существует сложная мозаика антигенов, которые локализуются в жгутиках, слизистой капсуле и оболочке. стимулируют специфический иммунитет антигены капсулы и клеточной оболочки.
Патогенез (что происходит?) во время Синегнойной инфекции у детей:
Проникая в организм, инфекция попадает в ЖКТ, дыхательные пути, кожу, конъюнктиву, пупочную ранку, мочевые пути. На месте попадания в организм ребенка палочка подавляет рост сопутствующей флоры из-за активности пигментов. Возбудитель связывается с поверхностью эпителиальных клеток при помощи жгутиков. Благодаря слизистому веществу синегнойная палочка лучше сцепляется с поверхностями тканей и лучше защищена от действия нейтрофилов и фагоцитов. Нейтрофилы – элементы крови человека, которые призваны защищать организм от бактериальных и грибковых (и, в меньшей мере, от вирусных) инфекций. Фагоциты – это клетки иммунной системы, которые так же, как и нейтрофилы, защищают организм от чужеродных частиц.
Антибиотикорезистентность P. aeruginosa способствует колонизации тканей макроорганизма. На начальном этапе инфекции важна протеолитическая активность синегнойной палочки.
Глубокое повреждающее воздействие на ткани макроорганизма оказывает экзотоксин А, блокирующий синтез белка в клетках. В дальнейшем развитии патологического процесса значительную роль играет эндотоксин, который вызывает экссудацию в просвет кишечника и способствует нарушению микроциркуляции в слизистой оболочке кишки. Фосфолипаза вызывает изъязвления и некроз тканей, играет роль в формировании очагов абспедирования. Экзоэнзим способствует генерализации заболевания, но этот процесс зависит не только от него. Генерализация болезни означает, что инфекция поражает множество органов ребенка.
Выздоровление при синегнойной инфекции обусловлено формированием антитоксического иммунитета.
Симптомы Синегнойной инфекции у детей:
От локализации процесса зависит проявленная симптоматика синегнойной инфекции у детей. Часто наступает поражение дыхательных путей, развивается пневмония и ЖКТ (желудочно-кишечный тракт), возникает энтероколит. Также случаются отиты, менингиты, пиелонефриты, остеомиелиты, сепсис, поражение глаз.
Пневмония начинается остро, температура повышается (38 °С), появляется упорный влажный кашель. Мокрота густой консистенции, обильная, вязкая, через несколько суток становится гнойной. Выражена одышка с признаками кислородной недостаточности (орбитальный и периоральный цианоз), также становятся всё более выраженными признаки сердечно-сосудистой недостаточности.
Наблюдаются морфологические изменения в легких по типу крупноочаговой, нередко сливной пневмонии, захватывающей целую долю или несколько долей. Клинический анализ крови показывает гипохромную анемию, тромбоцитопению, лейкоцитоз.
При поражении инфекцией ЖКТ возникает энтероколит. Начинаются боли в животе, жидкий стул, урчание по ходу кишечника. Больной испражняется от 5 до 15 раз за день и ночь. Испражнения жидкие, зеленоватых оттенков, есть примеси гноя и слизи, иногда с кровянистыми прожилками. С первых дней болезни не всегда начинается интоксикация и повышение температуры (она может повышаться на протяжении 2-3 суток). В некоторых случаях при синегнойном энтероколите возникает токсикоз с эксикозом. Из-за снижения количества бифидобактерий и полноценной кишечной палочки у больных отмечаются глубокие нарушения кишечного микробиоценоза с самого начала кишечных расстройств.
В кишечнике поражение может быть морфологически выражено как минимум катарально-эрозивным энтероколитом, как максимум – гнойно-некротическим энтероколитом. При тяжелых случаях может фиксироваться перитонит. Синегнойные палочки скапливаются в очагах деструкции (разрушения).
У старших детей при заражении через пищу появляется пищевая токсикоинфекция. Всего несколько часов длится инкубационный период, далее остро проявляются симптомы. Начинается тошнота, рвота съеденными продуктами, боли в области эпигастрия. Температура может подниматься незначительно. Стул имеет кашецеподобную или жидкую консистенцию, наблюдаются небольшие включения зелени и слизи. Испражнение случается от 3 до 8 раз за день и ночь. Тяжесть состояния заболевшего ребенка зависит от общего токсикоза.
При сепсисе инфекция попадает через кишечник, в более редких случаях – через нос или рот, пупочную ранку, раны на венах от катетера. Основные симптомы: пневмония (плевропневмония) с симптомами нарастающей дыхательной и сердечно-сосудистой недостаточности и кишечный синдром в виде энтероколита, тяжелый токсикоз с поражением ЦНС. Случаются приступы судороги, сознание нарушается (как максимум – ребенок впадает в кому).
Особенности заболевания у новорожденных детей. В отделениях для новорожденных случаются вспышки синегнойной инфекции. В особой группе риска – недоношенные малыши. Заражаются дети в основном через недостаточно продезинфицированные руки персонала. Наиболее часто поражается желудочно-кишечный тракт с развитием тяжелого энтероколита с геморрагическим компонентом.
Нередко фиксируют изъязвления и перфорации слизистой оболочки кишечника. Случается значительная потеря массы тела вследствие обезвоживания. Диарея сопровождается выраженным абдоминальным болевым синдромом. Инфекция может поражать не только ЖКТ, но и кожу, глаза, пупочную ранку, уши.
Конъюнктивит может быть слабо выражен (чуть-чуть слипаются веки) или в тяжелой форме (резкая гиперемия конъюнктивы, отек и эритема век, гнойное отделяемое).
У новорожденных с низкой массой тела легко возникают средние отиты. Появляются такие симптомы: раздражительность, рвота, повышение температуры, есть вероятность диареи. Во многих случаях отмечаются также сопутствующие острые респираторные инфекции, омфалит, конъюнктивит.
Диагностика Синегнойной инфекции у детей:
Для постановки диагноза пиоцианоза у детей необходимо провести бактериологическое и серологическое исследования. Синегнойную палочку выделяют из кала, мокроты, мочи, крови, спинномозговой жидкости, бронхиальных смывов и пр.
Врачи могут дополнительно назначить бактериологическое исследование смывов с предметов ухода за больными, с медицинской аппаратуры в очагах инфекции, с санитарно-гигиенического оборудования и т. д. Если в биоматериале обнаружена синегнойная палочка, оценивают ее количество.
Лечение Синегнойной инфекции у детей:
В комплексной терапии пиоцианозов (синегнойной инфекции) у детей важное место занимают антибиотики. Штаммы синегнойной палочки резистентны к большей части антибактериальных препаратов, потому для лечения часто назначают антибиотики широкого спектра действия (цефалоспорины 3-го и 4-го поколений). Тяжелые и затяжные случаи синегнойной инфекции лечат противосинегнойным у-глобулином и гипериммунной антитоксической донорской плазмой.
Профилактика Синегнойной инфекции у детей:
Специфическая профилактика синегнойной инфекции не получила широкого распространения. Существуют вакцины, основанные на анатоксине, а также апробирована гентавалентная вакцина (производство США) для вакцинации в хирургических стационарах. Существуют предположения, что вакцины перспективны не только для профилактики, но и для лечения пиоцианозов в случаях полирезистентности к антибиотикам выделяемых от больных штаммов синегнойной палочки.
К каким докторам следует обращаться если у Вас Синегнойная инфекция у детей:
Инфекционист
Гастроэнтеролог
Окулист
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Синегнойной инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Если Вами ранее были выполнены какие-либо исследования, обязательно возьмите их результаты на консультацию к врачу.
Если исследования выполнены не были, мы сделаем все необходимое в нашей клинике или у наших коллег в других клиниках.
У Вас ? Необходимо очень тщательно подходить к состоянию Вашего здоровья в целом. Люди уделяют недостаточно внимания симптомам заболеваний и не осознают, что эти болезни могут быть жизненно опасными. Есть много болезней, которые по началу никак не проявляют себя в нашем организме, но в итоге оказывается, что, к сожалению, их уже лечить слишком поздно. Каждое заболевание имеет свои определенные признаки, характерные внешние проявления – так называемые симптомы болезни. Определение симптомов – первый шаг в диагностике заболеваний в целом. Для этого просто необходимо по несколько раз в год проходить обследование у врача, чтобы не только предотвратить страшную болезнь, но и поддерживать здоровый дух в теле и организме в целом.
Если Вы хотите задать вопрос врачу – воспользуйтесь разделом онлайн консультации, возможно Вы найдете там ответы на свои вопросы и прочитаете советы по уходу за собой. Если Вас интересуют отзывы о клиниках и врачах – попробуйте найти нужную Вам информацию в разделе Вся медицина. Также зарегистрируйтесь на медицинском портале Eurolab, чтобы быть постоянно в курсе последних новостей и обновлений информации на сайте, которые будут автоматически высылаться Вам на почту.
Другие заболевания из группы Болезни ребенка (педиатрия):
Если Вас интересуют еще какие-нибудь виды болезней и группы заболеваний человека или у Вас есть какие-либо другие вопросы и предложения – напишите нам, мы обязательно постараемся Вам помочь.
Общие сведения
Синегнойная инфекция представляет собой группу различных инфекционных заболеваний, этиологическим фактором которых являются условно-патогенные микроорганизмы рода псевдомонада (на латыни — Pseudomonas). Микроорганизмы рода Pseudomonas являются свободно живущими бактериями и чрезвычайно распространенными в окружающей среде, в том числе в воде и почве, способны использовать почти все природные органические соединения в качестве источника энергии.
Наличие широкого спектра ферментов и плазмид у бактерий этого рода обеспечивает высокую изменчивость и способность быстро адаптироваться к изменяющимся условиям среды обитания, выдерживать мощный и длительный антропогенный пресс. Бактерии рода Pseudomonas способны размножаться высокими темпами, обладают высокой скоростью роста и широким спектром активности, что обуславливает их возможность колонизировать практически любые ниши и адаптироваться к действию новых химических соединений.
Эти приспособления могут выражаться в трансформации морфологии и генотипа микроорганизма. Могут являться составляющим компонентом нормальной микрофлоры кожи, особенно около ушей, в паховой/подмышечной области и слизистой оболочки (например, носа, в горле). Также часто обнаруживается синегнойная палочка в ухе и мокроте.
В настоящее время псевдомонады широко используются в практике (для извлечения из скважин остаточной нефти, производства антибиотиков, борьбы с загрязнением окружающей среды, в качестве моделей для теоретических исследований и др.). Наиболее важное значение в медицинской практике имеет синегнойная палочка (Pseudomonas aeruginosa), являющаяся одним из основных возбудителей системных/локальных гнойно-воспалительных процессов (бактериемий, септицемий), особенно у пациентов, находящихся в условиях стационара. Кроме псевдомонас аэругиноза возбудителем инфекционных заболеваний могут и некоторые другие виды псевдомонад (P. pseudomallei, P. Cepacia, P. Mallei, Р. fluorescens и др.), однако их удельный вес в заболеваемости существенно ниже.
Спектр инфекционных заболеваний, вызываемых pseudomonas aeruginosa, варьирует от внешних незначительных инфекций (инфекция мягких тканей, псевдомонадный фолликулит, наружный отит и др.) до тяжело протекающих и угрожающих жизни заболеваний (пневмония, бактериемия, инфекции костей и суставов, эндокардит и др.). Инфекции, обусловленные синегнойной палочкой, чаще встречаются и протекают более тяжело среди лиц:
- Находящихся в условиях стационара.
- Ослабленных и престарелых больных и у пациентов с выраженным иммунодефицитом.
- Больных диабетом/муковисцидозом/кистозным фиброзом.
- Принимающих иммуносупрессивные препараты.
- У детей с врожденными аномалиями и недоношенных детей.
Синегнойная палочка является одной из наиболее частой причин развития нозокомиальных (внутрибольничных) инфекций, на которую приходится до 20% случаев. На ее долю приходится почти 25% гнойных патологий у пациентов хирургического профиля и около 35% всех инфекций мочевыделительной системы. Синегнойная палочка также в 19,8% случаев является инфекционным агентом первичных бактериемий.
Патогенез
Патогенное действие синегнойной палочки обусловлено способностью бактерии к инвазии и длительной персистенции в различных тканях, к цитотоксическому эффекту и к стимуляции генерализованной воспалительной реакции. К непосредственно влияющим факторам на формирование локального/системного воспаления относятся экзотоксин S, липополисахарид, нитратредуктаза, флагеллин, фосфолипаза С, пиоцианин, большинство из которых инициируют секрецию ведущего провоспалительного медиатора — TNF (фактора некроза опухоли).
Р. aeruginosa характеризуется наличием системы экскреции 3 типа, которая обеспечивает выведение из внутренней среды бактериальной клетки экзоэнзимов и их последующую транслокацию непосредственно к мишеням внутри эукариотической клетки. Такими веществами у синегнойной палочки являются экзотоксины (ExoT, ExoS, ExoU, ExoY). Под их действием происходит ингибирование синтеза ДНК, изменение клеточной формы, стимуляция апоптоза, потеря способности клетки к локальной адгезии.
Различные штаммы популяции Р. aeruginosa являются неоднородными с позиций способности к синтезу/секреции различных факторов токсичности, обусловлено индивидуальным взаимодействием макро- и микроорганизмов, влиянием условия внешней среды и плотность популяции бактерий.
Важнейшим механизмом экспрессии факторов вирулентности является феномен кооперативной чувствительности, заключающийся в изменении физиологических функций бактерий при росте/снижении их численности с формированием ответной реакции нового качества. Под контролем этой системы находится образование биопленки путем агрегации клеток и выделения полисахаридов во внешнюю среду и синтез всех экзотоксинов.
Образование биопленки возникает благодаря упорядоченному/скоординированному поведению бактерий (чувству кворума), реализуемого путем передачи сигналов посредством химических соединений, что и обеспечивает популяции Р. aeruginosa устойчивость к воздействию некоторых дезинфектантов и противомикробных препаратов, приводящее к вспышкам внутрибольничных инфекций.
P. aeruginosa способна к специфической адгезии за счет молекул в состав белков плазмы, которые являются адгезинами для бактерий и неспецифической адгезии на различных имплантируемых устройствах (эндотрахеальные трубки, катетеры и др.). Распространение по внеклеточным пространствам обеспечивается секретируемыми белками с высокой ферментативной активностью: липаза, эластаза, протеазы, что и лежит в основе высокого риска развития бактериемии практически при любой локализации первичного инфекционного очага.
Классификация
В основе классификации семейства Pseudomonadaceae лежит признак рРНК гомологии, на основании которого выделяют 5 групп:
- I группа (род Pseudomonas) — Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas alcaligenes, Pseudomonas stutzeri, Pseudomonas fluorescens, Pseudomonas mendocina, Pseudomonas pseudoalcaligenes и др.
- II группа (род Burkholderia) — Burkholderia mallei Burkholderia pseudomallei, Burkholderia cepacia и др.
- III группа (род Comamonas) — Comamonas terrigena, Comamonas acidovorans и др.
- IV группа (род Brevundimonas) — Brevundimonas diminuta, Brevundimonas vesicularis.
- V группа (род Stenotrophomonas) — Stenotrophomonas maltophilia.
Таким образом, синегнойная палочка относится к царству — Bacteria, семейству Pseudomonadaceae, роду — Pseudomonas. Ранее к роду Pseudomonas относили и некоторых других представителей, однако по состоянию на сегодняшний день они выделены в самостоятельные род протеобактерий Brevundimonas, которые несмотря на широкое присутствие в окружающей среде, из клинических образцов выделяются крайне редко, например, brevundimonas pseudomonas naejangsanesis.
Причины
Возбудителем синегнойной инфекции является в большинстве случаев синегнойная палочка, которая относится к условно-патогенной микрофлоре организма, способная вызывать инфекционное заболевание лишь при недостаточном ответе или отсутствии адекватного ответа иммунной системы.
Микробиология псевдомонады
Микроорганизмы рода псевдомонада (на латинском — Pseudomonas) относятся к группе грамотрицательных неферментирующих бацилл. Представляют собой прямые одиночные/попарные или расположенные в виде цепочек палочки (рис. ниже), размером 1,0-1,7×0,6 мкм. Не образуют капсул, имеют жгутик и пили (выросты), обеспечивающие подвижность. Могут продуцировать при определенных условиях внеклеточную капсулоподобную слизь полисахаридной природы. Культуры продуцируют характерные пигменты: в состав которых входят соединения, окрашивающие среду в желто-зеленый, сине-зеленый и бурый цвета.
Устойчивы к высушиванию, хорошо сохраняются во влажной среде, погибают при кипячении, автоклавировании, при воздействии хлорсодержащих дезинфектантов и 3% перекиси водорода.
Эпидемиология
Источником инфекции являются больные и бактерионосители, преимущественная локализация в организме человека – кожа, кишечник. Как передается синегнойная палочка? Вне больничных учреждений палочка передается преимущественно воздушно-капельным и контактным способом. При госпитальном заражении основным путем инфицирования является контактный способ: передается через руки медицинского персонала, нестерильный инструментарий и предметы ухода за больными.
Благодаря отличной способности синегнойной палочки существовать во влажной среде она контаминируют самые различные экологические ниши — растворы, в т. ч. и некоторые дезинфектанты, например, Риванол, Фурацилин, а также медицинское оборудование, инструментарий, больничные предметы (особенно в местах скопления жидкости — краны, раковины, респираторы, посуду, увлажнители и др.). Фактором передачи часто бывают перидуральные, мочевые и сосудистые катетеры, кружки Эсмарха, инфузионные растворы, перевязочный материал, молочные смеси, пища, посуда и др. Следствием значительного распространения синегнойной палочки в системе лечебных учреждений является существенная колонизация ими кожных/слизистых покровов пациентов.
Экологическая система среды больниц не является стационарной. Можно сказать, что в ней происходят непрерывные фазовые преобразования, способствующие формированию эпидемических вариантов Pseudomonas aeruginosa и последовательной смене эпидемического и межэпидемичекого периода. При этом, эпидемические варианты имеют такие факторы вирулентности, метаболический потенциал и физиологические свойства, которые обеспечивают существование микроорганизма в двух формах: в виде подвижной формы, обеспечивающей им движение для колонизации новой ниши или среды обитания и фиксированной биопленки, защищающей от множества неблагоприятных факторов внешней среды и позволяющей им выживать в самых различных условиях.
Так, при стандартной дезинфекции сроки выживания Pseudomonas aeruginosa во среде реанимационного отделения превысили 3 месяца. Pseudomonas aeruginosa принадлежит к числу патогенов, обладающих высоким эпидемическим потенциалом и на протяжении короткого периода (6-7 суток) способна формировать госпитальные штаммы и через существующие пути передачи вызывать внутрибольничные вспышки.
Кроме экзогенного инфицирования существует и возможность эндогенного заражения, которое обусловлено собственной, нормальной микрофлорой человека. Инфекционный процесс развивается при слабости иммунной системы или в случаях нарушения антимикробных барьеров в виде инфицирования раневых поверхностей содержимым кишечника и др. Восприимчивость к развитию синегнойной инфекции высокая. Болеет ли взрослый человек синегнойной палочкой? Да, синегнойная инфекция встречается как у взрослых, так и детей независимо от возрастной группы.
Симптомы синегнойной палочки
Симптомы синегнойной инфекции крайне разнообразны, что обусловлено политропностью Pseudomonas aeruginosa, различными путями проникновения ее в организм, ее преимущественной локализацией в организме и индивидуальными особенностями пациента. В подавляющем большинстве случаи клинических проявлений синегнойной палочки относится к внутрибольничной инфекции. Выделяют следующие клинические проявления:
Локальная инфекция кожи/подкожной клетчатки (раневые инфекции, пиодермия, дерматит)
Наиболее часто возникает инфекционное воспаление на месте ожогов, травмы, порезов и операционных швов, пролежней, варикозных язв и др., особенно после антибактериальной терапии. На раневой поверхности появляется характерное сине-зеленое окрашивание, а струп, на раневой поверхности приобретает темно-коричневую, фиолетовую или черную окраску.
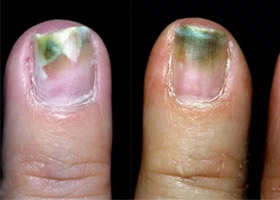
Инфекция на ногтях
Под струпом образуются: отек ткани и кровоизлияния, происходят некротическое разрушения ткани. Воспалительный процесс быстро распространяется на здоровые участки кожи и мягких тканей, о чем свидетельствует выраженное покраснение. Процесс часто заканчивается развитием абсцесса или гангрены.
Страдает общее состояние больного. Одним из частых проявлений синегнойной инфекции на коже является фолликулит — гнойничковые высыпания на коже, в центре которых находится волос. Могут сопровождаться выраженным зудом. Также синегнойная инфекция может проявляться дерматитом и пиодермией.
Инфекции глаз
Может проявляться гнойным конъюнктивитом, кератитом и даже панофтальмитом (повреждение глазного яблока) и в последующем деструкцией глазного яблока. Пациенты жалуются на ощущение постороннего тела, и боль в глазу и гнойные выделения, нарушение зрения. Наиболее частой причиной является травматизация глаза, ожоги или загрязнение контактных оптических линз. Вначале по центру роговицы появляется небольшая язва, которая быстро расширяется и захватывает склеру. Общее состояние больного не страдает. После операций на глазах и проникающих травмах возможно развитие гнойного эндофтальмита.
Инфекции уха, параназального/сосцевидного синусов
Синегнойная синегнойная палочка в ухе наиболее часто проявляется в виде наружного гнойного отита, проявляющегося гнойным/серозно-кровянистым выделением из наружного слухового канала. Реже — развитие среднего отита и мастоидита. При локализации на слизистой носа синегнойная палочка может вызывать хронический протекающий ринит и воспаление придаточных пазух носа (фронтит/гайморит), притекающие с характерными для них симптомами.
Инфекции желудочно-кишечного тракта
Синегнойная инфекция может поражение любой отдел ЖКТ с различной степенью воспалительных изменений от незначительно выраженного катарального до язвенно-некротического воспаления с прободением стенки кишечника и возникновением кровотечения. Чаще протекает в виде пищевой токсикоинфекции или гастроэнтероколита. Характерно острое начало, рвота и зловонный зеленоватый жидкий стул с примесью слизи (5-6 р. в сутки), боли в эпигастрии, высокая температура, урчание и вздутие живота. Длительность заболевания 2-5 суток.
Инфекция мочевыводящих путей
Чаще всего синегнойная палочка проникает в мочевые пути восходящим путем, но возможен и занос в мочевые пути гематогенным путем. Синегнойная палочка в мочевыводящих органах вызывает проявляется развитием уретрита (воспаление мочевыводящего канала), цистита (мочевого пузыря) и пиелонефрита.
Клиническая симптоматика синегнойного воспаления этих соответствует клиническим проявлениям этих заболеваний, вызванных другими микроорганизмами. Реже отмечаются язвы на слизистой мочевого пузыря, почечных лоханок или мочеточника, характерные для синегнойной инфекции. Характерным признаком является затяжное/хроническое течение с частыми обострениями и полирезистентоность к антибактериальным препаратам.
Синегнойная инфекция в легких
Синегнойная инфекция в органах дыхания наиболее часто развивается у пациентов с заболеваниями бронхолегочной системы: муковисцидозом, бронхитами, бронхоэктатической болезнью, а также у пациентов отделений реанимации и находящихся на аппаратах искусственного дыхания. Симптоматика соответствует появлениям типичной пневмонии, однако для нее характерно затяжное течение, возникновение деструкционных процессов в легких (распад легочной ткани), слабый эффект или отсутствие эффекта от проводимой антибактериальной терапии.
Поражение нервной системы
Ее проявлением является развитие менингита, возникающего чаще вторично при сепсисе путем заноса инфекции из других очагов. Реже отмечается первичный менингит, возникающий при заносе возбудителя в субарахноидальное пространство при спинальной анестезии, люмбальной пункции, медицинских манипуляциях или травмах в головы.
Эндокардит
Встречается относительно редко, преимущественно при заносе возбудителя при хирургических операциях на открытом сердце через инфицированный шовный материал. Последствиями эндокардитов этой этиологии могут быть метастатические абсцессы в костях (остеомиелит), суставах, надпочечниках и легких.
Бактериемия, вызванная Pseudomonas aeruginosa
Развивается вследствие генерализации местного инфекционного процесса — клиническими формами которого являются нагноившиеся раны, пневмония, инфекция мочевыводящих путей. Также часто бывает следствием имплантированного в кровеносное русло устройства, контаминированного возбудителем. Течение септицемии чрезвычайно тяжелое, сопровождающиеся в 35-70% случаев смертью пациента.
Анализы и диагностика
Диагноз устанавливается на основании результатов лабораторного обследования.
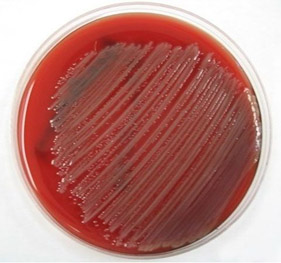
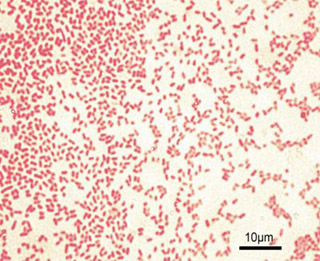
Бактериологический посев материала на питательные среды (слизи носоглотки, мокроты, мочи, крови, испражнений, отделяемого из ран и др.) с последующей микроскопией (рис. ниже). При необходимости инструментальные обследования — люмбальная пункция, рентгенография органов грудной клетки, ультразвуковое исследование, эхокардиография, бронхоскопия КТ и магнитно-резонансная томография.
Колонии P. aeruginosa
Синегнойная палочка при бактериоскопии
Лечение синегнойной палочки
Пациенты с внутрибольничной синегнойной инфекцией лечатся в том лечебном отделении, где проходили основное лечение до манифестации синегнойного инфекционного процесса. До устойчивого купирования лихорадки назначается постельный режим на протяжении 3-5 дней, при тяжелом течении — продолжительность постельного режима определяется степенью инвазии, клинической симптоматикой, наличием/отсутствием осложнений и сопутствующих болезней. При развитии локальной синегнойной инфекции лечение может проводится амбулаторно.
Основу лечения составляет этиотропная терапия, которая при синегнойной инфекции достаточно сложная их-за частой встречаемости антибиотико-резистентных штаммов P. aeruginosa преимущественно антибиотикам тетрациклинового/пенициллинового ряда, частично к карбапенемам, цефалоспоринам и аминогликозидам.
Низкая чувствительность к антибиотикам обусловлена блокадой поступления препарата-антибиотика к внутриклеточной мишени посредством способности бактерии продуцировать мукоидную оболочку, которая защищает ее от фагоцитов и специфических антител, что обеспечивает ее неуязвимость для различных химических веществ (антибиотики и дезинфектанты). Также важным механизмом является ферментативная инактивация антибактериальных препаратов (так, нуклеотидаза инактивируют аминогликозиды; бета-лактамы — пенициллины и цефалоспорины).
Тем не менее, определенные группы антибактериальных препаратов или отдельные препараты внутри группы, которые сохраняют свою эффективность при синегнойной инфекции. Применение антибактериальных препаратов может проводится как в режиме монотерапии, так и комбинированного (сочетанного) использования препаратов нескольких групп, которые могут назначаться как местно, так и системно. Наиболее эффективные антибиотики при лечении синегнойной палочки:
- Цефалоспорины (Цефипим, Цефтазидим, Цефоперазон). Не рекомендуется назначать Цефотаксим, Цефуроксим, Цефтриаксон.
- Аминогликозиды (Амикацин, Тобрамицин, Гентамицин).
- Фторхинолоны (Левофлоксацин, Ципрофлоксацин, Моксифлоксацин).
- Карбапенемы (Имипенем, Меропенем, Дорипенем).
- Монобактамы (Азтреонам).
- Антипсевдомонадные пенициллины (Пиперациллин, Тикарциллин).
- Полимиксины (Полимиксин В).
Крайне важным условием эффективности антибиотикотерапии синегнойной инфекции является ее продолжительность, поскольку неадекватная продолжительность лечения создает высокий риск развития резистентности, неэффективности терапии или клиническому рецидиву инфекции. Ее длительность определяется преимущественно локализацией инфекционного процесса и тяжестью течения.

Отзывы о синегнойном бактериофаге среди пациентов в большинстве случаев положительны. Однако к обязательным условиям эффективной фаготерапии относятся предварительное определение фагочувствительности штамма синегнойной палочки. Купить бактериофаг синегнойный (бактериофаг псевдомонас аэругиноза синегнойный) в аптечной сети трудностей не представляет.
Кроме этиотропной терапии при необходимости назначается патогенетическая и симптоматическая терапия (противовоспалительная, дезинтоксикационная, жаропонижающие, обезболивающие и др. средства) применительно к конкретному заболеванию. Лечение должно включать проведение общеукрепляющей терапии (Иммуноглобулин, Метилурацил, Пентоксил, витаминно-минеральные препараты и др.).
Лечение народными средствами может использоваться исключительно в качестве дополнения к назначенной терапии и преимущественно для синегнойной инфекции с локализацией в горле, на коже в виде полосканий горла различными противовоспалительными травами и для промывания раневых поверхностей (настой календулы, хвойные эфирные масла, раствор хлорофиллипта и др.).
Доктора
Лекарства
Антибактериальные препараты:
- Цефалоспорины (Цефепим, Цефтазидим, Цефоперазон).
- Аминогликозиды (Амикацин, Тобрамицин, Гентамицин).
- Фторхинолоны (Левофлоксацин, Ципрофлоксацин, Моксифлоксацин).
- Карбапенемы (Имипенем, Меропенем, Дорипенем).
- Монобактамы (Азтреонам).
- Антипсевдомонадные пенициллины (Пиперациллин, Тикарциллин).
- Полимиксины (Полимиксин В).
- Бактериофаги (Бактериофаг синегнойной палочки).
Процедуры и операции
Глубокая хирургическая обработка раневых поверхностей. Хирургическое вмешательство (вскрытии и дренирование) проводится при гнойных процессах (локализованных и разлитых), осложненных отитах, перфорации/некрозе участка кишки.
Синегнойная палочка у детей
Симптомы синегнойной палочки у детей, также как и у взрослых пациентов определяются локализацией инфекционного процесса. Следует отметить, что, если обнаружена синегнойная палочка у детей, Комаровский считает это не поводом к панике, поскольку она может встречаться и здоровых детей. Важно, чтобы ее выделение не сопровождалось конкретными симптомами заболевания. Наиболее часто у детей, особенно младшего возраста, поражаются желудочно-кишечный тракт с развитием симптоматики энтероколита и дыхательные пути с развитием пневмонии. Реже встречаются поражение глаз, отиты, менингиты, остеомиелиты, пиелонефриты и сепсис.
Поражение желудочно-кишечного тракта
Заболевание начинается остро с жидкого стула, болей в животе, урчания в кишечнике. Частота испражнений варьирует от 5 до 15 раз, а консистенция — от зеленоватого до желтоватого цвета с примесью слизи и гноя, реже прожилки крови. Температурная реакция и токсикоз у ребенка нарастает постепенно на протяжении первых 2-3 дней. У некоторых детей с синегнойным энтероколитом развивается токсикоз с эксикозом, а у подавляющей численности — глубокие нарушения микробиоценоза кишечника за счет значительного снижения полноценной кишечной палочки и бифидобактерий.
У детей старшего возраста при пищевом инфицировании развивается пищевая токсикоинфекция, для которой характерен кратковременный инкубационный период, тошнота, боли в эпигастральной области, рвота съеденной пищей. Стул жидкий/кашицеобразный с небольшим количеством слизи и частотой 3-8 раз в сутки. Тяжесть течения определяется явлениями общего токсикоза. Синегнойная инфекция у детей протекает чаще остро, реже может носить затяжной характер.
Особенно часто синегнойная инфекция встречается в отделениях для новорожденных в виде вспышек. Особо восприимчивы к инфекции недоношенные дети, заражение которых происходит через медперсонал. Поражается преимущественно желудочно-кишечный тракт с развитием клинической симптоматики энтероколита с геморрагическим компонентом, протекающего в тяжелой форме. Отмечается быстрое обезвоживание ребенка и выраженная потеря массы тела. Кроме пищеварительного тракта в патологический процесс могут вовлекаться уши, кожа, пупочная ранка, глаза. Лечение синегнойной палочки у детей принципиально не отличается от лечения взрослых пациентов.
Диета
Специальная диета при синегнойной инфекции отсутствует, однако диетическое питание является важнейшим компонентом лечения и определяется конкретным заболеванием.
Профилактика
Специфическая профилактика осуществляется путем введения поливалентной вакцины лицам с иммунным дефицитом, медицинским работникам, пациентам с глубокими/обширными ранами, открытыми переломами, ожоговым больным, пациентам старческого возраста.
Неспецифические профилактические мероприятия включают профилактику иммунодефицитных состояний, своевременную терапию хронических инфекций, укрепление здоровья, полноценное питание. Профилактика внутрибольничной инфекции достигается проведением комплексных противоэпидемических мероприятий.
Последствия и осложнения
Серьезными осложнениями локального синегнойного инфекционного процесса является развитие синегнойной бактериемии и септического шока.
Прогноз
Прогноз при локальных инфекционных процессах благоприятный. В случае развития синегнойной бактериемии и септического шока выживаемость больных находится на уровне 30-60% и прогноз ухудшается по мере нарастания прогрессирования тяжести органных расстройств.
Список источников
- Смирнов В. В., Киприанова Е. А. Бактерии рода Pseudomonas. Киев: Наукова думка, 1990. 264 с.
- Иванов Д.В. Распространение и механизмы резистентности микроорганизмов штаммов бактерий Pseudomonas//Фарматека / Иванов Д.В., Егоров А.М. — 2007. №8/9. — c.159-168.
- Белобородов В.Б. Проблема антибактериальной терапии инфекций в отделениях реанимации и интенсивной терапии с позиций доказательной медицины. // Consilium medicum. – 2002. – т.4. – №1. «Инфекции в стационаре».
- Страчунский, Л.С., Решедько, Г.К., Стецюк, О.У., Андреева, А.С., Щебников, А.Г. Сравнительная активность антисинегнойных антибиотиков в отношении нозокомиальных штаммов Pseudomonas aeruginosa, выделенных в отделениях реанимации и интенсивной терапии России// Антибиотики и химиотерапия, 2003. — №5. – с.35-46/
- Шагинян, И.А., Чернуха, М.Ю. Неферментирующие грамотрицательные бактерии в этиологии внутрибольничных инфекций: клинические, микробиологические и эпидемиологические особенности //Клин. микробиол. антимикроб. химиотер. – 2005. – Т.7. — №3. – с. 271-285.
Статьи
Опубликовано в журнале:
Русский медицинский журнал. Том 13, № 7, 2005
Профессор В.А. Руднов
Уральская государственная медицинская академия, Екатеринбург
Актуальность проблемы
Как следует из многоцентровых национальных и международных исследований, уже более 10 лет P. aeruginosa выступает в качестве одного из наиболее частых возбудителей госпитальных инфекций (ГИ), особенно в отделениях реанимации и интенсивной терапии (ОРИТ) [1–3]. Частота развития синегнойной инфекции во многом определяется нозологической структурой пациентов, тяжестью их исходного состояния, распространенностью инвазивных процедур, в частности, числом больных, нуждающихся в длительной респираторной поддержке, катетеризации мочевого пузыря или проведении длительной инфузионной терапии.
Необходимость обсуждения проблемы антибактериальной терапии инфекций, вызываемых данным микроорганизмом, наряду с их высокой распространенностью, связана также с ростом его резистентности практически ко всем из используемых в широкой практике антибиотикам, трудностями эрадикации из тканей и высокой летальностью.
Общая микробиологическая характеристика псевдомонад
Микроорганизмы рода Pseudomonas относятся к группе неферментирующих грамотрицательных бацилл. Они являются свободно живущими бактериями, чрезвычайно распространенными в окружающей среде, использующими в качестве источника энергии почти все природные органические соединения.
Благодаря способности существовать во влажной среде псевдомонады контаминируют самые разнообразные растворы, в том числе и некоторые из дезинфектантов (фурациллин, риванол), а также медицинский инструментарий и оборудование, особенно в местах скопления жидкости. Облигатная аэробность этих микроорганизмов имеющих мощную систему антиоксидантной защиты делает их устойчивыми и к действию синглетного кислорода. Псевдомонады выделяют из раковин, кранов, посуды, респираторов, увлажнителей, влагосборников, кондиционеров. Следствием широкого распространения псевдомонад в среде лечебных учреждений является колонизация ими слизистых и кожных покровов больных.
Синегнойная палочка принадлежит к бактериям, которые в естественных условиях патогенны и для человека, и для животных.
Особенности взаимодействия P. aeruginosa с макроорганизмом — объективные трудности для эрадикации антибиотиками
В отличие от подавляющего большинства представителей своего рода синегнойная палочка обладает многочисленными факторами вирулентности. Патогенность синегнойной палочки детерминирована способностью к инвазии и персистенции в тканях, а также к цито-токсическому эффекту и стимуляции генерализованной воспалительной реакции. Факторами, непосредственно влияющими на формирование локального и системного воспаления, являются липополисахарид, экзотоксин S, флагеллин, нитратредуктаза, пиоцианин, фосфолипаза С. Большинство из них инициируют секрецию ключевого провоспалительного медиатора — фактора некроза опухоли (TNF), а фосфолипаза наряду с этим способствует либерации IL-1; IL-6; γ–интерферона из моноцитов, полиморфноядерных нейтрофилов и Т-лимфоцитов [4-5]. У Р. aeruginosa, как и у других грамотрицательных бактерий, описана система экскреции III типа (своеобразный «молекулярный шприц»), обеспечивающая выведение экзоэнзимов из внутренней среды бактериальной клетки и их транслокацию внутрь эукариотической клетки, непосредственно к мишеням. К веществам, выделяемым данной системой, у синегнойной палочки относятся экзотоксины (ExoS; ExoT; ExoY; ExoU) [5].
Непосредственные внутриклеточные эффекты под действием экзотоксинов заключаются в ингибиции синтеза ДНК, стимуляции апоптоза, изменении клеточной формы, потере способности к локальной адгезии. Доказано, что секреция указанных экзотоксинов сопровождается снижением системного артериального давления и развитием септического шока. Популяции Р. aeruginosa — гетерогенны с позиций способности к синтезу и секреции факторов токсичности: различные штаммы этого микроорганизма обладают различной токсичностью [6-7]. По-видимому, на экспрессию факторов вирулентности оказывают влияние условия внешней среды и процесс индивидуального взаимодействия макроорганизма и бактерий, а также плотность популяции последних.
Одним из механизмов диктующих экспрессию факторов вирулентности служит присущий синегнойной палочке феномен кооперативной чувствительности («Quorum sensing»). Его суть заключается в модификации физиологических функций бактерий при изменении их численности, в результате продукции внеклеточных сигнальных молекул (аутоиндукторов), их детекции и формирования ответной реакции нового качества. Под контролем данной системы находится синтез всех экзотоксинов, а также образование биопленки. Блокада механизмов реализации феномена кооперативной чувствительности у Р. aeruginosa приводит к выраженному снижению вирулентности.
P. aeruginosa обладает способностью к неспецифической адгезии на имлантируемых устройствах (катетеры, эндотрахеальные трубки и др.). Наряду с этим присутствует и механизм специфической адгезии: молекулы, входящие в состав плазменных белков, являются адгезинами для микроорганизмов. Адгезия возрастает при нарушениях мукоцилиарного транспорта, развивающегося у подавляющего большинства пациентов ОРИТ, в послеоперационном или постравматическом периодах, при острой сердечной и дыхательной недостаточности, любой дегидратации и во всех случаях проведения ИВЛ. В дальнейшем микроколонии бактерий объединяются в сплошную биопленку, которая представляет из себя несколько слоев микробных клеток, покрытых общим гликокаликсом (полимер полисахаридной природы). Подавляющее большинство клеток находится в состоянии покоя и характеризуется крайне низкой чувствительностью к воздействию антибиотиков. Периодически возникающие очаги спонтанного размножения служат источником выделения в окружающую среду свободных микробных клеток. Прежде всего данный процесс лежит в основе катетер–ассоциированных инфекций. Распространение по внеклеточным пространствам обеспечивают секретируемые белки, обладающие ферментативной активностью: протеазы, эластаза, липаза. При любой локализации первичного очага инфекции возможно развитие бактериемии, существенно ухудшающей прогноз болезни.
Механизмы приобретенной устойчивости P. aeruginosa к антибиотикам
К антибиотикам, обладающим антипсевдомонадной активностью, относятся β–лактамы, аминогликозиды и фторхинолоны (табл. 1).
Таблица 1. Препараты с потенциальной антисинегнойной активностью и основные механизмы устойчивости
| Группа антибиотиков | Препараты | Основные механизмы устойчивости P. aeruginosa |
| Карбоксипенициллины | Карбенициллин, тикарциллин | Хромосомные β–лактамазы–AmpC |
| Уреидопенициллины | Азлоциллин, пиперациллин | Хромосомные β–лактамазы–AmpC |
| Ингибиторзащищенные пенициллины | Тикарциллин/клавуланат, Пиперациллин/тазобактам | Хромосомные β–лактамазы–AmpC |
| Цефалоспорины | Цефтазидим, цефоперазон, | AmpC, эффлюкс, |
| Цефалоспорины | Цефепим | АmpC (частично) эффлюкс |
| Монобактамы | Азтреонам | |
| Карбапенемы | Имипенем/циластатин, | Утрата поринового канала OprD |
| Карбапенемы | Меропенем | Эффлюкс |
| Аминогликозиды | Амикацин, тобрамицин, нетилмицин, гентамицин | Снижение проницаемости, ферментативная инактивация |
| Фторхинолоны | Ципрофлоксацин, левофлоксацин | Эффлюкс, модификация мишени действия |
| Полимиксины | Полимиксин В |
Мишенью действия β–лактамов являются пенициллинсвязывающие белки (ПСБ), локализованные в цито-плазматической мембране. Различия в уровне антипсевдомонадной активности отдельных β–лактамов в значительной степени объясняются их способностью диффундировать через внешнюю мембрану бактериальной клетки. Наибольшую природную активность проявляют карбапенемные антибиотики (меропенем in vitro активнее имипенема), поскольку они обладают сравнительно небольшой молекулярной массой, кроме этого, их транспорт через внешнюю мембрану облегчает наличие в молекуле двух противоположных электрических зарядов. Далее в порядке убывания антипсевдомонадной активности следуют: цефалоспорины IV поколения (цефепим), азтреонам, цефалоспорины III поколения (цефтазидим, цефоперазон), уреидопенициллины (прежде всего пиперациллин), тикарциллин и карбенициллин. Приобретенная резистентность к β–лактамным антибиотикам является весьма распространенным явлением среди P. aeruginosa. Основным механизмом резистентности является дерепрессия продукции хромосомных β–лактамаз класса С. Мутации, ведущие к дерепрессии синтеза хромосомных β–лактамаз, возникают спонтанно, независимо от воздействия антибиотиков. На фоне лечения карбапенемными антибиотиками штаммов–продуцентов селекции не происходит, так как, обладая устойчивостью к гидролизу хромосомными β–лактамазами, эти препараты подавляют и дерепрессированные мутанты. В меньшей степени подобным свойством обладают цефалоспорины IV поколения.
Главным механизмом устойчивости P. aeruginosa к карбапенемным антибиотикам является утрата в результате мутации одного из пориновых белков (или снижение его экспрессии). Этот механизм в большей степени характерен для резистентности к имипенему, чем меропенему, так как его транспорт может осуществляться и через другие пориновые белки (кроме OprD) [8]. Именно этим объясняются наблюдаемые случаи избирательной устойчивости к имипенему при сохранении чувствительности к меропенему, а иногда и к другим β–лактамам.
Анализ клинических штаммов показывает, что высокий уровень устойчивости к меропенему связан с наличием двух механизмов устойчивости (утратой белка OprD и активацией системы эффлюкса), для проявления высокого уровня устойчивости к имипенему достаточно одного механизма (утраты белка OprD) [9]. Формирование двух механизмов устойчивости (в результате двух одновременных мутаций) намного менее вероятно, чем формирование только одного (в результате одной мутации).
Доказано, что штаммы P. aeruginosa могут обладать одновременно несколькими механизмами резистентности к β–лактамным антибиотикам. Например: дерепрессия хромосомных β–лактамаз может сочетаться с продукцией плазмидных и со снижением проницаемости внешней мембраны.
Фторхинолоны способны проникать через внешнюю мембрану грамотрицательных микроорганизмов (псевдомонад в том числе), минуя пориновые каналы. Липофильные антибиотики достаточно хорошо проникают через цитоплазматическую мембрану в цитоплазму, где локализуются мишени их действия — ферменты топоизомеразы. Из группы гидрофобных антибиотиков наибольшее клиническое значение имеют фторхинолоны, среди них — ципрофлоксацин, обладающий максимальной антипсевдомонадной активностью. Фторхинолоны выводятся из цитоплазмы P. aeruginosa посредством систем активного выброса. Кроме того, важным механизмом устойчивости к ним является и модификация мишеней действия этих препаратов.
На уровне природной активности аминогликозидных антибиотиков особенности строения внешней мембраны и системы выброса P. aeruginosa сказываются лишь в незначительной степени. Величины минимально подавляющих концентраций (МПК) аминогликозидов в отношении P. aeruginosa близки к таковым для других грамотрицательных бактерий. Наибольшую природную активностью в отношении P. aeruginosa проявляют тобрамицин, гентамицин, нетилмицин, сизомицин и амикацин. Устойчивость P. aeruginosa к аминогликозидным антибиотикам формируется посредством трех механизмов: модификация участка связывания рибосом с антибиотиками, снижение транспорта внутрь бактериальной клетки (нарушение проницаемости внутренней или внешней мембраны), ферментативная инактивация антибиотиков. Достаточно часто штаммы P. aeruginosa могут продуцировать одновременно несколько ферментов [14].
Из других антибиотиков потенциальное клиническое значение может иметь полимиксин В. Механизм его действия связан с нарушением целостности внешней мембраны микроорганизма (действие по типу поверхностно активных веществ). Устойчивость к этому антибиотику встречается крайне редко. Проблема заключается в том, что в России отсутствуют лекарственные формы препарата, предназначенные для внутривенного введения.
Современная картина устойчивости клинических штаммов Р. aeruginosa к антибиотикам
В первом многоцентровом проспективном исследовании (NPRS), выполненном в 10 ОРИТ 9 городов России в 1995-1996 гг., P. aeruginosa являлась наиболее частым возбудителем ГИ — 28,8%. Уровень ее устойчивости к имипенему составлял 7,3%; амикацину — 6,9%; ципрофлоксацину — 15,2%; цефтазидиму — 10,7% [3]. Уже через 6 лет ситуация по некоторым АБП заметно изменилась: число нечувствительных штаммов к имипенему достигло в среднем 22,9%; к ципрофлоксацину — 32.8% при сохранении прежней активности к амикацину и цефтазидиму. Наибольшей активностью обладал меропенем — 3% устойчивых штаммов [12]. Однако уже тогда было отмечено, что ситуация в отношении устойчивости к цефтазидиму и меропенему по отдельным стационарам отличалась от общероссийского уровня. Сопоставление отечественных
данных с результатами, полученными в других регионах, свидетельствует о значительной вариабельности распространения устойчивых штаммов. Например, частота резистентных штаммов к меропенему составляла в Канаде 5,1–8,4%; в странах Европы – 10,2–26,2%; Латинской Америке – 23,4–26,2% [11].
Проводимый нами в течение 8 лет (1996–2004) мониторинг чувствительности возбудителей ГИ к антимикробным препаратам в наиболее крупных ОРИТ Екатеринбурга, демонстрирует крайне неблагоприятную тенденцию. На настоящий момент доля резистентных штаммов синегнойной палочки к цефтазидиму возросла до 42,8%; имипенему – до 36%; ципрофлоксацину – до 82,1%; амикацину – до 56,2%. Наиболее тревожная ситуация наблюдается в ОРИТ хирургического профиля с большим потоком тяжелых неотложных пациентов, требующих повторных оперативных вмешательств и длительной искусственной респираторной поддержки, нескольких курсов антибиотикотерапии [11]. Одной из главных причин подобной динамики служит широкое использование в этот период аминопенициллинов, цефалоспоринов I–II поколения, способствующих индукции хромосомных β–лактамаз разрушающих все антибиотики этого класса за исключением карбапенемов и частично цефепима. Рутинное использование практически во всех клинических ситуациях амикацина, пришедшего на смену гентамицину, не только способствовало развитию к нему устойчивости, но и, по–видимому, косвенным образом сказалось на чувствительности синегнойной палочки к имипенему [13].
Выбор схемы антибактериальной терапии синегнойной инфекции
Распространенность и устойчивость во внешней среде, особенности биологии микроорганизма, способность к инвазии и стимуляции системной воспалительной реакции (СВР), а также возможность быстрой реализации нескольких механизмов устойчивости к антибиотикам – основные причины трудностей терапии синегнойной инфекции. Данные многоцентровых исследований в России и других странах убедительно доказывают, что спектр чувствительности P. aeruginosa к АБП в отдельных ОРИТ может иметь существенные различия. Фенотипическое разнообразие синегнойной палочки в госпитальных отделениях прежде всего связано с нозологической структурой больных, частотой использования инвазивных технологий и практикой назначения АБП.
Очевидно, что разработка универсальных рекомендаций невозможна без проведения локального мониторинга характера и уровня антибиотикорезистентности.
В условиях значительной распространенности P. aeruginosa как колонизирующего микроорганизма в ОРИТ (через неделю ИВЛ колонизация НДП регистрировалась у 46% больных), первым шагом должна являться оценка клинической значимости ее выделения из биологического материала пациента.
Для правильной интерпретации результата бактериологического исследования следует принять во внимание несколько обстоятельств: из какого клинического материала получен рост (мокрота, кровь, моча, раневое отделяемое), количественную оценку (число КОЕ/мл), наличие или отсутствие локальных признаков инфекционного процесса, симптомов генерализованной воспалительной реакции и динамику общего состояния пациента в целом.
Если при изоляции синегнойной палочки из крови ситуация однозначно трактуется как инфекционный процесс, то в остальных случаях необходима комплексная оценка перечисленных признаков с принятием индивидуального решения.
Клинически значимыми концентрациями P.aeruginosa являются [14]:
- мокрота (трахеобранхиальный аспират) — не менее 105–106 кое/мл,
- моча — не менее 105 кое/мл,
- рана — не менее 104 кое/мл.
В основе алгоритма выбора схемы антибактериальной терапии должен лежать следующих моментов:
- тяжесть состояния (шок, ПОН);
- локализация инфекционного очага;
- предшествующая антибиотикотерапия (в т.ч. антипсевдомонадными антибиотиками);
- возможность устранения основного заболевания;
- локальные особенности чувствительности к антибиотикам;
- фармакодинамические характеристики препаратов (соотношение площади под кривой концентрации в плазме крови выше минимально подавляющей концентрации и самой МПК).
Рассмотрение больных с указанных позиций позволяет выделить несколько наиболее типичных клинических ситуаций и на этой основе определить рациональные схемы АБТ синегнойной инфекции (табл. 2).
Таблица 2. Выбор схемы антибактериальной терапии синегнойной инфекции у пациентов ОРИТ (до получения результатов о чувствительности)
| Клиническая ситуация, локализация очага | Факторы риска смерти (шок, ПОН, необходимость ИВЛ) | Наличие базы данных о локальной резистентности | Схема АБТ |
| Инфекция НДП во время ИВЛ, раневая инфекция или инфекция МВП | Нет | Нет | Цефепим или цефтазидим или цефоперазон |
| Бактериемия | Нет | Нет | Меропенем |
| Пневмония, раневая инфекция или инфекция МВП | Да | Нет | Меропенем |
| Пневмония, раневая инфекция или инфекция МВП | Да | Да | В зависимости от данных по локальной чувствительности цефтазидим, цефепим, имипенем, меропенем |
Обоснование алгоритма
Известно, что в случае осложнения локального инфекционного процесса септическим шоком или синдромом ПОН прогнозируемая выживаемость не превышает 60% и прогноз прогрессивно ухудшается по мере нарастания тяжести органных расстройств и числа поврежденных систем. В случае же развития синегнойной бактериемии риск развития неблагоприятного исхода увеличивается на 31,2-69% [15]. Вполне очевидно: в обозначенных условиях практически не остается резерва времени на исправление ошибок эмпирической АБТ и предпочтение должно быть отдано препаратам, к которым штаммы P. aeruginosa обладают наименьшим уровнем резистентности. При отсутствии доверительных локальных данных необходимо ориентироваться на результаты отечественных многоцентровых исследований. Есть основания предполагать, что в России в целом, несмотря на рост устойчивости синегнойной палочки ко всем АБП, меропенем остается наиболее активным препаратом [12]. Хотя по результатам проводимого нами мониторинга различие в активности между карбапенемами в отношении данного микроорганизма сократилось [11]. Повсеместно наблюдаемое нарастание частоты устойчивости P. aeruginosa к карбапенемам требует взвешенного и разумного подхода к их назначению. Препараты целесообразно резервировать для эмпирической терапии тяжелых и крайне тяжелых инфекций, вызванных синегнойной палочкой [14].
При получении доверительных лабораторных данных о чувствительности возбудителя к цефтазидиму, цефепиму или ципрофлоксацину и наличии отчетливых позитивных изменений в состоянии пациента может быть избран режим де–эскалации.
Главными доводами в его пользу де–эскалационного режима служат отсутствие доказательств преимущества полного курса назначения карбапенемов перед перед другими схемами терапии с точки зрения выживаемости при синегнойной инфекции. Не меньшее значение имеет снижение селективного давления и экономия материальных средств.
Наличие банка надежных данных, свидетельствующих о низком уровне резистентности (менее 10–15%) P. aeruginosa к карбапенемам или цефалоспоринам с антисинегнойной активностью, вполне позволяет начинать стартовую эмпирическую терапию и с этих антибиотиков.
Клиническое значение антипсевдомонадной активности ципрофлоксацина в последние годы подвергается ревизии, накапливаются клинические и экспериментальные данные о недостаточной способности этого препарата обеспечивать эрадикацию возбудителя при тяжелых инфекциях. Скорее всего, при синегнойных инфекциях ципрофлоксацин целесообразно применять лишь при локализации инфекционного очага в мочевыводящих путях [14].
В ситуации, когда инфекционный процесс не характеризуется как тяжелый сепсис вне зависимости от локализации очага и отсутствует бактериемия, внимание может быть обращено на более дешевые препараты – цефтазидим, цефоперазон, цефоперазон/сульбактам или цефепим.
Следует подчеркнуть, что данные, полученные в России, не позволяют рекомендовать для эмпирической антибиотикотерапии в том числе и среднетяжелых инфекций антисинегнойные пенициллины и ципрофлоксацин – их назначение должно осуществляться только на основании результатов оценки чувствительности возбудителя.
Режим дозирования антибактериальных препаратов с антисинегнойной активностью
С современной точки зрения выбор препарата и режима его дозирования должен строиться на расчете соотношения площади под кривой концентрации в плазме крови и минимально подавляющих концентраций (МПК) в отношении возбудителей ГИ — AUIC (area under inhibitory curvе). Фармакодинамика антимикробных препаратов описывает взаимосвязь между концентрацией антибиотиков в биологических средах организма и бактерицидной активностью. Такой подход позволяет определить не только индивидуальный режим дозирования, но и предсказать клинический ответ на конкретный препарат, снизить риск селекции резистентных штаммов бактерий в конкретном отделении.
Хороший и удовлетворительный клинический ответ наблюдается, когда значение AUIC, получаемое с помощью одного антибиотика или их комбинации, превышает величину 125. Причем если значение AUIC было на уровне 125, элиминация бактерий как при использовании фторхинолонов, так и β–лактамов осуществлялась за 7 дней. Увеличение AUIC до 250 сокращало время микробной эрадикации до 1-2-х суток на фоне применения фторхинолонов, но не β-лактамных антибиотиков [19].
Расчет значений AUIC для потенциально активных антимикробных средств в отношении Pseudomonas aeruginosa подводит к обоснованию назначения препаратов в максимальных дозах с увеличением кратности их введения в некоторых случаях: ципрофлоксацин — 400 мг × 3 в сутки; имипенем — 4,0/сутки; меропенем — 3,0/сутки; цефепим — 6,0/сутки; цефтазидим — 6,0/сутки.
Способ введения препаратов
Инфузионный способ введения цефтазидима, цефепима и меропенема более надежно обеспечивает необходимые для эрадикации микроорганизмов концентрации антибиотиков в крови (превышающие МПК в течение необходимого времени), чем их болюсное назначение [18-19].
Постоянная (24-х часовая) инфузия β–лактамов в условиях ОРИТ также возможна, но представляется не вполне целесообразной, — из-за невысокой стабильности этих препаратов может требоваться постоянное охлаждение раствора. В большинстве исследований длительность инфузии составляла 3 часа.
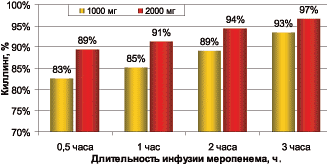
На рисунке 1 приведена вероятность достижения бактерицидного эффекта в отношении синегнойной палочки в зависимости от различных режимов введения меропенема.
Рис. 1. Вероятность достижения бактерицидного эффекта в отношении P. aeruginosa [20]
Таким образом, используя различные комбинации дозы β–лактамного антибиотика с длительностью инфузии, можно добиться улучшения результатов лечения при прежнем уровне затрат, а в ряде случаев возможно и удешевление антибактериальной терапии, так трехчасовая инфузия 1 г меропенема может быть более эффективна, чем введение 2 г в течение 0,5 часа [20].
Роль аминогликозидов
Отсутствие доказательств повышения выживаемости и торможения формирования устойчивости на фоне комбинированной терапии β–лактамами и аминогликозидами у пациентов без нейтропении [21], в условиях значительного повышения резистентности к амикацину, требуют отказаться от облигатного использования антибиотиков данного класса. Показаниями к их назначению как компонента схемы комбинированной терапии могут быть ограничены ситуациями выделения возбудителя, не демонстрирующего чувствительность к какому-либо антибиотику, а проявляющего умеренный уровень устойчивости к нескольким препаратам.
Длительность антибиотикотерапии
В отношении длительности проведения АБТ синегнойной инфекции не существует однозначных рекомендаций и конкретных сроков. Трудность принятия решения о прекращении АБТ обусловлена особенностями взаимодействия пациента и микроорганизма, которые имеют свою специфику в каждом конкретном случае.
Опираясь на существующее понимание инфекционного процесса, вызываемого P. aeruginosa, можно выделить следующие общие критерии, позволяющие принять решение о прекращении АБТ:
- Полноценная хирургическая санация (при необходимости) очагов инфекции.
- Очевидная позитивная динамика воспалительных изменений в ране.
- Регресс генерализованной воспалительной реакции и проявлений органной дисфункции, инфильтративных изменений в легких на рентгенограмме.
- Исчезновение бактериемии и/или снижение плотности бактериального обсеменения в мокроте, полученной путем трахеобронхиальной аспирации, раневом отделяемом и моче, как правило, менее 100 000 кое/мл.
- Отлучение от респиратора и деканюляция трахеи. Необходимо ориентироваться на сочетание перечисленных критериев.
В частности, сохранение субфебриллитета, умеренного лейкоцитоза (менее 11 000) и палочкоядерного сдвига (10 палочкоядерных форм), остаточной инфильтрации на рентгенограмме при общей позитивной динамике по комплексу критериев в целом не должно являться основанием для продолжения АБТ. В особенности для пациентов с кожной формой сепсиса или ВАП, когда выполнена деканюляция трахеи и налажена экспекторация мокроты. В обоих случаях существует возможность для активного местного воздействия на угасающий инфекционный процесс.
Следует помнить, что процесс полной эрадикации бактерий из очага, исключительно с помощью антибиотиков, трудно достижим, особенно со слизистых, сообщающихся с внешней средой, и тем более при наличии инородных тел. Пациент, перенесший критическое состояние, с присоединением госпитальной инфекции, вызванной синегнойной палочкой и выведенный на уровень «самообеспечения» по основным жизненноважным функциям и изложенным критериям, в большей степени нуждается в общей реабилитации вне ОРИТ, профилактике новых инфекционных осложнений, основанной на соответствующем квалифицированном уходе, определенной симптоматической терапии и контроле суперинфицирования.
Литература
- Vincent J-L. Intensive Care Med 2000; 26(1):3–8.
- Trouillet JL., Chastre J., Vuagnant A. et al. Am Rev Resp Crit Care Med 1998;157-531-9.
- Состояние антибиотикорезистентности грамотрицательных возбудителей нозокомиальных инфекций в отделениях реанимации и интенсивной терапии. Межведомств.научный совет по внутрибол.инф. при РАМН и Минздраве РФ, Межрегиональн.ассоциация по клин.микроб. и антимикроб.химиотер.,1997.
- Blackwood L, StoneR., Iglevski B. et al. Infect Immune 1983;39;198-201.
- Frithz- Lindsten E., Du Y., Rosquist r. et al. Mol Microbiol 1997;25: 1125 — 39.
- Kurahashi K., Kajikawa O., Sawa T. et al. J Clin Invest 1999;104:743-50.
- Roy-Burman A., Savel RH, Racine S. et al. J Infect Dis 2001;183:1767-74.
- Edvards J.R. J Antimicrobiol Chemother1995;36(Sup.l A):1-17
- PaiH.,Kim J-W.,Kim J. et al. J Antimicrobiol Chemother2001;45-480-484.
- Turner P.J., The MYSTIC (Meropenem Yearly Susceptubility Test Information Collection) programme. Int J Antimicrob Chemother 1999;13:117-25
- Бейкин Я.Б., Шилова В.П., Руднов В.А. и др. Микробный пейзаж и антибиотикорезистентность госпитальной флоры реанимационных отделений г.Екатеринбурга. Информационное письмо. Екатеринбург, 2004, 19с.
- Страчунский Л.С., Решедько Г.К., Стецюк О.У. и др. Сравнительная активность антисинегнойных антибиотиков в отношении нозокомиальных штаммов Pseudomonas aerunosa, выделенных в отделениях реанимации и интенсивной терапии. Клин.микробиол. и антимикроб.химиотер., 2003; Т.5(№1):35-46.
- Harris A.D., Perencevich E. Rohgmann M et al. Antimicro Agents Chemother 2002; 46:854-858.
- Ефименко Н.А., Гучев И.А., Сидоренко С.В. Инфекции в хирургии. Фармакотерапия и профилактика. Смоленск, 2004, 296с.
- Alliaga L, Diaz F., Cobo F. et al. . Abstracts of the 38th ICAAC 1998 San Diego K-79a.
- Bertrand X., Thouverez M., Talon D. et al. Intensive Care Med 2001; 27:1263-1268.
- Lipman J., Gomersall CD, Gin T. et al. J Antimicrob Chemother 1999;43:309-11.
- Thalhammer F., Traunmuller F., Menyavi IE et al. J Antimicrob Chemother 1999;43:523 -27.
- Schentag J.J.. J Chemother 1999;11:426-429.
- Drusano G.L., Clinical Infectious Diseases 2003; 36 (suppl 1), s42-45
- Paul M., Benuri — Silbiger I., Soares-Veiser K., Leibovici L. BMJ,doi:10.1136/bmj.308028.520995.63(published 2 March 2004).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)