Как утверждают многие специалисты, очень высокая кислотность организма нарушает нормальное функционирование систем органов, и они становятся беззащитными перед разнообразными бактериями и вирусами.
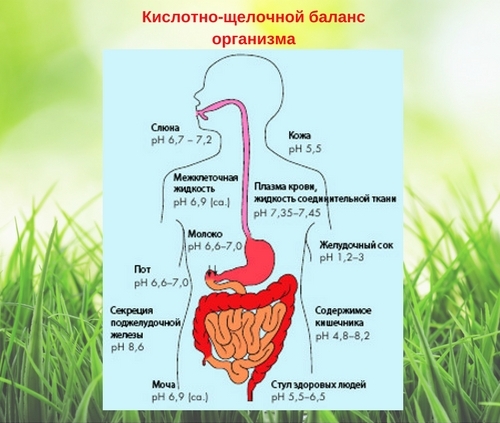
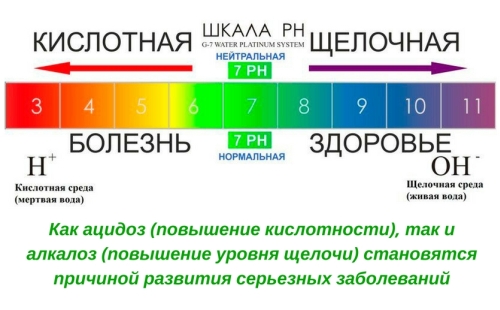
Показатель рН – это число атомов водорода в определённом растворе. Если он равен 7, то это нейтральная среда, если от 0 до 6,9, то это кислая среда, от 7,1 до 14 – щелочная. Как известно, человеческое тело на 80% состоит из водного раствора. Организм постоянно старается уравновесить соотношение кислоты и щелочи в этом растворе.
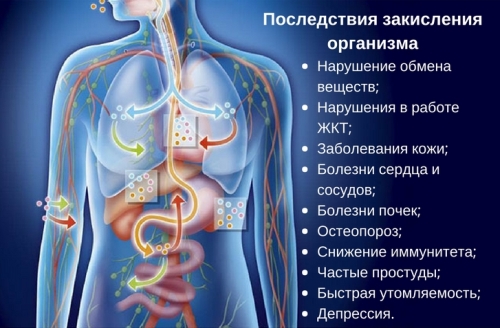
Последствия нарушения кислотно-щелочного баланса в организме
Если кислотно-щелочной баланс нарушается, то это может вызвать серьёзные нарушения в организме. При употреблении в пищу продуктов, богатых на кислоту, и недостаточном количестве воды возникает закисление всего организма. К таким продуктам относятся газированные напитки, крупы, продукты, содержащие сахар, заменители сахара, хлебобулочные изделия, мясные продукты и мясо.
Закисление опасно тем, что ухудшает перенесение кислорода по организму, начинают плохо усваиваться микро- и макроэлементы. Это может вызывать, прежде всего, нарушения со стороны пищеварительной системы, клеточного обмена, а также вызывает сердечно-сосудистые заболевания, болезни кожи, снижение плотности костей, иммунитета и другое. В среде, кислотно-щелочной баланс которой указывает на кислую, быстро растут и размножаются разные паразиты, в том числе вирусы, грибки и бактерии.
Нобелевский лауреат Отто Варбург получил свою премию за открытие, что в среде, богатой на кислород, раковые клетки не размножаются, а позже было ещё доказано, что в такой среде малоактивны вирусы, бактерии и грибки. Чем выше уровень pH, имеющий щелочную реакцию, тем выше концентрация молекул кислорода (калоризатор). В кислой среде происходит повышение концентрации CO2 и образование молочной кислоты, что создает предпосылки для роста раковых клеток.
Как проверить pH организма?
Проверить свой кислотно-щелочной баланс достаточно просто с помощью специального теста – тест-полосок лакмусовой бумаги, которые можно купить в аптеке. Самый оптимальный рН-баланс равен 6,4-6,5. Определять свой кислотно-щелочной баланс лучше всего за час до еды, или через два часа после.
pH мочи может колебаться в течение дня. Если утром его значение 6,0-6,4, а вечером 6,4-7,0 – нет повода для беспокойств. Однако если тест показывает 5,0 и ниже, то pH мочи резко закислен, а если 7,5 и выше, то преобладает щелочная реакция. По значению рН мочи можно определить насколько хорошо в нашем организме усваиваются минералы, например кальций, натрий, магний.
Что касается рН слюны, то его значение указывает на активную работу ферментов пищевого тракта, в особенности – печени и желудка. Нормальная кислотность смешанной слюны равна 6,8-7,4 pH. Измеряют её обычно в полдень натощак или через два часа после еды. Пониженная кислотность ротовой полости нередко приводит к кариесу, болезням десен, неприятному запаху изо рта.
Что такое кислая и щелочная среда?
В медицине существует такой термин, как «ацидоз» – это повышенная кислотность. К такому состоянию часто приводит употребление большого количества алкогольных напитков и осложнения сахарного диабета. При повышенной кислотности могут наблюдаться проблемы с сердцем и кровеносными сосудами. Человек может достаточно быстро набирать вес. Очень часто в таких случаях встречаются заболевания почек, мочевого пузыря и снижение иммунитета.
Повышение уровня щелочи в организме называется алкалоз. В этом случае также наблюдается плохое усвоение минеральных веществ. Причиной такого состояния в организме может быть длительное употребление лекарственных веществ, содержащих большое количество щелочи. Алкалоз встречается достаточно редко, но тоже могут вызвать серьёзные и негативные перемены в нашем организме. К ним относятся заболевания кожных покровов и печени, неприятный и ярко выраженный запах изо рта и другие.
Как поддерживать нормальный pH?
Для поддержки оптимального кислотно-щелочного баланса организма нужно пить достаточное количество воды (30 мл на 1 кг тела). Что касается еды, то продуктов, богатых на щелочь, должно быть в несколько раз больше, чем продуктов кислотного характера.
Растительная пища, как овощи и фрукты, способствует образованию щелочной реакции, а злаки, мясо, обработанная пища в виде колбас, полуфабрикатов, хлебобулочных изделий – кислой. Чтобы поддерживать оптимальный кислотно-щелочной баланс, необходимо, чтобы в рационе преобладала растительная пища.
Врачи утверждают, что в наших же с вами интересах поддерживать правильный уровень кислоты и щелочи в организме. Только при оптимальном рН-балансе наш организм хорошо усваивает полезные вещества.
В нашем организме есть естественные механизмы, которые налаживают кислотно-щелочной баланс. Это буферные системы крови, дыхательная система и система выделения. Когда эти процессы нарушаются, то наш организм выделяет кислоты в желудочно-кишечный тракт, в почки и лёгкие, а также нашу кожу. Также он способен нейтрализовать кислоты минеральными веществами и накапливать кислоты в мышечной ткани (calorizator). Если вы ощущаете усталость, то это может значить, что железо гемоглобина крови нейтрализует кислоту. Если наблюдаются головокружения, головные боли, судороги и бессонница, то это может сигнализировать о том, что в нервных окончаниях, мышечной ткани и костях используется магний.
Вот сколько проблем со здоровьем может возникнуть из-за нарушения кислотно-щелочного баланса. Не пускайте дело на самотёк, возьмите во внимание то, что профилактика – это залог крепкого здоровья. Следите регулярно за рН организма во избежание многих заболеваний.
Автор: Жанна Ш. (специально для Calorizator.ru)
Копирование данной статьи целиком или частично запрещено.
Очень важно, что величины произведений растворимости разных сульфидов различаются чрезвычайно сильно. Это позволяет,, надлежащим образом регулируя величину pH раствора, разделять катионы разных металлов путем осаждения их в виде сульфидов. Так, из качественного анализа известно, что сульфиды IV и V аналитических групп осаждаются сероводородом в кислой среде, так как величины их произведений растворимости очень малы (порядка 10 29 J, менее). Наоборот, осаждение катионов П1 аналитической группы (произведение растворимости порядка 10 —10″ ) сероводородом или сульфидом аммония проводят в щелочной среде (при pH около 9). Аналогичные методы нередко применяются и в количественном анализе, например для отделения катионов меди, висмута, олова и других металлов от катионов железа и т. д. Регулируя кислотность раствора при осаждении сульфидов, можно количественно разделять катионы, принадлежащие к одной и той же аналитической группе. Так, в присутствии уксусной кислоты цинк можно количественно отделить от железа, в присутствии 10 н. раствора НС1 — отделить мышьяк от олова и сурьмы и т. д. [c.121]
В щелочной среде (например, при помощи натрия в спирте или же амальгамы натрия во влажном эфире и т. п.), в которой оксимы почти не омыляются, можно их выделить при восстановлении нитросоединений [c.347]
Восстановление в щелочной среде осуществляется главным образом при помощи амальгамы натрия [47], а в нейтральной — обычно амальгамой алюминия [48]. [c.275]
В 56 было показано, что точка эквивалентности может находиться в нейтральной, кислой или щелочной средах в зависимости от природы титруемых веществ. Для того чтобы правильно выбрать индикатор, нужно знать, как изменяется pH в процессе титрования, вблизи точки эквивалентности, какое значение pH имеет раствор в точке эквивалентности. Чтобы ответить на все эти вопросы прибегают к расчету и построению кривых титрования./Кривые титрования в методе кислотно-основного титрования являются графическим изображением изменения pH раствора при постепенном прибавлении рабочего раствора к определенному количеству исследуемого раствора., Для упрощения вычислений (что не приводит к заметным ошибкам) обычно не учитывают [c.256]
В. Получение нитроспиртов взаимодействием нитропарафинов с альдегидами в щелочной среде [c.324]
Как уже упоминалось, нитропарафины могут быть превращены в кетоны окислением в щелочной среде такими окислителями, как перманганат калия, перекись водорода, озон и т. п. [c.348]
Иодометрическое титрование нельзя проводить в щелочной среде, так как иод реагирует со щелочами [c.399]
Переход диоксимов в изоксазолы уже давно известен, причем эта реакция в щелочной среде протекает самопроизвольно. [c.270]
Как уже упоминалось (см. стр. 271), нитропарафины в щелочной среде моментально реагируют с хлором или бромом с образованием галоиднитросоединений, в которых атом галоида связан с тем же атомом углерода, что и нитрогруппа. [c.339]
Количественный учет всех противоположных влияний здесь довольно сложен и требует знания констант устойчивости комплексов, а также величин перенапряжения водорода при разных значениях pH. Однако на опыте установлено, что электролитическое определение многих металлов (цинка, никеля и т. д.) из растворов, содержащих аммиачные, цианистые, оксалатные и другие комплексы, вполне возможно, и обычно дает хорошие результаты. К нему приходится прибегать всегда, когда хотят вести в щелочной среде электролитическое осаждение металла, гидроокись ко-торо о малорастворима. Кроме понижения концентрации Н -ионов [c.435]
Получение нитроспиртов взаимодействием нитропарафинов с альдеги дами в щелочной среде. ………… [c.618]
II пределах 10 —Ю , требуется создать нейтральную или щелочную среду (pH 7). [c.86]
Осаждение магния о-оксихинолином ведут в присутствии аммиака, т. е. в щелочной среде (pH 9,5—12,7). [c.415]
В щелочной среде (точнее, при pH 4,4) рассматриваемый индикатор оказывался зеленого цвета (сочетание желтого и синего цветов). В кислой среде (при pH сложение розового и синего цветов). При pH, соответствующем рТ данного индикатора (т. е. 4), окраска раствора слагается из розовато-оранжевого и синего цветов, являющихся дополнительными друг к другу, и представляется поэтому. бледно-серой, почти бесцветной. Момент этого обесцвечивания зеленого или фиолетового раствора при титровании с рассматриваемым индикатором уловить гораздо легче (особенно при искусственном освещении), чем появление пере.ходной розовато-оранжевой окраски самого метилового оранжевого. [c.256]
Особое значение эпихлоргидрин имеет для получения так называемых эпоксидных смол. Их получают взаимодействием эпихлоргидрина с двухатомными фенолами, особенно с 4,4 -ди-оксидифенилпропаном. Это соединение, известное нод названием диан , получают конденсацией ацетона и фенола в присутствии концентрированной серной кислоты. В щелочной среде из диана и эпихлоргидрина образуется диандиглицидный эфир, присоединяющий к себе еще молекулы диана с одновременным разрушением эпоксидного кольца. Таким путем получают полиэфир со степенью полимеризации, достигающей 15 [8] [c.176]
Реакция определения никеля (И) диметилглиоксимом (ОНг) в щелочной среде в присутствии окислителей получила большое распространение. В результате реакции образуется соединение, растворы которого окрашены в бурый цвет (отношение N1 [)Нг = = 1 3). Максимальное поглощение наблюдается при >, = 470 нм-, значение е= 13 000. В качестве окислителя используют раствор иода. Никель может быть определен указанной реакцией в сталях в присутствии ванадия, молибдена. Вольфрам, хром и титан могут присутствовать до 18%. Мешают медь, кобальт и все элементы, ионы которых дают осадки гидроокисей в щелочной среде. Это первый недостаток метода, второй — малая чувствительность. [c.493]
Если продукты восстановления (или окисления) адсорбируются на электроде, экранируя заметную часть его поверхности 0, которой уже нельзя пренебречь, то уравиение (17.67) должно быть модифицировано в соответствии с кинетическими особенностями, отличающими данную электродную реакцию. Этот случай целесообразно рассмотреть на примере реакции катодного выделения водорода из кислых и щелочных сред [c.361]
Независимо от того, происходит разряд в кислой или в щелочной среде, его непосредственным продуктом будут адсорбированные электродом атомы водорода . Для стационарного протекания электролиза необходимо поддерживать постоянной поверхностную концентрацию атомов водорода, т. е. обеспечивать их непрерывный отвод с поверхности катода. Атомы водорода могут удаляться тремя путями каталитической рекомбинацией, электрохимической десорбцией и эмиссией. При каталитическом механизме отвод атомов водорода происходит за счет их рекомбинации в молекулы с одновременной десорбцией [c.403]
Использование продуктов хлорирования нен-танов [19]. Как уже указывалось, продукты хлорирования пентанов применяются для получения амиловых спиртов. С этой целью смесь моно-хлорпентанов, выкипающую в пределах 85—107°, подвергают гидролизу в щелочной среде в присутствии олеата натрия. Процесс ведут при 170— 180° под давлением. Олеат натрия является диспергирующим агентом, улучшающим контакт хлорида с омыляющей средой. Схема установки ноказапа на рис. 64. [c.121]
При обработке нитропарафнпов в щелочной среде окислителями первичные нитропарафины превращаются в альдегиды или карбоновые кислоты, а вторичные нитропарафины в кетопы [39]. [c.132]
При действии хлора или брома на нитросоединения в щелочной среде мгновенно образуются геминально-замещеиные галопдоиитросоединеиия. Первичные нитросоединения могут присоединять два атома галоида, вторичные— только один. Действием гипохлорита на нитрометан получают хлорпикрин (N030013). В первую мировую войну хлорпикрин применялся как боевое отравляющее вещество, но в настоящее время он утратил это зна- [c.132]
Наилучшие результаты дает омыление содовым раствором, так как в этом случае сводится к минимуму образование побочного продукта — диаллилового эфира, которого получается тем больше, чем концентрированное омыляющип раствор щелочи. При применении соды в качестве омыляю-щего раствора необходимо непрерывно удалять образующуюся углекислоту. При этом имеют место значительные потери органического вещества. Для избежания этого в реакционную смесь непрерывно добавляют натриевую щелочь в количестве, необходимом для поддержания щелочности среды, [c.174]
Получать хлороформ прямым хлорированием метана или его моно-и дихлорпроизводных невозможно. Одним из способов его получения является частичное восстановление четыреххлористого углерода. Французская фирма Юзин дю Рон получает хлороформ с выходом 90% путем восстановления четыреххлористого углерода теплой взвесью гидрата закиси железа в щелочной среде [165]. Действием фтористого водорода на хлороформ в присутствии фтористой сурьмы получают монохлордифторметан (фреон-22) [166]. [c.210]
Кипящую в пределах 85—107° смесь монохлорпентанов подвергали гидролизу в щелочной среде при температуре 170—180° и повышенном давлении в присутствии олеиновокислото натрия. Поведение индивидуальных изомеров хлорпентана при этом весьма сильно различалось в зависимости от характера связи атома хлора —с первичным, вторичным или третичным углеродом. [c.218]
Олеиновокислый натрий, помимо его эмульгирующего действия, выполняет при омылении хлористого амила еще одну функцию. Он участвует в реакции двойного обмена хлористого алкила, приводящей к образованию сложного эфира соответствующей жирной кислоты, которая затем быстро омыляется в щелочной среде с регенерацией олеиново -кислой соли и образованием спирта [c.219]
Практически галоидирование производится, в щелочной среде при помощи гипогалогенидов. Этим путем получается, например, из нитро-метана и гипохлорита натрия хлорпикрин (ОзМ-ССи) [23]. [c.272]
НИИ 4 моля перекиси водорода и 2—3 моля щелочи [39]. Количественное превращение вторичных нитропарафннов в кетоны происходит при озонировании в щелочной среде [40]. [c.275]
Геминальпозамешенные динитропарафины, как 2,2-динитробутан, можно получить и электролитическим путем. При электролизе 2-нитро-бутана при температуре 70—90° в щелочной среде образуется смесь, состоящая нз 70% 3,4-динитро-3,4-диметилгексана с точкой плавления [c.340]
Разделение на фракции проводили ректификацией. О положении хлора в молекуле судили по физическим константам фракций (температура кипения, показатель преломления, плотность), сравнивая их с литературными данными. Омылением фракции, принятой за первичный хлористый ундецил, получен спирт, который был переведен в ундекано-вую кислоту окислением перекисью водорода в щелочной среде. Выход по отдельным стадиям авторы не приводят. [c.558]
Окислив продукты нитрования н-додекана перекисью водорода в щелочной среде, Грундман смог получить кетон, который состоял в основном из метилдецилкетона (см. также главу IV, стр. 274) [c.562]
Если же по Азингеру [79] с.месь нитропарафннов перевести количественно в кетоны обработкой озоном в щелочной среде, то соотношение отдельных изомерных кетонов точно отвечает соотношению нитропарафинов в исходной смеси. Продукт обработки такой смеси кетонов семикарбазидом уже не кристаллизируется он маслянист и иэ него семикарбазон додеканона-2 выделяется с незначительными выходами. [c.563]
Следовательно, чтобы осаждение СаСОз было полным, его нужно вести в щелочной среде, именно при pH 9,7. [c.88]
Кроме того, в щелочной среде увелич вается перенапряжение водорода. Однако наряду с этим понилсается окислительно-восстаио вите.тьный потенциал пары Zn +ZZn, так как в указанных условиях большая часть Zn -ионов оказывается превращенной в анионы Zn02 (при избытке сильной щелочи) или в катионы [2п(МНз)4] + (в аммиачной среде). [c.435]
Разнообразны продукты, получаемые при конденсации ацетона в щелочной среде [28]. При температуре 10 — 20 °С в м етанольном растворе ацетон димерпзуется в присутствии небольших количеств щелочи в диацстоповый спирт, из которого получаются следующие вещества [c.144]
В водном 0,1 н. растворе H2SO4 скорость разложения в 7 раз выше, чем в водном 0,1 н. растворе NaOH, и в 60 раз выше, чем в воде. Добавка тенсида повышает скорость разложения в кислой и щелочной среде [289]. [c.280]
Аналогичные результаты были получены при изучении реакции электровосстановления кислорода. Эта реакция играет важную роль в процессах коррозии металлов и при работе элементов с воздушной деполяризацией. Интерес к ней особенно возрос в последние годы в связи с проблемой нелосредствениого превращения химической энергии в электрическую при помощи топливных элементов. В настоящее время выяснены основные кинетические особенности реакции восстановления кислорода в кислых и щелочных средах (Н. Д. Томашев, А. И. Красильщиков, 3. А. Иофа, В. С. Багоцкий и др.). Так, электровосстановление кислорода на ртути, серебре и золоте оказалось возможным описать следующими уравнениями [c.441]
Теоретические основы аналитической химии 1980 (1980) — [
c.46
]
Катодная защита от коррозии (1984) — [
c.395
,
c.396
]
Справочник по общей и неорганической химии (1997) — [
c.0
]
Производство азокрасителей (1952) — [
c.64
,
c.66
]
Человек может быть здоров, если в его организме нормально протекает обмен веществ. Основной показатель обменных процессов в организме – это кислотно-щелочное равновесие (КЩР). Нормальное ph крови – 7,37 – 7,47. Сдвиг ph ниже 7,37 свидетельствует о переокислении (ацидозе), а выше 7,47 – о переощелачивании (алкалозе) организма.
Хотите прожить до 100 лет и больше? Тогда следуйте в своем питании рекомендациям йогов. Еще с давних времен они разделили пищу на кислую и щелочную. Если первая несет болезни и приводит к старению, то вторая дает силы и продлевает годы. Щелочная пища должна в вашем рационе в три раза превышать кислую.
Соотношение минеральных веществ кислотного и щелочного характера в некоторых продуктах питания
- Продукты; Соотношение минеральных веществ (%)
- ; кислотного характера; щелочного характера; Разность*
- Яйца куриные; 72,7; 27,3; -45,4
- Рис; 72,6; 27,4; -45,2
- Хлеб пшеничный; 72,0; 28,0; -44,0
- Мясо постное; 70,8; 29,2; -41,6
- Творог; 70,1; 29,9; -40,2
- Макароны; 69,7; 30,3; -39,4
- Рыба; 68,8; 31,2; -37,6
- Стручковые; 61,8; 38,2; -23,6
- Сало свиное; 58,9; 41,1; -17,8
- Белая мука грубого помола; 58,3; 41,7; -16,6
- Масло сливочное; 56,1; 43,9; -12,2
- Сыр; 54,4; 45,6; -10,8
- Ржаной хлеб из цельного зерна; 53,9; 46,1; -7,8
- Орехи; 52,2; 47,8; -4,4
- Какао; 51,8; 48,2; -3,6
- Свекла; 45,6; 54,4; 8,8
- Бобы зеленые; 42,3; 57,7; 15,4
- Шпинат; 40,9; 59,1; 18,2
- Помидоры; 38,0; 62,0; 24,0
- Клубника; 37,4; 62,6; 25,2
- Картофель; 36,6; 63,4; 26,8
- Лук; 35,5; 64,5; 29,0
- Морковь; 28,9; 71,1; 42,2
- Яблоки; 27,3; 72,7; 45,4
- Крыжовник; 25,5; 74,5; 49,0
- Огурцы; 25,0; 75,0; 50,0
- Слива; 23,1; 76,9; 53,8
- Лимоны; 20,5; 79,5; 59,0
- * Преобладание: (нет знака) — продукт щелочного характера (-) — продукт кислотного характера характера.
Лимонный сок и ферменты кураги, чернослива, яблок, клюквы, и других ягод (кислых на вкус) обладают свойствами конвертируемости (превращения).
В ходе реакции пищеварения они становятся сильными ощелачивающими веществами. Все цитрусовые (лимон, апельсин) первоначально кажутся кислыми, но их окончательный эффект в организме является щелочным.
Кислые (закисляющие) продукты: чай, кофе, алкоголь, табак, безалкогольные напитки. Все сладкие продукты и конфеты (содержащие белый сахар). Все продукты питания животного происхождения: мясо, яйца, рыба, домашняя птица и др. Орехи, горох, и бобы. Молочные продукты (стерилизованное и пастеризованное молоко, сыр, творог и масло). Жиры и масла. Все хлебные злаки и бобовые: пшеница, кукуруза, рис и бобы.
Щелочные продукты. Все фрукты (свежие или вяленые), включая цитрусовые. Все свежие овощи и зеленые корнеплоды (кроме гороха и бобов). Проростки.
Частично щелочные продукты. Свежие зеленые (в стручках) бобы, горох, зерно и просо. Свежие орехи: миндаль, кокос, бразильский орех. Размоченные семена и орехи. Свежее сырое молоко (не пастеризованное) и творог.
Рекомендуются при мочекаменной болезни следующие продукты питания:
Следует учитывать, что главная задача лечебного питания при мочекаменной болезни — сдвиг кислотно-щелочного равнове сия в организме в щелочную сторону, для чего в каждом кон кретном случае используются определенные продукты и блюда.
Пшеничный и ржаной хлеб из муки 1-го и 2-го сорта, выпечные изделия. Ограничиваются изделия из сдобного теста. Супы овощные, картофельные, с добавлением круп, молочные; окрошка, свекольник, борщи, щи.
Нежирные виды и сорта мяса, птицы, рыбы (после отварива ния) в виде тушеных, запеченных, жареных блюд, изделий из котлетной массы) — 2—3 раза в неделю по 150 г (мяса) или 160 г (рыбы). Возможно сочетание мяса и рыбы в равных ко личествах.
Молоко, кисломолочные напитки, творог и блюда из него, сметана, сыр.
В изобилии — сырые овощи, картофель, фрукты и ягоды в лю бой кулинарной обработке, особенно обладающие выражен ным ощелачивающим действием: лимоны, цитрусовые, свек ла, огурцы, арбузы, персики, курага, урюк, груши, сухофрукты. Можно использовать сок черной редьки с медом, обладаю щий мочегонным действием и способствующий растворению камней.
Кисели молочные, мармелад, варенье, мед, не шоколадные конфеты.
Салаты из свежих и квашеных овощей, из фруктов; винегре ты; икра из овощей.
Соусы — молочный, сметанный, томатный, на овощном отваре. Укроп, зелень петрушки, пряности (ванилин, корица, лавро вый лист, лимонная кислота).
Напитки: соки фруктов, ягод, овощей, морсы, вода с соками, квас. Компоты, отвар шиповника, пшеничных отрубей. Чай некрепкий, с лимоном, молоком; некрепкий кофе с молоком. Способствует удалению мочевых камней морковный сок.
Масло сливочное несоленое и топленое, растительные масла.
Одно яйцо в день в любой кулинарной обработке.
Блюда из любых круп, но в умеренном количестве.
Доктор Harold Hawkins, Южная Калифорния, при обследовании пациентов выявил 48 % слишком щелочных и только 32 % слишком кислотных. В этих исследованиях он ссылался не на желудок, а на кровь, обнаружив, что слюна близка к крови.
Функция поджелудочной железы зависит от уровня соляной кислоты в желудке. Дефицит возбуждения, необходимого для работы поджелудочной железы, может привести к нарушению усвоения белка, в дополнение к изначальному недостаточному усвоению белка.
Кальций и натрий — ощелачивающие, а фосфор и калий — закисляющие минералы. Яблочный уксус — это разведенный раствор кислого калия.
При ацидозе — закислении внутренней среды — резко падает активность внутриклеточных процессов, органы и системы организма работают с большим напряжением. В результате возникшего ацидоза ухудшается самочувствие, падает работоспособность и возникает депрессия. Длительный ацидоз часто приводит к разного рода тяжелым заболеваниям. Длительное перекисление крови может привести к декальцинированию (распаду костного вещества), когда для снижения закисленности внутренней среды организм вынужден использовать кальций, беря его из костной ткани скелета. При ацидозе (закисление организма) исключаются продукты: сахар, дрожжевой хлеб, пшеница, кукуруза, спиртные напитки, кофе, крепкий чай и курение.
Продукты, которые могут помочь восстановить баланс — это проростки пшеницы и не только, для этого нужно выбирать качественное зерно. Очень хорошо подходит и зелёная гречка.
Органическое зерно (пшеница, голозерный овес, зеленая греча, булгур, амарант, киноа, семена льна, пшеницу эйкорн, можно купить здесь. Смотрите Семена и зёрна. Проверенное качество.
Продукты на кислотной основе
Мясо, колбасные изделия, нежирные молочные продукты (творог и сыр), сахара и сладкое любого вида, зерновые (особенно очищенные), сладкие освежительные напитки, кофе.
Сильное окисление в организме вызывают яйца, виноград и сок лимона.
Окислителями также являются алкогольные напитки, кофе, чай, шоколад, табак.
Одним из основных положений раздельного питания является сбалансированность потребляемых продуктов по химической реакции и сохранение необходимого для жизнедеятельности организма кислотно-щелочного равновесия за счет принимаемой пищи. Теперь уже известно, что кислоты и щелочи поступают во внутреннюю среду организма двумя путями: через пищу и благодаря их образованию в процессе обмена веществ. В результате переваривания одних продуктов образуются кислоты, поэтому они относятся к разряду кислотообразующих
, а при переваривании других — щелочи, следовательно, они входят в число щелочеобразующих
продуктов питания. Итогом преобразования первых являются мочевина и мочевая кислота. Они выделяются через почки. При обильном потреблении кислотообразующих продуктов, организм может прийти к перекислению. Именно это является основной причиной возникновения многочисленных болезней. Накопление в организме молочной кислоты и углекислоты вызывает чувство усталости, ведет к возникновению боли в нервных окончаниях.
Смещение обмена веществ в сторону ацидоза — закисления жидкостных сред организма может привести к депрессии, к ощущению подавленности и разбитости. Продукты растительного происхождения, которые носят щелочеобразующий характер, напротив, смещают кислотно-щелочную реакцию крови, лимфы и межтканевой жидкости в щелочную сторону, способствуя повышению жизненного тонуса и настроения.
Для нормальной работы организма реакция его внутренней среды должна быть щелочная, и следовательно, нужно вести активный образ жизни, больше двигаться на свежем воздухе, чтобы через легкие и почки выводить излишки кислот в виде углекислого газа и воды.
С учетом этого все продукты в зависимости от их кислотных или щелочных свойств делятся на следующие четыре группы:
• Сильно кислотообразующие: мясо, колбаса, рыба, яйца, сыр, сласти, продукты из белой муки, алкоголь и кофе.
• Слабо кислотообразующие: творог, сметана, орехи и продукты из муки грубого помола.
• Слабо щелочеобразующие: сухие фрукты, сырое молоко и грибы.
• Сильно щелочеобразующие: овощи, свежие фрукты, картофель и зеленый салат.
Защелачивают кровь и ткани — овощи и фрукты.
Ощелачивающее действие оказывают органические соли со щелочными металлами. Эти соли в больших количествах присутствуют в продуктах растительного происхождения.
Фруктовые соки, попадая в ЖКТ, вначале проявляют кислую реакцию и на некоторое время повышают общую кислотность желудочного и кишечного содержимого, стимулируют дополнительное выделение соляной кислоты, что также приводит к повышению закисленности желудка. Такое действие у цитрусовых соков. Но в крови, в лимфе и в тканевой жидкости их действие становится противоположным: они превращаются в ощелачивающие агенты.
Защелачивающее питание
Защелачивающие дни можно ввести один раз в неделю, пример рациона на такие дни:
- только овощной, или арбузный день (2-2,5 кг арбуза),
- грейпфрутовый день (5-6 штук за день)
- пучок петрушки утром (основной завтрак после этого через 20-30 минут), или петрушка вместе с каждым приёмом пищи в течение всего дня
- 500 г размоченной кураги на весь день.
Одного раза в неделю защелачивающего питания часто хватает для поддержки здоровья.
Тёртая сырая свёкла, морковь, мелко нарезанная красная и белокочанная капуста, укроп, сельдерей, лук и чеснок должны непременно входить меню — это щелочное питание.
Щелочной джем, рецепт:
150 г кураги
100 г сушеных яблок
60 г изюма
4 стакана свежевыжатого сока апельсинового.
Варить все ингредиенты на слабом огне, пока фрукты не станут мягкими.
Натрия гидрокарбонат (пищевая сода)
На особом месте находится натрия гидрокарбонат (пищевая сода). Раньше он применялся очень широко (как и другие щелочи) в качестве средства при повышенной кислотности желудочного сока, язвенной болезни желудка. Гидрокарбонат натрия (или сода) входит, как главный ингредиент, в состав нашей крови. Сода входит в состав плазмы крови, а также лимфоплазмы, в которой находятся лимфоциты. Возможно, сода энергетически питает лимфоциты — клетки, ответственные за иммунный ответ организма.
Профилактика кариеса. Кислоты, образующиеся во рту в результате жизнедеятельности бактерий, разрушают эмаль зубов. Эти кислоты можно нейтрализовать, несколько раз в день полоща рот раствором пищевой соды. Можно поступить иначе: смочите зубную щетку водой, опустите ее в соду и почистите зубы. Сода, кроме того, оказывает легкое абразивное действие: она отполирует зубы, не повреждая эмали.
При ринитах, стоматитах, ларингитах, конъюнктивитах применяют 0,5-2% раствор соды.
Средство от курения: полоскать рот раствором пищевой соды (1 столовая ложка на 200 мл воды).
Сода представляет собой соединение катиона натрия и аниона гидрокарбоната, которое при введении в организм активно включается в коррекцию кислото-щелочного равновесия. При многих тяжелых заболеваниях в клетках и тканях организма наблюдается ацидоз (или закисление организма), недостаток катионов калия и избыток натрия, что приводит к подавлению энергетических биохимических обменных процессов в клетках, снижению усвоения кислорода, уменьшению жизнеспособности как каждой клетки, так и всего организма. Положительное оздоравливающее действие соды просто уникально. Благодаря введению анионов угольной кислоты повышается щелочной резерв организма: анион угольной кислоты выводит через почки избыток анионов хлора и натрия, что приводит к уменьшению отеков, снижению повышенного давления, в результате чего повышается валентность тканевых буферных систем, что создает условие для вхождения катиона калия в клетки, и тем самым объясняется калий-сберегающий эффект соды.
При тяжелом шоке получены хорошие результаты лечения внутриартериальным введением раствора соды. Отмечено положительное действие соды при морской болезни.
Применение соды и глюкозы приводит к значительному улучшению мозгового кровообращения, увеличению напряжения и поглощения кислорода клетками мозга.
Источник: www.edka.ru