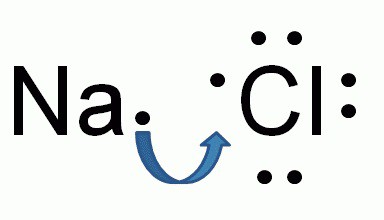Поваренная соль — это хлорид натрия, применяемый в качестве добавки к пище, консерванта продуктов питания. Используется также в химической промышленности, медицине. Служит важнейшим сырьем для получения едкого натра, соляной кислоты, соды и других веществ. Формула соли поваренной — NaCl.
Образование ионной связи между натрием и хлором
Химический состав хлорида натрия отражает условная формула NaCl, которая дает представление о равном количестве атомов натрия и хлора. Но вещество образовано не двухатомными молекулами, а состоит из кристаллов. При взаимодействии щелочного металла с сильным неметаллом каждый атом натрия отдает валентный электрон более электроотрицательному хлору. Возникают катионы натрия Na+ и анионы кислотного остатка соляной кислоты Cl—. Разноименно заряженные частицы притягиваются, образуя вещество с ионной кристаллической решеткой. Маленькие катионы натрия расположены между крупными анионами хлора. Число положительных частиц в составе хлорида натрия равно количеству отрицательных, вещество в целом является нейтральным.
Химическая формула. Поваренная соль и галит
Соли — это сложные вещества ионного строения, названия которых начинаются с наименования кислотного остатка. Формула соли поваренной — NaCl. Геологи минерал такого состава называют «галит», а осадочную породу — «каменная соль». Устаревшей химический термин, который часто употребляется на производстве, — «хлористый натрий». Это вещество известно людям с глубокой древности, когда-то его считали «белым золотом». Современные ученики школ и студенты при чтении уравнений реакций с участием хлорида натрия называют химические знаки («натрий хлор»).
Проведем несложные расчеты по формуле вещества:
1) Mr (NaCl) = Ar (Na) + Ar (Cl) = 22,99 + 35,45 = 58,44.
Относительная молекулярная масса составляет 58,44 (в а.е.м.).
2) Численно равна молекулярному весу молярная масса, но эта величина имеет единицы измерения г/моль: М (NaCl) = 58,44 г/моль.
3) Образец соли массой 100 г содержит 60,663 г атомов хлора и 39,337 г натрия.
Физические свойства поваренной соли
Хрупкие кристаллы галита — бесцветные или белые. В природе также встречаются месторождения каменной соли, окрашенной в серый, желтый либо голубой цвет. Иногда минеральное вещество обладает красным оттенком, что обусловлено видами и количеством примесей. Твердость галита по шкале Мооса составляет всего 2-2,5, стекло оставляет на его поверхности черту.
Другие физические параметры хлорида натрия:
- запах — отсутствует;
- вкус — соленый;
- плотность — 2,165 г/ см3 (20 °C);
- температура плавления — 801 °C;
- точка кипения — 1413 °C;
- растворимость в воде — 359 г/л (25 °C);
Получение хлорида натрия в лаборатории
При взаимодействии металлического натрия с газообразным хлором в пробирке образуется вещество белого цвета — хлорид натрия NaCl (формула поваренной соли).
Химия дает представление о различных способах получения одного и того же соединения. Вот некоторые примеры:
Реакция нейтрализации: NaOH (водн.) + HCl = NaCl + H2O.
Окислительно-восстановительная реакция между металлом и кислотой:
2Na + 2HCl = 2NaCl + Н2.
Действие кислоты на оксид металла: Na2O + 2HCl (водн.) = 2NaCl + H2O
Вытеснение слабой кислоты из раствора ее соли более сильной:
Na2CO3 + 2HCl (водн.) = 2NaCl + H2O + CO2 (газ).
Для применения в промышленных масштабах все эти методы слишком дорогие и сложные.
Производство поваренной соли
Еще на заре цивилизации люди знали, что после засолки мясо и рыба сохраняются дольше. Прозрачные, правильной формы кристаллы галита использовались в некоторых древних странах вместо денег и были на вес золота. Поиск и разработка месторождений галита позволили удовлетворить растущие потребности населения и промышленности. Важнейшие природные источники поваренной соли:
- залежи минерала галита в разных странах;
- вода морей, океанов и соленых озер;
- прослойки и корки каменной соли на берегах соленых водоемов;
- кристаллы галита на стенках вулканических кратеров;
- солончаки.
В промышленности используются четыре основных способа получения поваренной соли:
- выщелачивание галита из подземного слоя, испарение полученного рассола;
- добыча в соляных шахтах;
- выпаривание морской воды или рассола соленых озер (77% от массы сухого остатка приходится на хлорид натрия);
- использование побочного продукта опреснения соленых вод.
Химические свойства хлорида натрия
По своему составу NaCl — это средняя соль, образованная щелочью и растворимой кислотой. Хлорид натрия — сильный электролит. Притяжение между ионами настолько велико, что его могут разрушить только сильно полярные растворители. В воде ионная кристаллическая решетка вещества распадается, освобождаются катионы и анионы (Na+, Cl—). Их присутствием обусловлена электропроводность, которой обладает раствор поваренной соли. Формула в этом случае записывается так же, как для сухого вещества — NaCl. Одна из качественных реакций на катион натрия — окрашивание в желтый цвет пламени горелки. Для получения результата опыта нужно набрать на чистую проволочную петлю немного твердой соли и внести в среднюю часть пламени. Свойства поваренной соли также связаны с особенностью аниона, которая заключается в качественной реакции на хлорид-ион. При взаимодействии с нитратом серебра в растворе выпадает белый осадок хлорида серебра (фото). Хлороводород вытесняется из соли более сильными кислотами, чем соляная: 2NaCl + H2SO4 = Na2SO4 + 2HCl. При обычных условиях хлорид натрия не подвергается гидролизу.
Сферы применения каменной соли
Хлорид натрия снижает температуру плавления льда, поэтому зимой на дорогах и тротуарах используется смесь соли с песком. Она впитывает в себя большое количество примесей, при таянии загрязняет реки и ручьи. Дорожная соль также ускоряет процесс коррозии автомобильных кузовов, повреждает деревья, посаженные рядом с дорогами. В химической промышленности хлорид натрия используется как сырье для получения большой группы химических веществ:
- соляной кислоты;
- металлического натрия;
- газообразного хлора;
- каустической соды и других соединений.
Кроме того, поваренная соль применяется в производстве мыла, красителей. Как пищевой антисептик используется при консервировании, засолке грибов, рыбы и овощей. Для борьбы с нарушениями работы щитовидной железы у населения формула соли поваренной обогащается за счет добавления безопасных соединений йода, например, KIO3, KI, NaI. Такие добавки поддерживают выработку гормона щитовидной железы, предотвращают заболевание эндемическим зобом.
Значение хлорида натрия для организма человека
Формула соли поваренной, ее состав приобрел жизненно важное значение для здоровья человека. Ионы натрия участвуют в передаче нервных импульсов. Анионы хлора необходимы для выработки соляной кислоты в желудке. Но слишком большое содержание поваренной соли в пище может приводить к высокому кровяному давлению и повышению риска развития заболеваний сердца и сосудов. В медицине при большой кровопотере пациентам вводят физиологический солевой раствор. Для его получения в одном литре дистиллированной воды растворяют 9 г хлорида натрия. Человеческий организм нуждается в непрерывном поступлении этого вещества с пищей. Выводится соль через органы выделения и кожу. Среднее содержание хлорида натрия в теле человека составляет примерно 200 г. Европейцы потребляют в день около 2-6 г поваренной соли, в жарких странах эта цифра выше в связи с более высоким потоотделением.
- Хлори́д на́трия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту под названием поваренной соли, основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде, придавая ей солёный вкус. Встречается в природе в виде минерала галита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Источник: Википедия
Связанные понятия
Соля́ная кислота́ (также хлороводоро́дная, хлористоводоро́дная кислота) — раствор хлороводорода (HCl) в воде, сильная одноосновная кислота. Бесцветная, прозрачная, едкая жидкость, «дымящаяся» на воздухе (техническая соляная кислота — желтоватого цвета из-за примесей железа, хлора и пр.). В концентрации около 0,5 % присутствует в желудке человека. Соли соляной кислоты называются хлоридами.
Аммоний — полиатомный катион с химической формулой NH4+. Аммоний с анионами образует соли аммония, аммониевые соединения, последние входят в большой класс ониевых соединений. Ион аммония NH4+ является правильным тетраэдром с азотом в центре и атомами водорода в вершинах тетраэдра. Размер иона — 1,43 Å.
На́трий (Na, лат. natrium) — химический элемент первой группы, третьего периода периодической системы Менделеева, с атомным номером 11. Как простое вещество представляет собой мягкий щелочной металл серебристо-белого цвета. На внешнем энергетическом уровне натрий имеет один электрон, который он легко отдаёт, превращаясь в положительно заряженный катион Na+. Единственным стабильным изотопом является 23Na. В свободном виде не встречается, но может быть получен из различных соединений. Натрий — шестой…
Хлори́ды — группа химических соединений, соли хлороводородной (соляной) кислоты HCl.
Фтори́ды — химические соединения фтора с другими элементами. Фториды известны для всех элементов, кроме гелия и неона. К фторидам относят как бинарные соединения — ионные фториды (соли фтороводородной кислоты и металлов, ковалентные фториды переходных металлов в высших степенях окисления и фториды неметаллов), так и сложные неорганические соединения (фторангидриды кислот, комплексные фториды, гидрофториды металлов, фторированный графит).
Упоминания в литературе
Очистка соли, как правило, включает в себя и рекристаллизацию: сушку в горячей печи с добавлением специальных химикатов. Природная структура кристаллов соли разрушается. Столовая соль проходит настолько интенсивную очистку, что в ней остаётся от 97 % до 99 % хлорида натрия. То есть содержание других полезных веществ в такой соли не превышает 3 %, в отличие от 14 % в морской соли
Морская соль немного дешевле, при этом ее полезные свойства не вызывают сомнений. Ее получают путем кристаллизации хлорида натрия из морской воды.
Органолептические свойства воды формируют природные и антропогенные факторы. Запах, привкус, окраска и мутность являются важными характеристиками качества питьевой воды. Причины появления запахов, привкуса, цветности и мутности воды весьма разнообразны. Для поверхностных источников это в первую очередь почвенные загрязнения, поступающие с током атмосферных вод. Запах и привкус могут быть связаны с цветением воды и с последующим разложением растительности на дне водоема. Вкус воды определяется ее химическим составом, соотношением отдельных компонентов и количеством этих компонентов в абсолютных величинах. Это особенно относится к высокоминерализованным подземным водам в силу повышенного содержания в них хлоридов, сульфатов натрия, реже – кальция и магния. Так, хлорид натрия обуславливает соленый вкус воды, кальций – вяжущий, а магний – горьковатый. Вкус воды определяется и газовым составом: 1/3 всего газового состава составляет кислород, 2/3 – азот. В воде очень небольшое количество углекислого газа, но роль его велика. Углекислота может быть представлена в воде в различных формах:
Процесс седиментации дисперсной фазы может быть проведён добавлением к водному извлечению чаги специально подобранных электролитов из числа нейтральных солей [64]. Авторами проведено исследование агрегативной устойчивости коллоидной системы водного извлечения чаги с содержанием сухих веществ 1,2 % растворами солевых электролитов различной концентрации. При применении максимальной концентрации раствора хлористого натрия (32 %) в осадок выпадало только 44,1 % меланина, что может свидетельствовать об относительно высокой устойчивости дисперсной фазы водного извлечения чаги к нейтральным солям одновалентных катионов. При добавлении 8 % раствора хлористого кальция из водной вытяжки чаги осаждалось почти в 2 раза больше меланина, чем при добавлении насыщенного раствора хлорида натрия. Применение в качестве осаждающего агента раствора алюмокалиевых квасцов в той же концентрации (8 %) вызывало почти полное осаждении меланина (98,72 %). Растворы уксуснокислого свинца даже в незначительной концентрации (2 %) осаждали меланин полностью (98,90 %).
• Соль – белые кристаллы хлорида натрия. Ее добывают, используя естественное испарение морской воды (морская соль), а также путем разработки соляных шахт (каменная соль) и выпаривания соляного рассола, полученного из каменной соли. Соль бывает крупного и мелкого помола, делится по сортам в зависимости от количества примесей других минеральных солей, которые могут придавать ей различный оттенок от серо-желтоватого до розового (так называемая гималайская соль). Во многом обеспечивает нормальное функционирование организма человека и животных, способствуя образованию соляной кислоты (основы желудочного сока). Суточная потребность в соли – 10–15 г. Соль не просто придает пище соленый вкус, но влияет на консистенцию различных блюд. Даже тесто для самого обычного хлеба или для пельменей не получится нужной плотности, если забыть добавить соли. Соль также является простейшим консервантом для мяса, рыбы, овощей.
Связанные понятия (продолжение)
Гидра́ты (от др.-греч. ὕδωρ «вода») — продукты присоединения воды к неорганическим и органическим веществам.
Со́ли — сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды.
Кремниевые кислоты — очень слабые, малорастворимые в воде кислоты общей формулы nSiO2•mH2O.
Ио́д (тривиальное (общеупотребительное) название — йод; от греч. ἰώδης — «фиалковый (фиолетовый)») — химический элемент с атомным номером 53. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в пятом периоде таблицы. Атомная масса элемента 126,90447 а. е. м.. Обозначается символом I (от лат. Iodum). Химически активный неметалл, относится к группе галогенов…
Хлорид аммония (хлористый аммоний; техническое название — нашаты́рь; NH4Cl) — соль аммония, белый кристаллический слегка гигроскопичный порошок без запаха.
Хлорид лития — химическое соединение щелочного металла лития и хлора с формулой LiCl.
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов.
Иоди́д ка́лия (иодистый калий) — неорганическое соединение, калиевая соль иодоводородной кислоты с химической формулой KI. Бесцветная кристаллическая соль, желтеющая на свету. Широко используется в качестве источника иодид-ионов. Менее гигроскопична чем иодид натрия. Применяется в медицине как лекарственное средство, в сельском хозяйстве как удобрение, а также в фотографии и аналитической химии.
Гидрокси́ды (гидроо́киси, водокиси) — неорганические соединения, содержащие в составе гидроксильную группу -OH. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов. Гидроксиды щелочных и щёлочноземельных металлов, а также аммония являются растворимыми и называются щелочами.
Иодиды — бинарные соединения иода с менее электроотрицательными элементами. Иодиды металлов могут рассматриваться как соли иодоводородной кислоты HI.
Ортофо́сфорная кислота́ (фо́сфорная кислота́) — неорганическая кислота средней силы с химической формулой H3PO4, которая при стандартных условиях представляет собой бесцветные гигроскопичные кристаллы. Обычно ортофосфорной (или просто фосфорной) кислотой называют 85 %-ый водный раствор (бесцветная сиропообразная жидкость без запаха). Растворима в этаноле и других растворителях.
Бром (от др.-греч. βρῶμος — «вонючка», «вонючий») — химический элемент с атомным номером 35. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в четвёртом периоде таблицы. Атомная масса элемента 79,901…79,907 а. е. м. . Обозначается символом Br (от лат. Bromum). Химически активный неметалл, относится к группе галогенов. Простое вещество бром при нормальных…
Фторид кальция — неорганическое бинарное ионное химическое соединение. Химическая формула CaF2.
Мышьяковая кислота — (ортомышьяковая кислота) H3AsO4, трехосновная кислота средней силы. Легко растворима в воде, из растворов кристаллизуется в виде кристаллогидрата H3AsO4·0,5Н2O. Предполагается существование метамышьяковой (HAsO3) и пиромышьяковой (H4As2O7) кислот. Кислота и все ее соли ядовиты.
Хлори́д ка́лия — химическое соединение, формула KCl, калиевая соль соляной кислоты.
Хлорная кислота HClO4 — одноосновная кислота, одна из самых сильных (в водном растворе, pK ≈ −10), безводная — исключительно сильный окислитель, так как содержит хлор в высшей степени окисления +7.
Гигроскопи́чность (от др.-греч. ὑγρός «влажный» + σκοπέω «наблюдаю») — способность некоторых веществ поглощать водяные пары из воздуха.
Селе́нистая кислота́ — неорганическое химическое соединение селена, кислота. Химическая формула H2SeO3.
Бромноватая кислота — неорганическое соединение, одноосновная кислота с формулой HBrO3, в свободном состоянии не выделена, существует в растворе — бесцветная (или слегка желтоватая) жидкость с максимальной концентрацией до 50%, сильная кислота.
Неорганические сульфиды (от лат. sulphur — сера) — класс химических соединений, представляющих собой соединения металлов (а также ряда неметаллов В, Si, Р, As) с серой (S), где она имеет степень окисления −2. Могут рассматриваться как соли сероводородной кислоты H2S. Свойства сульфидов сильно зависят от металлов, входящих в их состав.
Фтор (F, лат. fluorum) — химический элемент 17-й группы, второго периода периодической системы (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA) с атомным номером 9. Самый химически активный неметалл и сильнейший окислитель, самый лёгкий элемент из группы галогенов. Как простое вещество при нормальных условиях фтор представляет собой двухатомный газ (формула F2) бледно-жёлтого цвета с резким запахом, напоминающим озон или хлор. Токсичен…
Вольфрамовая кислота — моногидрат триоксида вольфрама — WO3·H2O, вопреки часто распространенному мнению формула H2WO4 не отвечает действительной структуре соединения. Впервые кислота была получена Карлом Вильгельмом Шееле в 1781 году.
Щелочны́е мета́ллы — элементы 1-й группы периодической таблицы химических элементов (по устаревшей классификации — элементы главной подгруппы I группы): литий Li, натрий Na, калий K, рубидий Rb, цезий Cs, франций Fr, унуненний Uue. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щелочами.
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным.
Щёлочноземе́льные мета́ллы — химические элементы 2-й группы периодической таблицы элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba), радий (Ra), унбинилий (Ubn).
Хлор (от греч. χλωρός — «жёлто-зелёный») — химический элемент с атомным номером 17. Принадлежит к 17-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе VII группы, или к группе VIIA), находится в третьем периоде таблицы. Атомная масса элемента 35,446…35,457 а. е. м. . Обозначается символом Cl (от лат. Chlorum). Химически активный неметалл. Входит в группу галогенов.
Ка́лий — элемент первой группы (по старой классификации — главной подгруппы первой группы), четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий — мягкий щелочной металл серебристо-белого цвета.
Хромовая кислота — кристаллическое вещество красного цвета. Окрашивает раствор в жёлтый цвет. Выделена в свободном состоянии при охлаждении насыщенных водных растворов хромата. Химическая формула H2CrO4. Соли хромовой кислоты называются хроматами. Токсична, канцерогенна.
Марганцо́вая кислота́ — сильная, нестабильная, неорганическая кислота фиолетово-красного цвета с химической формулой HMnO4. В чистом виде не выделена, существует в виде раствора. Соли марганцовой кислоты называются перманганаты. Анион MnO4- окрашивает соли в малиново-фиолетовый цвет. Самым известным производным марганцовой кислоты является перманганат калия (марганцовка).
Раствори́мость — способность вещества образовывать с другими веществами однородные системы — растворы, в которых вещество находится в виде отдельных атомов, ионов, молекул или частиц. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе либо в процентах, либо в весовых или объёмных единицах, отнесённых к 100 г или 100 см³ (мл) растворителя (г/100 г или см³/100 см³). Растворимость газов в жидкости зависит от температуры и давления. Растворимость жидких и твёрдых…
Хроматы — соли хромовой кислоты H2CrO4. Устойчивы в нейтральной и щелочной среде, в кислой среде обратимо переходят в дихроматы — соли дихромовой кислоты H2Cr2O7.
Хлори́д ба́рия (хлористый барий) — бинарное неорганическое вещество, относящееся к классу солей. Химическая формула — BaCl2.
Гидроксид цезия (CsOH) — химическое соединение, содержащее атом цезия и гидроксильную группу.
Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). При обычных условиях концентрированная серная кислота — тяжёлая маслянистая жидкость без цвета и запаха, с сильнокислым «медным» вкусом. В технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Если молярное отношение SO3 : H2O 1 — раствор SO3 в серной кислоте (олеум).
Стандартные условия для температуры и давления — значения температуры и давления, с которыми соотносятся значения других физических величин, зависящих от давления и температуры. Принятые в разных дисциплинах и разных организациях точные значения давления и температуры в стандартных условиях могут различаться, поэтому указание значений физических величин (например, молярного объёма газа, электродного потенциала, скорости звука и так далее) без уточнения условий, в которых они приводятся, может приводить…
Сероводоро́д (серни́стый водоро́д, сульфи́д водоро́да, дигидросульфи́д) — бесцветный газ со сладковатым вкусом, обеспечивающий характерный неприятный тяжёлый запах тухлых яиц (тухлого мяса). Бинарное химическое соединение водорода и серы. Химическая формула — H2S. Плохо растворим в воде, хорошо — в этаноле. В больших концентрациях ядовит. Огнеопасен. Концентрационные пределы воспламенения в смеси с воздухом составляют 4,5—45 % сероводорода. Используется в химической промышленности для синтеза некоторых…
Иодная кислота HIO4 (гексаоксоиодат (VII) водорода, периодат Н5IO6)— слабая кислота, гигроскопичное кристаллическое вещество.
Сульфа́ты — минералы, соли серной кислоты H2SO4. В их кристаллической структуре обособляются комплексные анионы SO42−. Наиболее характерны труднорастворимые сульфаты сильных двухвалентных оснований, особенно Ba2+, а также Sr2+ и Ca2+. Более слабые основания образуют основные соли, часто весьма неустойчивые (например сульфаты окисленного железа), более сильные основания — двойные соли и кристаллогидраты, а они в свою очередь образовывают купоросы.
Гидрокси́д ба́рия (е́дкий бари́т) — неорганическое соединение, проявляющее сильные основные свойства. Химическая формула — Ba(OH)2. Насыщенный водный раствор гидроксида бария называется баритовой водой.
Сульфа́т ка́льция (CaSO4) — неорганическое соединение, кальциевая соль серной кислоты.
Бор (B, лат. borum) — химический элемент 13-й группы, второго периода периодической системы (по устаревшей короткой форме периодической системы принадлежит к главной подгруппе III группы, или к группе IIIA) с атомным номером 5. Бесцветное, серое или красное кристаллическое либо тёмное аморфное вещество. Известно более 10 аллотропных модификаций бора, образование и взаимные переходы которых определяются температурой, при которой бор был получен.
Се́ра — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 16. Проявляет неметаллические свойства. Обозначается символом S (лат. sulfur). В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
Щёлочи (в русском языке происходит от слова «щёлок», возможно, производное от того же корня, что и др.-исл. «skola» — «стирать») — гидроксиды щелочных, щёлочноземельных металлов и некоторых других элементов, например, таллия. К щелочам относятся хорошо растворимые в воде основания. При диссоциации щёлочи образуют анионы OH− и катион металла.
Тиосульфа́т на́трия (антихлор, гипосульфит, сульфидотриоксосульфат натрия, натрий серноватистокислый) — Na2S2O3 или Na2SO3S, соль натрия и тиосерной кислоты, образует кристаллогидрат Na2S2O3·5H2O.
Оксид бария — соединение бария с кислородом, имеющее химическую формулу BaO. Является основным оксидом. При стандартных условиях представляет собой бесцветные кристаллы с кубической решёткой.
Упоминания в литературе (продолжение)
Иным был и состав океана. Поскольку основным источником главного морского аниона – Cl– – является глубинная дегазация Земли, а поглощается этот анион в результате геохимических преобразований океанической коры, то за последние 4 млрд лет его среднее содержание не очень сильно менялось. А вот соотношение катионов, преобладающих в морской воде, не могло не измениться: пока не появились кислородная атмосфера и достаточно большая фельзитовая суша, благодаря выветриванию которой усилился сток щелочных (Na+, К+) и некоторых щелочноземельных катионов (Mg2+), обильным и достаточно активным в водной среде был Са2+. Важнейший источник этого катиона – гидротермальная активность, связанная с высокотемпературными преобразованиями океанической коры, – уже существовал. И архейский океан, вероятно, представлял собой не концентрированный раствор хлорида натрия, как сейчас, а раствор хлорида кальция (СаCl2). Модель такого океана доступна (почти доступна): озеро Дон-Жуан в антарктической долине Райта, на дне которого формируется минерал антарктицит (СаCl2 × 6Н2О), а в гиперсоленой (44?) воде обитают цианобактерии и некоторые одноклеточные эукариоты.
Натрий (Na). Калий и натрий были открыты вместе и оба важны для нормального роста и состояния организма. Они являются антагонистами, т. е. повышение содержания натрия приводит к уменьшению калия. Нормы суточного потребления не существует, однако считается, что потребность взрослого человека составляет около 500 мг хлорида натрия (поваренной соли) в сутки. Натрий в первую очередь нужен для нормального функционирования нервно-мышечной системы. При дефиците натрия происходит нарушение усвоения углеводов, возможны невралгии, отчасти понижение давления.
Соль, добываемая из Мертвого моря, отличается от других видов соли тем, что хлорид натрия здесь присутствует вместе с соединениями калия и магния. Это делает соль Мертвого моря незаменимой в диетическом питании гипертоников.
Яйца содержат много белка, а также микроэлементы, необходимые для здоровья, среди них йод, кобальт, медь, в небольшом количестве хлорид натрия и пуриновые вещества.
Океан является огромной кладовой воды и многих химических веществ. В каждой кубической миле морской воды содержится 1,5–1011 кг растворенных твердых веществ. Океан столь огромен, что если концентрация какого-либо вещества в морской воде составляет всего одну миллиардную долю по весу, то его содержание в мировом океане исчисляется в 5–109 кг. Тем не менее, океан еще мало используется как источник сырьевых ресурсов, поскольку стоимость извлечения необходимых веществ из воды слишком высока. Лишь три вещества получают из морской воды в промышленно широких масштабах: хлорид натрия, бром и магний.
Яйца содержат микроэлементы, необходимые для здоровья, среди них йод, кобальт, медь, в небольшом количестве хлорид натрия и пуриновые вещества.
Приступая к промышленному получению препарата, культуру гриба выращивают в инокуляторе на ИПС. Среда состоит из кормовых дрожжей – 2 %, крахмала – 1 %, хлорида натрия – 0,2 %, хлорида марганца – 0,01 % и хлорида кальция – 0,05 %, который усиливает устойчивость конидиоспор к неблагоприятным факторам.
2. Изотоничность. Бактерии должны содержать набор солей для поддержания осмотического давления, определенную концентрацию хлорида натрия.
Местное лечение – полоскание зева и орошение глотки. Для полоскания используют растворы натрия бикарбоната (соды), натрия хлорида, фурацилина 1:5000, настои и отвары ромашки, шалфея, эвкалипта. Внутрь применяют антибиотики широкого спектра действия, сульфаниламидные препараты, салицилаты. При тяжелых формах ангины антибиотики назначаются в уколах. Показано применение противоаллергических средств, аскорбиновой кислоты.
Состав
Действующее составляющее этого средства — натрия хлорид. Формула хлорида натрия – NaCl, это кристаллы белого цвета, которые быстро растворяются в воде. Молярная масса 58.44 г/моль. Код ОКПД — 14.40.1.
Физиологический раствор (изотонический) – это раствор 0,9%, в нем содержится 9 г натрия хлорида, до 1 л дистиллированной воды.
Гипертонический раствор хлорида натрия – это раствор 10%, в нем содержится 100 г хлорида натрия, до 1 л дистиллированной воды.
Форма выпуска
Производится раствор натрия хлорида 0,9%, который может содержаться в ампулах по 5 мл, 10 мл, 20 мл. Ампулы применяются с целью растворения лекарств для введения инъекции.
Также производится раствор натрия хлорида 0,9% во флаконах емкостью по 100, 200, 400 и 1000 мл. Их применение в медицине практикуется для применения наружно, проведения капельных вливаний внутривенно, проведения клизм.
Раствор натрия хлорида 10% содержится во флаконах емкостью 200 и 400 мл.
С целью перорального применения выпускаются таблетки по 0,9 г .
Производится также назальный спрей во флаконах по 10 мл.
Фармакологическое действие
Хлорид натрия – это препарат, который действует как регидратирующее и дезинтоксикационное средство. Лекарство способно восполнять в организме недостаток натрия при условии развития разнообразных патологий. Хлорид натрия также увеличивает количество жидкости, которая циркулирует в сосудах.
Такие свойства у раствора проявляются благодаря наличию в нем хлорид-ионов и ионов натрия. Они способны проникать сквозь мембрану клеток с помощью разных транспортных механизмов, в частности натрий-калиевого насоса. Важную роль натрий играет в процессе передачи сигналов в нейронах, также он задействован в процессе метаболизма в почках и в электрофизиологических процессах сердца человека.
Фармакопея свидетельствует, что хлорид натрия поддерживает во внеклеточной жидкости и плазме крови постоянное давление. При нормальном состоянии организма достаточное количество этого соединения попадает в организм с продуктами питания. Но при патологических состояниях, в частности, при рвоте, поносе, серьезных ожогах отмечается повышенное выделение из организма этих элементов. Как следствие, организм испытывает дефицит ионов хлора и натрия, вследствие чего кровь становится гуще, нарушаются функции нервной системы, кровоток, судороги, спазмы гладкой мускулатуры мышц.
Если в кровь своевременно вводится изотонический раствор натрия хлорида, применение его способствует восстановлению водно-солевого баланса. Но так как осмотическое давление раствора аналогичное давлению плазмы крови, в сосудистом русле надолго он не задерживается. После введения он быстро выводится из организма. Как следствие, через 1 час в сосудах задерживается не больше половины введенного количество раствора. Поэтому в случае кровопотери раствор не является достаточно эффективным.
Средство также имеет плазмозамещающие, дезинтоксикационные свойства.
При введении внутривенно гипертонического раствора отмечается усиление диуреза, восполнение дефицита хлора и натрия в организме.
Фармакокинетика и фармакодинамика
Выведение из организма происходит в основном через почки. Немного натрия выделяется с потом и с калом.
Показания к применению
Натрия хлорид — это физраствор, который применяется в случае потери организмом внеклеточной жидкости. Показан при состояниях, которые ведут к ограничению поступления жидкости:
- диспепсия при отравлении;
- рвота, диарея;
- холера;
- обширные ожоги;
- гипонатриемия или гипохлоремия, при которых отмечается обезвоживание организма.
Учитывая, что такое натрий хлорид, его применяют наружно с целью промывания ран, глаз, носа. Препарат применяется с целью увлажнения перевязок, для ингаляций, для лица.
Показано использование NaCl для проведения форсированного диуреза при запоре, отравлениях, при внутренних кровотечениях (легочных, кишечных, желудочных).
Обозначено также в показаниях к применению хлорид натрия, что это такое средство, которое применяется для разведения и растворения лекарств, которые вводятся парентерально.
Противопоказания
Противопоказано применение раствора при таких болезнях и состояниях:
- гипокалиемия, гиперхлоремия, гипернатриемия;
- внеклеточная гипергидратация, ацидоз;
- отек легких, отек мозга;
- острая левожелудочковая недостаточность;
- развитие циркуляторных нарушений, при которых существует угроза отека мозга и легких;
- назначение больших доз ГКС.
Осторожно раствор назначают людям, которые болеют артериальной гипертензией, периферическими отеками, декомпенсированной хронической сердечной недостаточностью, почечной недостаточностью в хронической форме, преэклампсией, а также тем, у кого диагностированы другие состояния, при которых происходит задержка натрия в организме.
Если раствор применяется в качестве растворяющего средства для других лекарств, следует учесть существующие противопоказания.
Побочные действия
При применении хлорида натрия могут развиться следующие состояния:
- гипергидратация;
- гипокалиемия;
- ацидоз.
Если препарат применяется правильно, то маловероятно развитие побочных эффектов.
Если раствор NaCl 0.9% применяется как базовый растворитель, то побочные явления определяются свойствами лекарств, которые разводятся раствором.
При проявлении любых негативных эффектов нужно сразу сообщить об этом специалисту.
Инструкция по применению Натрия Хлорида (Способ и дозировка)
Инструкция на физ раствор (изотонический раствор) предусматривает его введение внутривенно и подкожно.
В большинстве случаев практикуется внутривенное капельное введение, для чего капельница Хлорида Натрия прогревается до температуры 36-38 градусов. Объем, который вводят пациенту, зависит от того, в каком состоянии пациент, а также от того количества жидкости, которая была потеряна организмом. При этом важно учесть возраст человека и его вес.
Средняя суточная доза препарата — 500 мл, вводится раствор со средней скоростью 540 мл/ч. Если отмечается сильная степень интоксикации, то максимальный объем лекарства в сутки может составлять 3000 мл. Если существует такая необходимость, можно вводить объем 500 мл на скорости 70 капель в минуту.
Детям вводится доза от 20 до 100 мл в сутки на 1 кг веса. Дозировка зависит от массы тела, от возраста ребенка. Следует учитывать, что при продолжительном применении этого лекарства необходимо обязательно контролировать уровень электролитов в плазме и моче.
Чтобы развести препараты, которые нужно вводить капельно, применяется от 50 до 250 мл натрия хлорида на одну дозу лекарства. Определение особенностей введения проводится по основному лекарству.
Введение гипертонического раствора проводится внутривенно струйно.
Если раствор применяется с целью немедленного восполнения дефицита ионов натрия и хлора, вводится капельно 100 мл раствора.
Чтобы провести ректальную клизму для вызывания дефекации, вводят 100 мл 5% раствора, также можно ввести на протяжении суток 3000 мл изотонического раствора.
Применение гипертонической клизмы медленно показано при почечных и сердечных отеках, повышенном внутричерепном давлении и при гипертонии проводится медленно, вводится 10-30 мл. Нельзя проводить такую клизму при эрозии толстой кишки и воспалительных процессах.
Гнойные раны раствором проводят согласно с той схемой, которую назначает врач. Компрессы с NaCl прикладывают непосредственно к ране или другому поражению на коже. Такой компресс способствует отделению гноя, гибели патогенных микроорганизмов.
Назальный спрей закапывают в полость носа после ее очищения. Взрослым пациентам закапывают по две капли в каждую ноздрю, детям – по 1 капле. Применяется как для лечения, так и для профилактики, для чего капают раствор на протяжении примерно 20 дней.
Натрия хлорид для ингаляций применяется при простудных заболеваниях. Для этого раствор смешивают с бронхолитическими препаратами. Ингаляция проводится на протяжении десяти минут трижды в день.
При крайней необходимости физраствор можно приготовить в домашних условиях. Для этого полную чайную ложку поваренной соли нужно размешать в одном литре кипяченной воды. При необходимости приготовить определенного количество раствора, например, с солью массой 50 г, следует провести соответствующие измерения. Такой раствор можно применять местно, использовать для клизм, полосканий, ингаляций. Однако ни в коем случае нельзя такой раствор вводить внутривенно или использовать для обработки открытых ран или глаз.
Передозировка
При передозировке пациент может чувствовать тошноту, страдать от рвоты и диареи, у него могут развиваться боли в животе, лихорадка, учащенное сердцебиение. Также при передозировке могут повышаться показатели артериального давления, развиваться отек легких и периферические отеки, почечная недостаточность, судороги мышц, слабость, головокружение, генерализованные судороги, кома. При чрезмерном введении раствора может развиться гипернатриемия.
При чрезмерном поступлении в организм может развиться гиперхлоримический ацидоз.
Если натрия хлорид применяется для растворения лекарств, то в основном передозировка связана со свойствами тех препаратов, которые подвергаются разведению.
При непреднамеренном избыточном введении NaCl важно прекратить этот процесс и оценить, есть ли негативнее симптомы у пациента. Практикуется симптоматическое лечение.
Взаимодействие
NaCl совмещается с большинством лекарств. Именно это его свойство обуславливает применение раствора для разведения и растворения ряда препаратов.
При разведении и растворении нужно обязательно контролировать совместимость препаратов визуально, определяя, не появляется ли в процессе осадок, не меняется ли цвет и др.
Плохо совмещается с норадреналином.
При одновременном назначении препарата с кортикостероидами важно постоянно отслеживать содержание электролитов в крови.
При параллельном приеме понижается гипотензивное действие Эналаприла и Спираприла.
Несовместим Натрия Хлорид со стимулятором лейкопоэза Филграстимом, а также с полипептидным антибиотиком Полимиксин В.
Есть данные о том, что изотонический раствор увеличивает биодоступность лекарств.
При разведении раствором порошкообразных антибиотиков они усваиваются организмом полностью.
Условия продажи
В аптеках продается по рецепту. При необходимости применения препарата для разбавления других лекарств и т.п. выписывают рецепт на латинском языке.
Условия хранения
Хранить порошок, таблетки и раствор нужно в сухом месте, в хорошо закупоренной таре, при этом температура должна составлять не более 25 градусов Цельсия. Важно беречь препарат от доступа детей. Если упаковка герметична, то замораживание не влияет на свойства препарата.
Срок годности
Для хранения порошка и таблеток ограничений нет. Раствор в ампулах 0,9% может храниться на протяжении 5 лет; раствор во флаконах 0,9% – один год, раствор во флаконах 10%– 2 года. Нельзя использовать после того, как срок хранения завершился.
Особые указания
Если проводится инфузия, нужно тщательно следить за состоянием пациента, в частности, за электролитами плазмы крови. Следует учитывать, что у детей ввиду незрелости функции почек возможно замедление экскреции натрия. Важно определить его концентрацию в плазме перед проведением повторных инфузий.
Важно контролировать состояние раствора перед его введением. Раствор должен быть прозрачным, упаковка – неповрежденной. Применять раствор для внутривенного введения может только квалифицированный специалист.
Растворять любые препараты Натрием Хлорида должен только специалист, который может квалифицированно оценить, является ли полученный раствор пригодным для введения. Важно строго выдерживать все правила антисептики. Введение любого раствора нужно проводить сразу же после его приготовления.
Итогом ряда химических реакций с участием натрия хлорида является образование хлора. Электролиз расплава Хлорида Натрия в промышленности – способ получения хлора. Если провели электролиз раствора Хлорида Натрия, также в итоге получают хлор. Если на кристаллический Хлорид Натрия подействовали серной кислотой концентрированной, в итоге получают хлороводород. Сульфат натрия и гидроксид натрия можно получить путем цепочки химических реакций. Качественная реакция на хлорид ион – реакция с нитратом серебра.
Аналоги
Совпадения по коду АТХ 4-го уровня:
У разных производителей лекарственных средств раствор может выпускаться под отдельным названием. Это препараты Натрия хлорид Браун, Натрия хлорид Буфус, Ризосин, Салин Натрия хлорид Синко и др.
Также производятся препараты, вмещающие в составе хлорид натрия. Это комбинированные солевые растворы натрия ацетат + натрия хлорид и др.
Детям
Применяется согласно с инструкцией и под тщательным контролем специалистов. Следует учитывать незрелость функции почек у детей, поэтому повторное введение проводится только после точного определения уровня натрия в плазме.
При беременности и лактации
При беременности капельница с хлоридом натрия может применяться только при патологических состояниях. Это токсикоз в средней или тяжелой стадии, а также гестоз. Здоровые женщины получают натрий хлорид с пищей, причем, его избыток может привести к развитию отеков.
Отзывы
Большинство отзывов – положительные, так как пользователи пишут об этом средстве, как о полезном препарате. Особенно много отзывов о назальном спрее, который, по мнению пациентов, является неплохим средством как для профилактики, так и для лечения насморка. Средство эффективно увлажняет слизистую носа и способствует выздоровлению.
Цена Натрия Хлорида, где купить
Цена физ раствора в ампулах по 5 мл составляет в среднем 30 рублей за 10 шт. Купить натрия хлорид 0,9% во флаконе 200 мл составляет в среднем 30-40 рублей за 1 флакон.
- Интернет-аптеки РоссииРоссия
- Интернет-аптеки УкраиныУкраина
- Интернет-аптеки КазахстанаКазахстан
ЗдравСити
-
Натрия хлорид р-ль д/приг. лек. форм. д/ин. 0,9% амп 5мл №10ОАО Дальхимфарм
-
Натрия хлорид Браун р-р д/инф 0,9% 100мл бут п/эт №20B.Braun Melsungen AG
-
Натрия хлорид р-р д/инф. 0.9% 250мл №10Гематек ООО
-
Ардуан лиоф д/приг. р-ра для в/в введ. 4мг фл.10мг №25+ растворитель( натрия хлорид 0,9%) 2мл 25шт.ОАО Гедеон Рихтер
-
Натрия хлорид буфус раствор для ин. 0,9% 5мл 10 шт.АО Обновление ПФК
Аптека Диалог
-
Натрия хлорид — СОЛОфарм (0,9% 200 мл)Гротекс ООО
-
Натрия хлорид — СОЛОфарм (р-р д.инф.0,9% 400мл Домус)Гротекс ООО
-
Натрия хлорид буфус (амп. 0,9% 5мл №10)Обновление ПФК ЗАО
-
Натрия хлорид буфус (амп. 0,9% 10мл №10)Обновление ПФК ЗАО
-
Натрия хлорид (амп. 0,9% 10мл №10)Гротекс ООО
показать еще
Аптека24
-
Натрия хлорид 0.9% 250мл (ПВХ) раствор для инфузий ДП»Фарматрейд»,Україна
-
Натрия хлорид 0.9% 400 мл раствор пакет
-
Натрия хлорид-Дарница 9 мг/мл 200 мл раствор ПрАТ»Фармацевтична фірма «Дарниця», Україна
-
Натрия хлорид 0.9% 3000 мл раствор ДП»Фарматрейд»,Україна
-
Натрия хлорид 0.9% 100 мл ПрАТ»Інфузія», Україна
ПаниАптека
-
Натрия хлорид ампула Натрия хлорид р-р д/ин. 0.9% амп. 5мл №10 Украина , Дарница ЧАО
-
Натрия хлорид инфузия Натрия хлорид р-р инф. 0.9% 100мл Украина , Юрия-Фарм ООО
-
Натрия хлорид инфузия Натрия хлорид р-р инф. 0.9% 200мл Украина , Юрия-Фарм ООО
-
Натрия хлорид инфузия Натрия хлорид р-р 0.9% 200мл пласт.уп. Украина , Фарматрейд ДП
-
Натрия хлорид инфузия Натрия хлорид р-р 0.9% 500мл Украина , Фарматрейд ДП
показать еще
БИОСФЕРА
-
Натрия хлорид 0,9%/10 мл №10 р-р д/ин.амп.Новосибхимфарм ОАО (Россия)
-
Натрия хлорид 0,9% 200 мл р-р д/инф.фл.Келун-Казфарм ТОО (Казахстан)
-
Натрия хлорид 0,9% 500 мл р-р д/инф.фл.Хуашидан АК (Китай)
-
Натрия хлорид 0,9% 400 мл р-р д/инф.Биосинтез (Россия)
-
Натрия хлорид-Дарница 0,9%/5 мл №10 р-р д/ин.амп.Дарница (Украина)
показать еще
Окраска раствора должна измениться от прибавления не более 0,5 мл 0,01 М раствора натрия гидроксида или не более 0,5 мл 0,01 М раствора хлористоводородной кислоты
| Показатели качества | |
| Наименование показателя | Требования ФСП |
| 1. Описание | Белый кристаллический порошок или крупинки, или бесцветные кристаллы |
| 2. Растворимость | Легко растворим в воде, мало растворим в спирте 96% |
| 3. Подлинность | Дает характерные реакции на натрий и хлориды |
| 4. Прозрачность раствора | Должен быть прозрачным |
| 5. Цветность раствора | Должен быть бесцветным |
| 6. Кислотность или щелочность | Окраска раствора должна измениться от прибавления не более 0,5 мл 0,01 М раствора натрия гидроксида или не более 0,5 мл 0,01 М раствора хлористоводородной кислоты |
| Щелочноземельные металлы и магний | Не более 0,01% в пересчете на кальций |
| 8. Барий | Мутность раствора субстанции не должна превышать мутность эталонного раствора |
| 9. Железо, %, не более | 0,0003 |
| 10. Тяжелые металлы, %, не более | 0,0005 |
| 11. Сульфаты, %, не более | 0,005 |
| 12. Калий, %, не более | 0,05 |
| 13. Соли аммония, %, не более | 0,004 |
| 14. Потеря в массе при высушивании, %, не более | 0,5 |
| 15. Мышьяк, %, не более | 0,00005 |
| 16. Фосфаты, %, не более | 0,0025 |
| 17. Бромиды, %, не более | 0,005 |
| 18. Иодиды | Раствор не должен окрашиваться в голубой цвет |
| 19. Ферроцианиды | Раствор не должен окрашиваться в голубой цвет |
| 20. Микробиологическая чистота | Категория 1.2.Б |
| 21. Количественное определение (NaCl), %, в пределах | Не менее 99,5% NaCl в пересчете на сухое вещество |
| 22. Бактериальные эндотоксины, предельное содержание не более | Не более 5 ЕЭ на 1 г субстанции |
| Упаковка | По 1 кг, 3 кг, 5 кг в полипропиленовые пакет из полиэтиленовой пленки, который термосваривают двумя швами, снабжая внутренней этикеткой. Пакеты укладывают в тканый полипропиленовый мешок с внутренним полиэтиленовым пакетом и прошивают вместе с этикеткой. По 25 кг – в тканый полипропиленовый мешок с внутренним полиэтиленовым пакетом Полиэтиленовый пакет термосваривают, полипропиленовый мешок прошивают. Каждая упаковка снабжена этикеткой. Этикетка из этикеточной бумаги, писчей, офсетной. |
| Маркировка | В соответствии с нормативной документацией |
| Хранение | В сухом месте при температуре не выше 250С |
| Срок годности | 5 лет |
Не более 5 ЕЭ на 1 г субстанции
| Общие свойства | |
|---|---|
| Систематическое наименование | Хлорид натрия |
| Традиционные названия | Соль, поваренная соль, столовая соль, пищевая соль, каменная соль, галит |
| Хим. формула | NaCl |
| Физические свойства | |
| Молярная масса | 58,44277 г/моль |
| Плотность | 2,165 г/см³ |
| Термические свойства | |
| Температура плавления | 800,8 °C |
| Температура кипения | 1465 °C |
| Мол. теплоёмк. | 50,8 Дж/(моль·К) |
| Энтальпия образования | −234,8 кДж/моль |
| Удельная теплота испарения | 170,85 кДж/моль |
| Удельная теплота плавления | 28,68 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 35,6 г/100 мл (0 °C) 35,9 г/100 мл (+25 °C) 39,1 г/100 мл (+100 °C) |
| Растворимость в метаноле | 1,49 г/100 мл |
| Растворимость в аммиаке | 21,5 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,544202 (589 нм) |
| Структура | |
| Координационная геометрия | Октаэдральная (Na +) Октаэдральная (Cl -) |
| Кристаллическая структура | гранецентрированная кубическая, cF8 |
| Классификация | |
| Рег. номер CAS | 7647-14-5 |
| PubChem | 5234 |
| Рег. номер EINECS | 231-598-3 |
| SMILES | [Na+].[Cl-] |
| InChI | InChI=1S/ClH.Na/h1H;/q;+1/p-1 FAPWRFPIFSIZLT-UHFFFAOYSA-M |
| RTECS | VZ4725000 |
| ChEBI | 26710 |
| ChemSpider | 5044 |
| Безопасность | |
| ЛД50 | 3000–8000 мг/кг |
| NFPA 704 | |
Наш завод предоставляет гарантию на хранение вещества при должном соответствии требований, предъявляемые при правильной транспортировке и хранении.
Так как хлорид натрия требует к себе особого внимания при транспортировке, то нужно отнестись к его упаковке с особой тщательностью. Вообще, разработаны ГОСТы по его упаковке, и мы конечно, стараемся их соблюдать. Поэтому на нашем химическом заводе готовое вещество упаковываются в прочные полиэтиленовые мешки, которые в свою очередь завязываются двойным узлом нитью (или запаиваются). После этого возможна дополнительная упаковка в в фанерные коробы или в картонные. Или, на выбор покупателя, так же возможна упаковка этого вещества в бумажные пяти-шести-слойные мешки.
Хлорид натрия добывается из естественных природных источников, обычно к ним относятся залежи галита, осадочной горной породы в виде каменной соли ну и конечно же он содержится в огромном количестве в морской воде, из которой ее просто выделяют методом выпаривания
Для приготовления стерильных (инъекционных) лекарственных форм
В фармацевтике изотонический раствор хлорида натрия применяется как средство для дезинтоксикации, а так же в качестве растворителя каких либо других лекарственных средств. А так же при многих других ситуациях — как гипертонический раствор, вспомогательный осмотический диуретик, так же используется для поднятия давления при кровотечениях, при отравлении нитратом серебра, а так же для обработки гнойных ран и при отечностях в качестве наружного средства.
Как видно из описания, данный химический элемент довольно распространен в медицинской области. Но он так же активно применяется чуть ли не повсеместно и в промышленности и быту.

Мы предлагаем выгодные условия оплаты и удобные варианты доставки хлорида калия по России и миру. Один из вариантов — это использование железнодорожных перевозок. На нашем предприятии имеется собственный ЖД тупик, благодаря которому мы можем в точные сроки доставить требуемый объем вещест покупателю.
А так же имеем собственный автотранспорт, специально приспособленный для перевозки химических веществ на дальние расстояния.
При заключении долговременного на поставки продукции с нашего химического предприятия, для Вас начинают действовать особые цены, которые помогут сделать общение с нами еще более выгодным.
Хлорид калия оптом доступен для отгрузки с нашего склада, в любых количествах, в различных фасовках по самым выгодным ценам от Российского производителя. Предоставляем готовые ТУ, а также разрабатываем новые — под ваши конкретные запросы.
Изза того что вещество само по себе практически безопасно для человека, само собой в умеренных количествах, особые меры предосторожности не обязательны.
В помещениях где активно ведется работа с хлорид натрием, у рабочих должны быть маски (респираторы) и защитные очки. При попадании вещества в глаза, обильно промыть водой. При вдыхании большого количества пыли, выйти на свежий воздух, продышаться.
Среди экологических меры предосторожности есть рекомендации держать вещество подальше от канализации, поверхностных и грунтовых вод.
Производитель натрий хлорида

У нас не случайно одни из самых высоких стандартов производства хим.веществ на всем постсоветском пространстве. Все потому что наше предприятие начало совю работу еще при СССР — в 1930 году. И с тех пор мы несем эти традиции и делаем нашу работу на «отлично».
МЗХР обладает всем необходимым, что бы выполнить любой заказ точно по техническим условиям заказчика и, что не маловажно, в нужный временной интервал.
Вот какие преимущества позволяют нам этого добиться:
- собственный ж/д тупик, благодаря которому возможно отправить продукцию в любую точку Европы или Азии, а так же ближнего востока;
- контроль качества производства, имеется собственная лаборатория;
- Надежное и проверенное оборудование, которое позволяет произвести большие объемы за короткое время;
- наличие больших запасов сырья;
- собственные склады;
- свой автотранспорт.
Михайловский завод химических реагентов — российский производитель натрий хлорида, географически расположенный примерно по центру России — в Алтайском крае, нам удобно отправить продукцию как на запад, так и на восток страны.
Структурная формула
Истинная, эмпирическая, или брутто-формула: ClNa
Химический состав Хлорида натрия
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| Cl | Хлор | 35,453 | 1 | 60,7% |
| Na | Натрий | 22,99 | 1 | 39,3% |
Молекулярная масса: 58,443
Хлори́д на́трия или хлористый натрий (NaCl) — натриевая соль
соляной кислоты. Известен в быту под названием поваренной соли, основным компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде, придавая ей солёный вкус. Встречается в природе в виде минерала галита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
Нахождение в природе и производство
В природе хлорид натрия встречается в виде минерала галита, который образует залежи каменной соли среди осадочных горных пород, прослойки и линзы на берегах солёных озёр и лиманов, соляные корки в солончаках и на стенках кратеров вулканов и в сольфатарах. Огромное количество хлорида натрия растворено в морской воде. Мировой океан содержит 4 × 1015 тонн NaCl, то есть из каждой тысячи тонн морской воды можно получить в среднем 1,3 тонны хлорида натрия. Следы NaCl постоянно содержатся в атмосфере в результате испарения брызг морской воды. В облаках на высоте полтора километра 30 % капель, больших 10 мкм по размеру, содержат NaCl. Также он найден в кристаллах снега.
Наиболее вероятно, что первое знакомство человека с солью произошло в лагунах теплых морей или на соляных озёрах, где на мелководье солёная вода интенсивно испарялась под действием высокой температуры и ветра, а в осадке накапливалась соль. По образному выражению Пифагора, «соль была рождена благородными родителями: солнцем и морем».
Галит
В природе хлорид натрия чаще всего встречается в виде минерала галита. Он имеет гранецентрированную кубическую решётку и содержит 39,34 % Na, 60,66 % Cl. Другими химическими элементами, входящими в состав примесей, являются: Br, N, H, Mn, Cu, Ga, As, I, Ag, Ba, Tl, Pb, K, Ca, S, O. Плотность 2,1—2, 2 г / см ³, а твёрдость по шкале Мооса — 2. Бесцветный прозрачный минерал со стеклянным блеском. Распространённый минерал соленосных толщ. Образуется при осаждении в замкнутых водоёмах, а также как продукт сгона на стенках кратеров вулканов. Составляет пласты в осадочных породах лагунных и морских фаций, штокоподобные тела в соляных куполах и тому подобных.
Каменная соль
Каменной солью называют осадочную горную породу из группы эвапоритов, состоящую более чем на 90 % из галита. Галит также часто называют каменной солью. Эта осадочная горная порода может быть бесцветной или снежно-белой, но чаще она окрашена примесями глин, талька (серый цвет), оксидами и гидроксидами железа (жёлтый, оранжевый, розовый, красный), битумами (бурая). Каменная соль содержит хлориды и сульфаты натрия, калия, магния и кальция, бромиды, иодиды, бораты, гипс, примеси карбонатно-глинистого материала, доломита, анкериту, магнезита, битумов и так далее.
По условиям формирования месторождений каменную соль подразделяют на следующие виды:
- рассолы современных соляных бассейнов
- соляные подземные воды
- залежи минеральных солей современных соляных бассейнов
- ископаемые залежи (важнейшие для промышленности).
Морская соль
Морская соль является смесью солей (хлориды, карбонаты, сульфаты и т. д.), образующейся при полном испарении морской воды. Среднее содержание солей в морской воде составляет:
| Соединение | Масс. доля, % |
|---|---|
| NaCl | 77,8 |
| MgCl2 | 10,9 |
| MgSO4 | 4,7 |
| KCl | 2,5 |
| K2SO4 | 2,5 |
| CaCO3 | 0,3 |
| Ca(HCO3)2 | 0,3 |
| другие соли | 0,2 |
При испарении морской воды при температуре от +20 до +35 °C в осадке сначала кристаллизуются наименее растворимые соли — карбонаты кальция и магния и сульфат кальция. Затем выпадают более растворимые сульфаты натрия и магния, хлориды натрия, калия и магния, и после них — сульфаты калия и магния. Последовательность кристаллизации солей и состав осадка может несколько варьироваться в зависимости от температуры, скорости испарения и других условий. В промышленности морскую соль получают из морской воды, в основном методом обычного выпаривания. Она отличается от каменной соли значительно большим содержанием других химических солей, минералов и различных микроэлементов, в первую очередь йода, калия, магния и марганца. Соответственно, она отличается от хлорида натрия и по вкусу — горько-солёный привкус ей придают соли магния. Она используется в медицине: при лечении кожных заболеваний, таких как псориаз. Как лечебное вещество в аптечной и обычной торговой сети, распространённым продуктом является соль из Мёртвого моря. В очищенном виде этот вид соли также предлагается в продуктовой торговой сети — как натуральная и богатая йодом пищевая.
Залежи
Залежи каменной соли найдены во всех геологических системах. Важнейшие из них сосредоточены в кембрийских, девонских, пермских и третичных отложениях. Каменная соль составляет мощные пластовые залежи и ядра сводчатых структур (соляных куполов и штоков), образует прослойки, линзы, гнезда и вкрапления в других породах. Среди озёрных месторождений России крупнейшие — Эльтонское, Баскунчак в Прикаспии, Кучукское озеро, Кулундинское озеро, Эбейты и другие озёра в Западной Сибири.
Производство
В древности технология добычи соли заключалась в том, что соляную рапу (раствор) вытаскивали лошадиным приводом из шахт, которые назывались «колодцами» или «окнами», и были достаточно глубокими — 60—90 м. Извлечённый солевой раствор выливали в особый резервуар — творило, откуда она через отверстия стекала в нижний резервуар, и системой жёлобов подавалась в деревянные башни. Там её разливали в большие чаны, на которых соль вываривали.
На Руси поморы вываривали соль на побережье Белого моря и называли её морянка. В 1137 году новгородский князь Святослав определил налог на соляные варницы:
…на мори от чрена и от салгы по пузу…
Беломорской солью, называемой «морянкой», торговали по всей Российской империи до начала XX века, пока её не вытеснила более дешёвая поволжская соль.
Современная добыча хлорида натрия механизирована и автоматизирована. Соль массово добывается выпариванием морской воды (тогда её называют морской солью) или рассола с других ресурсов, таких как соляные источники и соляные озера, а также разработкой соляных шахт и добычей каменной соли.
Для добычи хлорида натрия из морской воды необходимы условия жаркого климата с низкой влажностью воздуха, наличие значительных низменных территорий, лежащих ниже уровня моря, или затопляемых приливом, слабая водопроницаемость почвы испарительных бассейнов, малое количество осадков в течение сезона активного испарения, отсутствие влияния пресных речных вод и наличие развитой транспортной инфраструктуры.
Мировое производство соли в 2009 году оценивается в 260 миллионов тонн. Крупнейшими мировыми производителями являются Китай (60,0 млн тонн), США (46,0 млн тонн), Германия (16,5 млн тонн), Индия (15,8 млн тонн) и Канада (14 млн тонн).
Применение
В пищевой промышленности и кулинарии
В пищевой промышленности и кулинарии используют хлорид натрия, чистота которого должна быть не менее 97 %. Его применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия имеет товарное название поваренная соль, порой также употребляются названия пищевая, столовая, а также уточнение названия в зависимости от её происхождения — каменная, морская, и по составу добавок — йодированная, фторированная и т. д. Такая соль является кристаллическим сыпучим продуктом с солёным вкусом без привкуса, без запаха (за исключением йодированной соли), в котором не допускаются посторонние примеси, не связанные с методом добывания соли. Кроме хлорида натрия, поваренная соль содержит небольшое количество солей кальция, магния, калия, которые придают ей гигроскопичности и жёсткости. Чем меньше этих примесей в соли, тем выше её качество.
Выделяют сорта: экстра, высший, первый и второй. Массовая доля хлористого натрия в сортах, %:
- экстра — не менее 99,5;
- высший — 98,2;
- первый — 97,5;
- второй — 97,0.
Массовая доля влаги в выварочной соли сорта «экстра» 0,1 %, в высшем сорте — 0,7 %. Допускают добавки йодида калия (йодистого калия), йодата калия, фторидов калия и натрия. Массовая доля йода должна составлять (40,0 ± 15,0) × 10−4 %, фтора (25,0 ± 5,0) × 10−3 %. Цвет экстра и высшего сортов — белый, однако для первого и второго допускается серый, желтоватый, розовый и голубоватый оттенки в зависимости от происхождения соли. Пищевую поваренную соль производят молотой и сеяной. По размеру зёрен молотую соль подразделяют на номера: 0, 1, 2, 3. Чем больше номер, тем больше зерна соли.
В кулинарии хлорид натрия потребляют как важнейшую приправу. Соль имеет характерный вкус, без которого пища кажется человеку пресной. Такая особенность соли обусловлена физиологией человека. Однако зачастую люди потребляют соли больше, чем нужно для физиологических процессов.
Хлорид натрия имеет слабые антисептические свойства — 10-15%-ное содержание соли предотвращает размножение гнилостных бактерий. Этот факт обусловливает её широкое применение как консерванта.
В медицине
Изотонический раствор хлорида натрия в воде (0,9 %) применяется как дезинтоксикационное средство, для коррекции состояния систем организма в случае обезвоживания, как растворитель других лекарственных препаратов. Гипертонические растворы (10 % р-р) используют как вспомогательный осмотический диуретик при отёке головного мозга, для поднятия давления при кровотечениях, в состояниях, характеризующихся дефицитом ионов натрия и хлора, при отравлении нитратом серебра, для обработки гнойных ран (местно). В офтальмологии как местное средство раствор хлорида натрия обладает противоотёчным действием.
В коммунальном хозяйстве. Техническая соль
Зимой хлорид натрия, смешанный с другими солями, песком или глиной — так называемая техническая соль — применяется как антифриз против гололёда. Ею посыпают тротуары, хотя это отрицательно влияет на кожаную обувь и техническое состояние автотранспорта в виду коррозийных процессов.
Регенерация Nа-катионитовых фильтров
Nа-катионитовые фильтры широко применяются в установках умягчения воды всех мощностей при водоподготовке. Катионитным материалом на современных водоподготовительных установках служат в основном глауконит, полимерные ионообменные смолы и сульфированные угли. Наиболее распространены сульфокатионитные ионообменные смолы.
Регенерацию Nа-катионитовых фильтров осуществляют 6—10%-м раствором поваренной соли, в результате катионит переводится в Na-форму, регенерируется. Реакции идут по уравнениям:
CaR2 + 2NaCl → 2NaR + CaCl2
MgR2 + 2NaCl → 2NaR +MgCl2
Химическая промышленность
Соль, наряду с каменным углем, известняками и серой, образует «большую четвёрку» продуктов минерального сырья, которые являются важнейшими для химической промышленности. Из неё получают соду, хлор, соляную кислоту, гидроксид натрия, сульфат натрия и металлический натрий. Кроме этого соль используется также для промышленного получения легкорастворимого в воде хлората натрия, который является средством для уничтожения сорняков. Суммарное уравнение реакции электролиза горячего раствора хлорида натрия:
NaCl + 3H2O → NaClO3 + 3H2
Физические и физико-химические свойства
Температура плавления +800,8 °С, кипения +1465 °С.
Умеренно растворяется в воде, растворимость мало зависит от температуры: коэффициент растворимости NaCl (в граммах на 100 г воды) равен 35,9 при +21 °C и 38,1 при +80 °C. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов. Растворяется в жидком аммиаке, вступает в реакции обмена. В чистом виде хлорид натрия не гигроскопичен. Однако соль часто бывает загрязнена примесями (преимущественно ионами Ca2+, Mg2+ и SO2-4), и такая соль на воздухе сыреет. Кристаллогидрат NaCl · 2H2O можно выделить при температуре ниже +0,15 °C.
Смесь измельчённого льда с мелким порошком хлорида натрия является эффективным охладителем. Так, смесь состава 30 г NaCl на 100 г льда охлаждается до температуры −20 °C. Это происходит потому, что водный раствор соли замерзает при температуре ниже 0 °C. Лёд, имеющий температуру около 0 °C, плавится в таком растворе, поглощая тепло окружающей среды.
| Термодинамические характеристики | |
|---|---|
| ΔfH0g | −181,42 кДж/моль |
| ΔfH0l | −385,92 кДж/моль |
| ΔfH0s | −411,12 кДж/моль |
| ΔfH0aq | −407 кДж/моль |
| S0g, 1 bar | 229,79 Дж/(моль·K) |
| S0l, 1 bar | 95,06 Дж/(моль·K) |
| S0s | 72,11 Дж/(моль·K) |
Диэлектрическая проницаемость NaCl — 6,3
Плотность и концентрация водных растворов NaCl
| Концентрация, % | Концентрация, г/л | Плотность, г/мл |
|---|---|---|
| 1 | 10,05 | 1,005 |
| 2 | 20,25 | 1,012 |
| 4 | 41,07 | 1,027 |
| 6 | 62,47 | 1,041 |
| 8 | 84,47 | 1,056 |
| 10 | 107,1 | 1,071 |
| 12 | 130,2 | 1,086 |
| 14 | 154,1 | 1,101 |
| 16 | 178,5 | 1,116 |
| 18 | 203,7 | 1,132 |
| 20 | 229,5 | 1,148 |
| 22 | 256 | 1,164 |
| 24 | 283,2 | 1,18 |
| 26 | 311,2 | 1,197 |
Структура
Хлорид натрия образует бесцветные кристаллы кубическая сингония, пространственная группа Fm3m, параметры ячейки a = 0,563874 нм, d = 2,17 г/см3. Каждый из ионов Cl— окружён шестью ионами Na+ в октаэдрической конфигурации, и наоборот. Если мысленно отбросить, например, ионы Na+, то останется плотно упакованная кубическая структура ионов Cl—, называемая гранецентрированной кубической решёткой. Ионы Na+ тоже образуют плотно упакованную кубическую решётку. Таким образом, кристалл состоит из двух подрешёток, сдвинутых друг относительно друга на полупериод. Такая же решётка характерна для многих других минералов.
В кристаллической решётке между атомами преобладает ионная химическая связь, что является следствием действия электростатического взаимодействия противоположных по заряду ионов.