Из Википедии, бесплатной энциклопедии
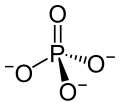
| Структурная формула | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Общий | ||||||||||
| Фамилия | Фосфат натрия | |||||||||
| Другие названия |
| |||||||||
| Молекулярная формула | Na 3 PO 4 | |||||||||
| Краткое описание | белое твердое вещество без запаха | |||||||||
| Внешние идентификаторы / базы данных | ||||||||||
| ||||||||||
| Информация о наркотиках | ||||||||||
| Код УВД | A06 AD17 , V10 XX01 | |||||||||
| характеристики | ||||||||||
| Молярная масса |
| |||||||||
| Физическое состояние | твердо | |||||||||
| плотность | 1,62 г см -3 (додекагидрат) | |||||||||
| Температура плавления |
| |||||||||
| значение pK s | pK b : 1,64 | |||||||||
| растворимость | легко в воде (285 г л -1 при 20 ° C, додекагидрат) | |||||||||
| Инструкции по технике безопасности | ||||||||||
| ||||||||||
| Насколько это возможно и общепринято, используются единицы СИ . Если не указано иное, приведенные данные относятся к стандартным условиям . | ||||||||||
Фосфат натрия представляет собой натриевую соль из фосфорной кислоты . Он состоит из ионов натрия (3 Na + ) и фосфата (PO 4 3– ).
Извлечение и представление
Фосфат натрия может быть получен путем нейтрализации фосфорной кислоты с гидроксидом натрия . Это не обязательно должно происходить в водной среде.
характеристики
Фосфат натрия образует бесцветные кристаллы. Фосфат натрия в водном растворе имеет основную реакцию , поскольку основной ион фосфата протонирован . РН десять процентов раствора составляет 11.8-12.2.
Соединение встречается в нескольких модификациях, таких как тетрагональная [α], орторомбическая [β] и орторомбическая (псевдокубическая) [γ] форма. Α-форма возникает при температуре ниже 600 ° C (a = 10,757 и c = 6,824 Å ). Γ-форма возникает между 700 ° C и 800 ° C (a = 5,237, b = 5,203 и c = 7,400 Å) и имеет кристаллическую структуру с пространственной группой Pnma (пространственная группа № 62) . Ранее не охарактеризованная β-форма, по-видимому, является промежуточным продуктом при изменении α → γ и γ → α и всегда была получена в смеси с α или γ формой. Их структура тесно связана со структурой β- арсената натрия Na 3 AsO 4 . Теплопроводность при 300 К составляет 0,8 Вт · м −1 · K −1 .
использовать
Фосфаты используются в качестве добавок к моющим средствам . Они способны образовывать комплексы с ионами многовалентных металлов (Mg 2+ и др.). Твердость снижена. Их использование сейчас запрещено в некоторых странах (включая Швейцарию ). Фосфат натрия, известный как «тринатрийфосфат», используется в качестве дозирующего раствора при работе паровых котлов и контуров нагрева воды для смягчения содержащейся воды и в то же время для ее подщелачивания ( защита от коррозии ). Для этого в дозирующую емкость готовят 3–5- процентный раствор (3–5 кг / 100 л). Дозирование целесообразно производить с помощью дозирующего насоса в бак питательной воды , при необходимости в бак конденсата . Количество воды, добавляемой для заполнения в системах отопления, зависит от жесткости и количества воды для заполнения. На 1 м³ наполняемой воды при 0,18 моль / м³ = 1 ° dH добавляют 68 г тринатрийфосфата.
Пример:
- Заполняемый объем отопительной системы: 0,8 м³.
- Заполняющая вода — GH 2,14 моль / м³ = 12 ° dH
- Количество тринатрийфосфата = количество заправки [м³] умноженное на [° dGH] умноженное на 68 [г] = 0,8 × 12 умноженное на 68
- Количество добавленного тринатрийфосфата = 650 г
Добавление целесообразно проводить в обратной линии отопления с помощью дозирующего насоса или шлюза для подачи химикатов.
В пищевой промышленности фосфат натрия используется в качестве комплексообразователя , кислотного регулятора , плавящейся соли или агента для схватывания . Вместе с дигидрофосфатом натрия и гидрофосфатом динатрия он одобрен в ЕС в качестве пищевой добавки под общим номером E 339 («фосфат натрия») для определенных пищевых продуктов, каждый из которых имеет различные ограничения по максимальному количеству. Согласно Постановлению об одобрении добавок , это — в основном единообразные для большинства одобренных фосфатов — индивидуальные спецификации для широкого диапазона с множеством различных типов пищевых продуктов. Максимально допустимые количества варьируются от 0,5 до 50 граммов на килограмм (в сливках для торговых автоматов) или при отсутствии фиксированного ограничения ( квантовое удовлетворение — по мере необходимости, для пищевых добавок и иногда для жевательной резинки).
Фосфаты также используются в качестве искусственных удобрений .
Радиоактивный фосфор 32 используется в качестве фосфата натрия (или дигидрофосфата ) для терапии ядерной медициной при истинной полицитемии ( радиофосфорная терапия ).
Биологическое значение
Следствием использования фосфатов в моющих средствах является больший запас питательных веществ в воде . Это приводит к усиленному росту водорослей , что может привести к опрокидыванию водоема.
Индивидуальные доказательства
- ↑ Запись на E 339: Фосфаты натрия в европейской базе данных по пищевым добавкам, по состоянию на 29 декабря 2020 г.
- ↑ б с д е е г ч записи на тринатрийфосфате в базе данных GESTIS вещества в IFA , доступ к 10 января 2017 года. (Требуется JavaScript)
- ↑ Запись о фосфорной кислоте. В: Römpp Online . Георг Тиме Верлаг, доступ 29 мая 2014 г.
- ↑ М. Кизилялли, AJE Welch: Получение и данные порошковой рентгеновской дифракции для безводных ортофосфатов натрия. В: Журнал неорганической и ядерной химии. 38, 1976, стр. 1237, DOI : 10.1016 / 0022-1902 (76) 80127-3 .
- ↑ Башир М. Сулейман и Арнольд Лунден: Теплопроводность и коэффициент диффузии ортофосфата натрия . В кн . : J. Phys.: Condens. Материя . Лента 15 , вып. 41 , 2003, с. 6911-6918 , DOI : 10,1088 / 0953-8984 / 15/41/001 .
Свойства фосфата натрия
Физические свойства
| Свойство | Описание |
| Внешний вид | Кристаллическое вещество белого цвета |
| Молярная масса | 163,941 г/моль |
| Плотность | 2,536 г/см3 |
| Температура плавления | 1340°С |
| Cтандартная мольная энтальпия образования при 298К Δ G Delta G ΔG °298, кДж/моль | -1922,8 |
| Cтандартная мольная энергия Гиббса образования при 298 К Δ Delta Δ кДж/моль | -1819 |
| Стандартная мольная энтропия при 298 К S°298, Дж/(моль•К) | 224,7 |
| Растворимость в воде, 100 г | при 0°С — 5,4 при 25°С — 14,5 при 100°С — 94,6 |
Химические свойства
В водных растворах гидролизуется по аниону:
Na3P04 + H2O = Na2HP04 + Na0H.
Раствор имеет щелочную реакцию.
При взаимодействии с кислотами образует кислые соли:
Na3P04 + HСl = Na2HP04 + NaCl,
Na3P04 + H2SO4 = NaH2P04 + Na2SO4.
Вступает в реакции обмена с образованием нерастворимых фосфатов:
2Na3P04 + 3CaCl2 = 6NaCl + 2Ca3(P04)2↓,
Na3P04 + AlCl3 = 3NaCl + AlP04↓,
Na3P04 + 3AgNO3 = 6NaCl + Ag3P04↓.
Последняя реакция является качественной реакцией на растворимые фосфаты щелочных металлов и аммония. При добавлении к их раствором раствора нитрата серебра AgNO3 выпадает осадок фосфата серебра Ag3P04 желтого цвета. А натрий можно определить окрашиванию пламени в желтый цвет.
Литература
- Химическая энциклопедия / Редкол.: Зефиров Н.С. и др.. — М.: Большая Российская энциклопедия, 1998. — Т. 5. — 783 с. — ISBN 5-85270-310-9.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др.
Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
Это заготовка статьи о неорганическом веществе. Вы можете помочь проекту, дополнив её.
Получение химического соединения
Лабораторные способы получения
Фосфат натрия получают взаимодействием фосфорной кислоты с гидроксидом или карбонатом натрия:
H3PO4 + 3NaOH = Na3PO4 + 3H2O; 2H3PO4 + 3Na2CO3 =2Na3PO4 + 3H2O + 3CO2↑.
Получение фосфата натрия в промышленности
В промышленности фосфат натрия получают в два этапа.
Сначала взаимодействием кальцинированной соды Na2CO3 с фосфорной кислотой H3PO4 получают гидрофосфат натрия Na2HP04:
Н3Р04 + Na2C03 = Na2HP04 + С02↑+ Н20,
а затем взаимодействием едкого натра NaOH с полученным гидрофосфатом натрия Na2HP04 получают фосфат натрия Na3PO4:
Na2HP04 + Na0H = Na3P04 + H20.
После охлаждения нейтрализованных растворов до 30°С фосфат натрия кристаллизуются в виде Na3PO4·12H2O. Он плавится при 70°С. Чтобы получить безводный фосфат натрия, кристаллогидрат прокаливают 2 часа при температуре 120°С, а затем 30 мин при температуре 800°С.
Гексаметафосфат натрия — пищевая добавка и эффективный умягчитель воды
Продолжаем тему пищевых добавок — производных натрия. Гексаметафосфат натрия — неорганическое соединение, натриевая соль гексафосфорной кислоты. В литературе можно встретить такие названия, как натрий фосфорнокислый; гексафосфат, полифосфат, соль Грэма (в другой транскрипции Грэхама); добавка Е452 (i).
Формула соединения — Na6P6O18. Получают его из расплава гидрофосфата натрия или химической реакцией соли ортофосфорной кислоты и соли натрия.
Свойства
Мелкий белый порошок со стеклообразными прозрачными кристалликами, гранулами или чешуйками, не имеющими запаха и вкуса. Водорастворим, легко впитывает влагу, расплывается от контакта с влагой воздуха, превращается в пирофосфат (Na4P2O7), а затем в ортофосфат (Na3PO4). Может выкристаллизовываться из раствора в качестве кристаллогидрата Na6P6O18•6H2O. Не горит, не взрывается, не ядовит. Обладает высокими адсорбционными и гомогенизирующими (эмульгирующими) качествами. В химических реакциях образует комплексные соединения с различными металлами, в том числе с кальцием и магнием.
| Магний металлический (стружка) «хч» | Натрия полифосфат (гексаметафосфат натрия, Е452, соль Грэма) | Склянка светлая (флакон), 2000 мл, с пробкой (шир. горловина) |
Вещество присутствует в организме человека, участвует в ионном обмене и в создании тромбоцитов, частично регулируя свертываемость крови. Способствует накоплению и освобождению энергии в клетках. Гексаметафосфат натрия полезен для пищеварительной системы, он убивает бактерии, вырабатывающие крайне опасный ботулотоксин. Не накапливается в организме, разрешен для использования в пище почти во всех странах.
Фосфорнокислый натрий относится к 3-му классу опасности (как и поваренная соль). Его пыль может вызывать раздражение верхних дыхательных путей. При приеме внутрь большой дозы может произойти сбой кислотно-щелочного баланса, в работе органов ЖКТ, развиться обезвоживание.
Работать с гексафосфатом надо в вентилируемом помещении, используя средства защиты кожи, глаз, органов дыхания. Хранить вещество следует в герметично заваренных полиэтиленовых мешках, укрепленных бумажными или тканевыми мешками, защищая от влаги воздуха. Помещение должно быть крытым, неотапливаемым.
Применение
- В пищепроме — стабилизатор, эмульгатор, фиксатор окраски. Способствует удержанию влаги, уплотнению и однородности структуры продукта, продлению срока хранения, развитию дрожжевых культур, усилению действия антиоксидантов. Используется при изготовлении плавленых сыров, маргаринов, мясных и рыбных консервов, полуфабрикатов быстрой заморозки, колбасных изделий; продуктов переработки картофеля; сливок, сухого и сгущенного молока; продуктов с пектинами, глазированных фруктов, фруктового мороженого; хлебобулочных изделий; ликероводочных напитков; спортивных смесей.
- В текстильпроме — для приготовления рабочих растворов (реагент переводит нерастворимые соли кальция в растворимые).
- В кожевенном деле.
- Для смягчения воды, уменьшения накипи, защиты от коррозии, продления срока службы котлов и трубопроводов в различных системах водоснабжения и охлаждения, в том числе в железнодорожных и промышленных силовых установках.
- Для фильтрации растворов и пульпы в нефтедобыче.
- В химпроме — компонент средств для удаления накипи и моющих средств. Добавка полифосфата в стиральные моющие средства избавляет вещи после стирки от серого налета.
- При производстве бумаги в целлюлозно-бумажной индустрии.
- В зубных пастах — для уменьшения зубного налета и камня, защиты от воздействия кислот.
- При производстве комплексных удобрений в сельском хозяйстве, в фотоделе.
- В фармацевтике.
Применение
Фосфат натрия в быту используют как чистящее средство, так как он прекрасно отмывает жир. Благодаря этому свойству он также входит в состав моющих средств. Кроме того, фосфат натрия смягчает воду, переводя соли жесткости в нерастворимые фосфаты:
3Ca(HCO3)2 + 2Na3P04 = 6NaHCO3 + Ca3(P04)2↓, 3Mg(HCO3)2 + 2Na3P04 = 6NaHCO3 + Mg3(P04)2↓. Применяется он также и в стекольной промышленности для получения оптических стекол.
В строительстве фосфат натрия используют для упрочнения бетона. Его добавка увеличивает также влагостойкость бетона, так как он становится менее пористым.
В медицине фосфат натрия изредка применяют как слабительное и средство от изжоги.
В пищевой промышленности он известен как пищевая добавка Е339(iii). Фосфат натрия используют в качестве эмульгатора, стабилизатора, влагоудерживающего агента. Добавляют его в майонезы и кетчупы, плавленные сыры и хлебобулочные изделия, правда чаще применяют гидрофосфат (пищевая добавка Е339(i)) и дигидрофосфат натрия (пищевая добавка Е339(iii)). Фосфатом натрия обрабатывают куриные окорочка, мясо и рыбу, чтобы удержать воду и сохранить вес.
Относится к малоопасным веществам (4 класс опасности), но при передозировке в пищевых продуктов приводит к расстройствам пищеварения, а у детей нередко вызывает возбуждение и гиперактивность.
Отрывок, характеризующий Метафосфат натрия
«Весна, и любовь, и счастие!» – как будто говорил этот дуб, – «и как не надоест вам всё один и тот же глупый и бессмысленный обман. Всё одно и то же, и всё обман! Нет ни весны, ни солнца, ни счастия. Вон смотрите, сидят задавленные мертвые ели, всегда одинакие, и вон и я растопырил свои обломанные, ободранные пальцы, где ни выросли они – из спины, из боков; как выросли – так и стою, и не верю вашим надеждам и обманам». Князь Андрей несколько раз оглянулся на этот дуб, проезжая по лесу, как будто он чего то ждал от него. Цветы и трава были и под дубом, но он всё так же, хмурясь, неподвижно, уродливо и упорно, стоял посреди их. «Да, он прав, тысячу раз прав этот дуб, думал князь Андрей, пускай другие, молодые, вновь поддаются на этот обман, а мы знаем жизнь, – наша жизнь кончена!» Целый новый ряд мыслей безнадежных, но грустно приятных в связи с этим дубом, возник в душе князя Андрея. Во время этого путешествия он как будто вновь обдумал всю свою жизнь, и пришел к тому же прежнему успокоительному и безнадежному заключению, что ему начинать ничего было не надо, что он должен доживать свою жизнь, не делая зла, не тревожась и ничего не желая. По опекунским делам рязанского именья, князю Андрею надо было видеться с уездным предводителем. Предводителем был граф Илья Андреич Ростов, и князь Андрей в середине мая поехал к нему. Был уже жаркий период весны. Лес уже весь оделся, была пыль и было так жарко, что проезжая мимо воды, хотелось купаться. Князь Андрей, невеселый и озабоченный соображениями о том, что и что ему нужно о делах спросить у предводителя, подъезжал по аллее сада к отрадненскому дому Ростовых. Вправо из за деревьев он услыхал женский, веселый крик, и увидал бегущую на перерез его коляски толпу девушек. Впереди других ближе, подбегала к коляске черноволосая, очень тоненькая, странно тоненькая, черноглазая девушка в желтом ситцевом платье, повязанная белым носовым платком, из под которого выбивались пряди расчесавшихся волос. Девушка что то кричала, но узнав чужого, не взглянув на него, со смехом побежала назад. Князю Андрею вдруг стало от чего то больно. День был так хорош, солнце так ярко, кругом всё так весело; а эта тоненькая и хорошенькая девушка не знала и не хотела знать про его существование и была довольна, и счастлива какой то своей отдельной, – верно глупой – но веселой и счастливой жизнию. «Чему она так рада? о чем она думает! Не об уставе военном, не об устройстве рязанских оброчных. О чем она думает? И чем она счастлива?» невольно с любопытством спрашивал себя князь Андрей. Граф Илья Андреич в 1809 м году жил в Отрадном всё так же как и прежде, то есть принимая почти всю губернию, с охотами, театрами, обедами и музыкантами. Он, как всякому новому гостю, был рад князю Андрею, и почти насильно оставил его ночевать. В продолжение скучного дня, во время которого князя Андрея занимали старшие хозяева и почетнейшие из гостей, которыми по случаю приближающихся именин был полон дом старого графа, Болконский несколько раз взглядывая на Наташу чему то смеявшуюся и веселившуюся между другой молодой половиной общества, всё спрашивал себя: «о чем она думает? Чему она так рада!». Вечером оставшись один на новом месте, он долго не мог заснуть. Он читал, потом потушил свечу и опять зажег ее. В комнате с закрытыми изнутри ставнями было жарко. Он досадовал на этого глупого старика (так он называл Ростова), который задержал его, уверяя, что нужные бумаги в городе, не доставлены еще, досадовал на себя за то, что остался. Князь Андрей встал и подошел к окну, чтобы отворить его. Как только он открыл ставни, лунный свет, как будто он настороже у окна давно ждал этого, ворвался в комнату. Он отворил окно. Ночь была свежая и неподвижно светлая. Перед самым окном был ряд подстриженных дерев, черных с одной и серебристо освещенных с другой стороны. Под деревами была какая то сочная, мокрая, кудрявая растительность с серебристыми кое где листьями и стеблями. Далее за черными деревами была какая то блестящая росой крыша, правее большое кудрявое дерево, с ярко белым стволом и сучьями, и выше его почти полная луна на светлом, почти беззвездном, весеннем небе. Князь Андрей облокотился на окно и глаза его остановились на этом небе. Комната князя Андрея была в среднем этаже; в комнатах над ним тоже жили и не спали. Он услыхал сверху женский говор. – Только еще один раз, – сказал сверху женский голос, который сейчас узнал князь Андрей. – Да когда же ты спать будешь? – отвечал другой голос. – Я не буду, я не могу спать, что ж мне делать! Ну, последний раз… Два женские голоса запели какую то музыкальную фразу, составлявшую конец чего то.
Получение[ | ]
1. Взаимодействие H3PO4 с Na2CO3:
2 H 3 P O 4 + 3 N a 2 C O 3 ⟶ 2 N a 3 P O 4 + 3 C O 2 + 3 H 2 O {displaystyle {mathsf {2H_{3}PO_{4}+3Na_{2}CO_{3}longrightarrow 2Na_{3}PO_{4}+3CO_{2}+3H_{2}O}}}
2. Взаимодействие H3PO4 с NaOH:
H 3 P O 4 + 3 N a O H ⟶ N a 3 P O 4 + 3 H 2 O {displaystyle {mathsf {H_{3}PO_{4}+3NaOHlongrightarrow Na_{3}PO_{4}+3H_{2}O}}}
3. Сплавление P 2 O 5 {displaystyle {ce {P2O5}}} с щелочью, оксидом, карбонатом, пероксидом и др. солями:
P 2 O 5 + 6 NaOH ⟶ 2 Na 3 PO 4 + 3 H 2 O {displaystyle {ce {P2O5 + 6NaOH -> 2Na3PO4 + 3H2O}}}
P 2 O 5 + 3 Na 2 CO 3 ⟶ 2 Na 3 PO 4 + 3 CO 2 {displaystyle {ce {P2O5 + 3Na_2CO_3 -> 2Na_3PO_4 + 3CO_2}}}
P 2 O 5 + 3 Na 2 O ⟶ 2 Na 3 PO 4 {displaystyle {ce {P2O5 + 3Na2O -> 2Na3PO4}}}
( 1 оценка, среднее 5 из 5 )
Фосфат натрия, что это. Трифосфат натрия
| Трифосфат натрия | |
|---|---|
| Общие | |
| Хим. формула | Na5Р3О10 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 367.864 г/ моль |
| Плотность | 2.52 г/см³ |
| Термические свойства | |
| Т. плав. | 622 °C |
| Химические свойства | |
| Растворимость в воде | 14.5 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7758-29-4 |
| PubChem | 24455 |
| Рег. номер EINECS | 231-838-7 |
| SMILES | |
| InChI | 1S/5Na.H5O10P3/c;;;;;1-11(2,3)9-13(7,8)10-12(4,5)6/h;;;;;(H,7,8)(H2,1,2,3)(H2,4,5,6)/q5*+1;/p-5 HWGNBUXHKFFFIH-UHFFFAOYSA-I |
| Кодекс Алиментариус | E451 |
| RTECS | YK4570000 |
| ChemSpider | 22863 |
| Приводятся данные для, если не указано иного. |
Трифосфат натрия — это соль триполифосфорной кислоты Na5Р3О10. Является пищевым стабилизатором , более известным как Е451.
Фосфаты ослабляют электростатическое взаимодействие внутри актомиозинового комплекса. Только фосфаты могут расщеплять актин и миозин, и это является главной причиной распространения фосфатов.
Практически все пищевые фосфаты и их смеси, которые используются мясоперерабатывающей и рыбной промышленности, имеют щелочную реакцию. Добавка щелочных фосфатов в мясо и рыбу приводит к росту pH , и как следствие, к увеличению влагосвязывающего свойства белков.
Пирофосфаты (E450) и триполифосфат (E451) лучше всего способствуют эмульгированию жира, что объясняет включение этого вещества в состав многих стиральных порошков и средств для посудомоечных машин.
Потребление выше разрешённых норм фосфатов может негативно сказаться на здоровье человека, из-за чего происходит ухудшение усвоения кальция, что приводит к отложению в почках кальция и фосфора, и способствует развитию остеопороза .
Трифосфат натрия синтезируется путём конденсации из ортофосфорной кислоты :
В лабораторных условиях он синтезируется из фосфата натрия и дифосфата натрия :
Также возможен синтез из триметафосфата натрия :
- М.: Советская энциклопедия, 1983. — 792 с.
С чем реагирует фосфат натрия. Ортофосфат натрия
(перенаправлено с «»)
| Ортофосфат натрия | |
|---|---|
|
Внешний вид водного ортофосфата натрия . | |
| данные приведены по изданию Химическая энциклопедия. В пяти томах. / Под ред. И.Л. Кнунянц. — | |
| Общие | |
| Систематическое наименование | натрия ортофосфат |
| Хим. формула | Na3PO4 |
| Физические свойства | |
| Состояние | твёрдое кристаллическое вещество |
| Примеси | вода, входит в состав кристаллогидратов ортофосфатов натрия |
| Молярная масса | 163,94067 г/ моль |
| Плотность | безводный — 2,536; кристаллогидрат — 1,62 г/см³ |
| Термические свойства | |
| Т. плав. | безводный — 1340; кристаллогидрат — 73,3÷76,7 °C |
| безводный -1922,8; кристаллогидрат -4471,6 кДж/моль | |
| Химические свойства | |
| Растворимость в воде | в пересчете на безводный 12,1(0°С); 94,6(100°С) |
| Классификация | |
| Рег. номер CAS | 7601-54-9 |
| PubChem | 24243 |
| Рег. номер EINECS | 231-509-8 |
| SMILES | |
| InChI | 1S/3Na.H3O4P/c;;;1-5(2,3)4/h;;;(H3,1,2,3,4)/q3*+1;/p-3 RYFMWSXOAZQYPI-UHFFFAOYSA-K |
| Кодекс Алиментариус | E339(iii) |
| RTECS | TC9575000 |
| ChEBI | 37583 |
| ChemSpider | 22665 |
| Приводятся данные для, если не указано иного. |
Фосфат натрия (ортофосфат натрия) — натриевая соль ортофосфорной кислоты с химической формулой Na3PO4.
Фосфат натрия — соль. Белого цвета, гигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде, гидролизуется по аниону, создает в растворе сильнощелочную среду. Реагирует в растворе с цинком и алюминием. Вступает в реакции ионного обмена.
В присутствии воды образует кристаллогидрат с общей формулой Na3PO4×12H2O.
Использование фосфата натрия в стиральных порошках запрещено во многих странах для уменьшения эвтрофикации водоемов.
В продуктах питания (пищевая добавка E339(iii)) используется не фосфат натрия, а дигидрофосфат как разрыхлитель для теста (при взаимодействии с пищевой содой ) и эмульгатор для плавленого сыра , колбасы , сгущённого молока .
Применяется для обесцвечивания стекла при его плавке.
- Натрия фосфаты
- ГОСТ 31725-2012 . Добавки пищевые. Натрия фосфаты Е339. Общие технические условия
Фосфат натрия + хлорид кальция. Читайте также
Kladkova2001 / 01 янв. 2015 г., 0:16:17
К 250 г. раствора хлорида кальция прилили 500 г. 8,48 % раствора соды. Полученный осадок отфильтровали. К фильтрату добавили 10% раствор соляной кислоты
до прекращения выделения пузырьков газа, всего было израсходовано 146 г. кислоты. Вычислите массовую долю хлорида кальция в исходном растворе.
10-11 класс химия
Kjbkjh / 10 апр. 2014 г., 17:44:03
Помогите! Нужно записать уравнения в ионной, молекулярной, полной и краткой формах1) гидроксит бартя+азотная кислота2) карбонат калия+ фосфорная кислота3)
хлорид магния+фосфат натрия
10-11 класс химия
Иралия00 / 15 апр. 2014 г., 15:04:59
1. При сливании растворов хлорида алюминия и карбоната натрия…
1) образуется только осадок, а газ не выделяется 2) образуется осадок и выделяется газ
3) выделяется газ, а раствор остается прозрачным 4) ничего не происходит
2. В водных растворах не подвергается гидролизу
1)сульфат натрия 2)сульфат алюминия 3)сульфит натрия 4)сульфат меди
3. В водных растворах не подвергается гидролизу хлорид
1) меди 2) бария 3) цинка 4) бериллия
4. В водных растворах необратимо гидролизуются
А) нитрат железа(III) Б) нитрат железа(II) В) фосфат натрия
Г) сульфид алюминия Д) силикат аммония Е) нитрат цезия
1) А,Б,Е 2) В, Д 3) Г 4)Г, Д
5.При добавлении к воде щелочную среду создает:
1) сульфата меди (II) 2) карбонат калия 3) карбонат кальция 4) нитрат алюминия
6. При добавлении к воде кислотную среду создает:
1)ацетат натрия 2) сульфид свинца 3) нитрат железа(III) 4) фосфата калия
7. Кислотную реакцию среды имеют растворы:
1) сульфата магния и нитрата кальция
2) нитрата железа(III) и хлорида алюминия
3) бромида аммония и карбоната натрия
4) сульфида натрия и хлорида калия
8. Гидролиз по аниону имеет место в водных растворах:
А) K2SO4 Б) FeSO4 В) Na2CO3 Г) CH3COONa Д) K2S Е) FeCl3
1) А, Б, Е 2) В, Г, Д 3) Г, Д 4)В, Д
9.Полному и необратимому гидролизу подвергается
1) сульфид алюминия 2) силикат натрия 3) сульфид калия 4) хлорид бария
10. Щелочную реакцию среды имеют растворы:
1) иодида кальция и сульфата аммония
2) нитрата железа(III) и нитрата алюминия
3) фосфата натрия и перманганата калия
4) карбоната калия сульфида натрия
11. Какое вещество полностью гидролизуется в водном растворе?
Фосфат натрия вред
 Фосфат натрия – это частый «спутник» многих продуктов питания. Также его можно обнаружить в составе синтетических моющих средств. И несмотря на то, что данное вещество является потенциально опасным для здоровья человека, во многих странах мира его использование не запрещено, и Россия также входит в список этих государств.
Фосфат натрия – это частый «спутник» многих продуктов питания. Также его можно обнаружить в составе синтетических моющих средств. И несмотря на то, что данное вещество является потенциально опасным для здоровья человека, во многих странах мира его использование не запрещено, и Россия также входит в список этих государств.
Характеристика вещества
Фосфат натрия относится к ряду солей натрия фосфорных кислот.
Его физические свойства будут следующими:
- данное вещество являет собою белые гранулы либо кристаллы;
- в воде растворимо хорошо;
- термически устойчиво.
Технологические функции
В промышленном производстве добавка Е339 выполняет такие функции:
- регулятор кислотности, который способствует поддержанию необходимого рН уровня;
- стабилизатор – придает продукту определенную текстуру, форму, принимает непосредственное участие в формировании и сохранности консистенции;
- эмульгатор – помогает соединить вещества, которые при обычных условиях не смешиваются.
Виды фосфатов
Существует три вида фосфатов натрия, которые будут отличаться химической формулой и номенклатурным значением, при помощи которого их можно распознать на этикетках продуктов:
- однозамещенный фосфат, или добавка Е339 (I) — NaH2PO4 ;
- двузамещенный фосфат, или добавка Е339 (II) — Na2HPO4 ;
- трехзамещенный фосфат, или добавка Е339 (III) — Na3PO4 .
Вредное воздействие
Вред фосфата натрия проявляется в зависимости от вида продукта, в который он входит. Например, синтетические моющие средства с его содержанием оказывают неблагоприятное воздействие на кожные покровы, а проявляется это в виде аллергии – сыпи, а в особо тяжелых ситуациях развивается экзема.
Рекомендация! Чтобы защитить свою кожу, при использовании фосфатосодержащих средств желательно надевать резиновые перчатки!
Продукты питания, содержащие в своем составе добавку с индексом Е339, обладают более широким спектром вредных свойств, которые проявляются, как:
- диарея;
- гастриты;
- язва желудка;
- нарушение обмена кальция;
- злокачественные новообразования в желудочно-кишечном тракте.
Что такое фосфат натрия для ребенка?
Детский организм более восприимчив к влиянию подобных веществ и его реакция проявляется в виде нервных и психических расстройств.
У ребенка может наблюдаться:
- моторное беспокойство;
- гиперактивность;
- импульсивность;
- агрессия;
- беспокойство;
- снижение концентрации внимания.
На заметку! Что характерно, если из меню убрать продукты, содержащие добавку Е339, то все симптомы постепенно будут сходить на нет и в скором времени полностью исчезнут без применения медикаментозного лечения!
Применение
В непищевой промышленности фосфат кальция входит в состав стиральных и чистящих порошков. А список продуктов питания, содержащих эту вредную добавку, выглядит следующим образом:
- хлебобулочные и кондитерские изделия, где он исполняет функцию разрыхлителя;
- молочная продукция – молоко, сухие сливки, сгущенное молоко, где он применяется как антикристаллизатор и вещество, которое помогает увеличить сроки хранения готовых продуктов;
- сыры, в основном, плавленые – колбасные, ломтевые, пастообразные, где его используют в качестве сольплавителя.
На заметку! При изготовлении всех вышеописанных продуктов питания используется фосфат натрия двухзамещенный!
Кроме того, добавку Е339 можно встретить на упаковках мясных продуктов, сухих бульонов и супов, соусов, чая в пакетиках.
Фосфат натрия гидролиз. Na3PO4 + H2O = ? уравнение реакции
Что происходит при растворении фосфата натрия в воде (Na3PO4 + H2O = ?)? Подвергается ли данная соль гидролизу? Дайте определение понятию «гидролиз». Расскажите о том, какие соли подвергаются гидролизу, а какие – не подвергаются.
1 ответ
Фосфат натрия – средняя соль, образованная слабой кислотой – фосфорной () и сильным основанием – гидроксидом натрия (), это означает, что она подвергается гидролизу по аниону (Na3PO4 + H2O = ?). Теоретически возможно записать гидролиз в три ступени, но в реальности он протекает только по первой:
Наличие гидроксид-ионов в реакционной смеси свидетельствует о щелочном характере среды.
Гидролизом называется взаимодействие вещества с водой, при котором составные части вещества соединяются с составными частями воды. Примером гидролиза может служить взаимодействие хлорида фосфора (III)с водой. В результате этой реакции образуются фосфористая кислотаи соляная кислота:
Гидролизу подвержены соединения различных классов.
В реакции гидролиза вступают соли, образованные слабой кислотой и слабым основанием, или слабой кислотой и сильным основанием, или слабым основанием и сильной кислотой. Соли. Образованные сильной кислотой и сильным основанием, гидролизу не подвергаются; нейтрализация в этом случае сводится к процессу:
а обратная реакция – диссоциация молекулы воды на ионы – протекает в ничтожно малой степени.








