Содержание
- История открытия Zn
- Происхождение названия
- Нахождение в природе
- Получение цинка
- Физические свойства
- Химические свойства
- Применение
- Производство цинка в мире
- Биологическая роль цинка
- Содержание в продуктах питания
- Отражение недостатка цинка на здоровье человека
- Токсичность цинка
История открытия Zn
Еще в Древней Греции был открыт такой элемент, как латунь. Это сплав цинка и меди. Из латуни в те времена делали очень многие изделия. Чистый цинк люди не могли выделить длительное время из-за сложностей в его окислении на воздухе.
Андреас Сигизмунд Маргграф
В XVII веке в Англии наконец сумели изобрести способ добычи цинк в чистом виде с помощью метода дистилляции. В следующем веке начали получать его уже в промышленных масштабах. В городе Бристоле даже создали специальный цинковый завод, который успешно работал длительное время.
Несколько позже цинк научились добывать другим методом — с помощью прокаливания оксида цинка и угля, при этом обязательным условием было отсутствие доступа кислорода. Такую смесь требовалось хранить в специальных условиях и поддерживать температурный режим.
Немецкий химик Анреас Маргграф в 1746 г. впервые изобрел такой способ получения цинка. Именно этот человек и считается первооткрывателем чистого цинка. Он также определил и строение атома этого элемента.
С помощью так называемой прокатки уже в XVIII в. ученые Чарльз Сильвестр и его тезка Гобсон запатентовали получение такого металла при определенной температуре.
В нашей стране первые заводы по добыче этого металла начали свою работу уже веком позднее.
Происхождение названия
Само название, которое мы привыкли видеть в периодической системе Менделеева, впервые люди обнаружили в трудах, описанных швейцарским алхимиком Парацельсом. Именно он в те времена именовал этот металл zinken.
В последующем название было адаптировано для других языков. В переводе данное слово означает «зубец». Такое название Парацельс дал цинку именно потому, что металл напоминает кристаллы с иглами или с некими зубцами на поверхности.
Нахождение в природе
Всего ученые насчитывают около 66 минералов цинка или его производных. Этот металл научились смешивать с другими элементами, тем самым получая разнообразные смеси и различные цвета.
Первичным минералом считается так называемая цинковая обманка, которая была обнаружена еще в Древней Греции. В природе она встречается в виде смеси с бурым шпатом.
В земной коре содержится около 10% цинка. Также его можно найти в извергаемых земных породах. В кислых содержится значительно меньше. Также в природе встречается и гидроксид цинка. Всего насчитывается 5 его модификаций.
Цинк имеет свойство мигрировать в термальных водах. Кроме того, его можно обнаружить и в подземных и поверхностных водах, где он также успешно мигрирует.
Ученые выяснили, что и в живых организмах находится относительно большое количество цинка. Он необходим им для успешной жизнедеятельности.
Получение цинка
Самостоятельно как металл в природе невозможно встретить данный элемент. Люди добывают его из руд, а затем обогащают и получают его концентраты. После получения производят обжиг в специальных печах, далее доводя его до необходимого состояния.
Основным способом получения этого металла считается электролитический способ. Концентраты, полученные при обжигании в печи, обрабатывают специальным раствором, после чего тщательно очищают от различных примесей и подвергают электролизу.
Физические свойства
Внешне цинк напоминает обычный бело-серебристый металл, у которого на поверхности много мелких иголочек. При комнатной температуре этот элемент является очень хрупким и его легко согнуть или повредить. Пластичность его возникает при температуре плавления около 100 и более градусов.
Степень окисления или валентность цинка +2. Молярная масса — 65,38 г/моль. Плотность — 7,1333 г/см3. Химическая формула — Zn. Электронная конфигурация содержит около 40 атомов ядер. Вокруг по орбитам движутся 30 электронов.
Химические свойства
В обычной среде обитания или при комнатной температуре этот элемент покрывается оксидом. Когда его нагревают, то происходит сгорание и образуется белый оксид цинка. Его можно соединять с различными соединениями кислот, щелочами, и взаимодействиями растворами.
С некоторыми элементами периодической системы цинк никак не реагирует. Это азот, водород и другие элементы.
Применение
Цинк применяется не как самостоятельный металл. Он полезен людям для того, чтобы добывать с помощью выщелачивания золото и серебро.
Также цинк полезен тем, что используется как антикоррозийное покрытие для металлических предметов или емкостей.
Очень эффективен металл для использования в качестве материала в химических источниках тока. Часто окись его применяют в батарейках или аккумуляторах разной направленности.
Цинк применяется и в полиграфии в качестве пластин для печатей. Как противовоспалительное средство люди научились применять оксид цинка. Также люди используют и нитрат цинка ввиду его специфических свойств. Например, в авиастроении для защиты металлических частей от коррозии.
Производство цинка в мире
В мире очень широко применяется данный материал. Этот элемент является четвертым по частоте использования во всем мире.
Наиболее массово производят цинк в Китае, Австралии, Перу, США и Канаде. В России производят около 190000 тонн цинка в год.
Биологическая роль цинка
У взрослого человека в организме содержится определенное количество цинка, а именно около 2 г. В человеческом организме он содержится в качестве органических соединений, которые находятся в мышечной ткани, поджелудочной железе и печени.
Цинк очень полезен для человека, а его недостаток обычно определяет появление различных заболеваний и патологий. Множество ферментов в человеческом организме содержат данный элемент.
Биологически цинк нужен организму для:
- выработки мужских половых гормонов, в частности, спермы;
- правильной деятельности простаты;
- метаболизма витаминов и питательных веществ;
- синтеза гормонов;
- расщепления клеток алкоголя и ускорения выведения токсинов.
Польза данного элемента очень важна как для взрослых, так и для детей. Для аллергиков и людям с некоторыми заболеваниями хорошо подходят витамины в жидком виде, так как они хорошо усваиваются и для их производства не применяются консерванты. Существуют цинкосодержащие препараты как для взрослых, так и для детей.
Важно помнить, что переизбыток цинка так же вреден, как и недостаток. Поэтому крайне важно следить за правильными пропорциями.
Содержание в продуктах питания
В день взрослому здоровому человеку рекомендуется употреблять около 8 — 10 мг данного элемента. Суточная норма потребления варьируется в зависимости от возраста, пола и индивидуальных особенностей человека.
Очень много цинка содержится в морепродуктах, семенах тыквы и подсолнечника, некоторых крупах.
Есть в природе минеральные воды, которые также богаты наличием цинка в составе.
Отражение недостатка цинка на здоровье человека
Недостаток данного микроэлемента в организме обуславливается появлением некоторых возникающих симптомов. А именно могут появиться: аллергия, головокружение, высыпания на теле, ухудшение зрения и слуха, повышенная утомляемость.
Многие люди замечают появление у себя подобных симптомов, но редко связывают это с переизбытком или недостатком каких-либо микроэлементов. Хотя зачастую при регулировании их нормального потребления все патологические процессы самостоятельно исчезают.
Для того, чтобы регулировать нормальное содержание витаминов и минералов, врачи нередко назначают цинксодержащие препараты. Они положительно влияют не только на внутреннее состояние здоровья человека, но и благотворно влияют на его внешний вид.
Очень часто назначается пиколинат цинка. По сути это смесь цинка с пиколиновой кислотой. Такое сочетание усиливает благоприятное воздействие на здоровье человека.
Усваиваемость данного микроэлемента разная у каждого человека. Поэтому врачи должны учитывать данный факт. В некоторых случаях назначается глюконат цинка. В других — ацетат. Для лечения назначается и сульфат цинка, но его содержание должно строго регулироваться лечащим врачом.
Токсичность цинка
Переизбыток данного микроэлемента очень вреден для здоровья человека, так же как и его недостаток. Переизбыток цинка вызывает интоксикацию организма.
В особенности при длительном чрезмерном насыщении организма данным веществом, соли и сульфаты цинка отравляют человека своей токсичностью.
Сульфаты цинка образуются при неправильном хранении продуктов питания. Особенно вредно хранить продукты в закрытых емкостях из оцинкованной посуды.
Токсичность цинка вызывает даже бесплодие, импотенцию и другие проблемы со здоровьем. Можно отравиться им, вдыхая его пары. Проявляться такое отравление будет в виде головокружения, потери сознания, учащении пульса и появлении неприятного привкуса в ротовой полости.
Предыдущая
Что такое цинк? Цинк – серебристо-белый металл с голубоватым оттенком. В чистом виде в природе цинк, как химический элемент, практически не встречается. Согласно таблице Менделеева
Цинк — химический элемент 12-й группы (по устаревшей классификации — побочной подгруппы второй группы), четвёртого периода периодической системы, Символ обозначения Zn (лат. Zincum)
В настоящее время хорошо исследованы пять стабильных изотопов цинка, с массовыми числами соответственно 64,66,67,68,70. Самым распространённым среди стабильных изотопов цинка считается Zn 64 (48.89%). Девять радиоактивных цинковых изотопов получены искусственным путем. К ним относится 65 Zn. Это самый долгоживущий цинковый изотоп, период полураспада которого составляет 245 суток, поэтому он используется в качестве изотопного индикатора.
| Название, символ, номер | Цинк / Zincum (Zn), 30 |
| Атомная масса (молярная масса) | 65,38(2)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d10 4s2 |
| Радиус атома | 138 пм |
Цинк при стандартных климатических условиях хрупкий металл. После нагревания цинка до 100 градусов и выше (до 150 градусов С) происходят изменения в кристаллической решетке, в результате чего металл становится пластичным, гибким, его можно подвергать дополнительной механической обработке. Строение кристаллической решетки – гексагональное.
| Структура решётки | гексагональная |
| Параметры решётки | a=2,6648 c=4,9468 Å |
| Отношение c/a | 1,856 |
| Температура Дебая | 234 K |
Общие сведения:
| 100 | Общие сведения | |
| 101 | Название | Цинк |
| 102 | Прежнее название | |
| 103 | Латинское название | Zincum |
| 104 | Английское название | Zinc |
| 105 | Символ | Zn |
| 106 | Атомный номер (номер в таблице) | 30 |
| 107 | Тип | Металл |
| 108 | Группа | Амфотерный, переходный, цветной металл |
| 109 | Открыт | Известен с глубокой древности |
| 110 | Год открытия | до 1000 года до н.э. |
| 111 | Внешний вид и пр. | Хрупкий металл голубовато-белого цвета |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,0078 % |
| 120 | Содержание в морях и океанах (по массе) | 5,0·10-7 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,00003 % |
| 122 | Содержание в Солнце (по массе) | 0,0002 % |
| 123 | Содержание в метеоритах (по массе) | 0,018 % |
| 124 | Содержание в организме человека (по массе) | 0,0033 % |
Цинк (Zn, Zincum)
История цинка
Цинк в чистом виде впервые выделил Уильям Чемпион в 1738 году, хотя латунь (сплав меди с цинком) использовали в Древнем Египте и Древней Греции (calorizator). Иногда первооткрывателем цинка называют немца С. Маргграфа, который в 1746 году разработал аналогичный способ выработки цинка и описал его более подробно, чем Чемпион.
Названием цинк обязан Парацельсу, в чьих трудах встречаются слова zincum и zinken, которыми назван металл, видимо, из-за схожести его кристаллитов с иглами (zinke – зубец).
Общая характеристика цинка
Цинк является элементом побочной подгруппы II группы IV периода периодической системы химических элементов Д.И. Менделеева, имеет атомный номер 30 и атомную массу 65,39. Принятое обозначение – Zn (от латинского Zincum).
Нахождение в природе
Цинк достаточно распространённый элемент, он содержится в земной коре, практически во всех водных ресурсах Мирового Океана и во многих живых организмах. На сегодняшний день известно более 60-ти минералов цинка (сфалерит, цинкит, каламин и др.). крупные месторождения цинка обнаружены в Австралии, Боливии, Иране и Казахстане.
Физические и химические свойства
Цинк является хрупким, пластичным переходным металлом, имеет бело-голубоватый цвет, на воздухе покрывается слоем оксида цинка, что приводит к потускнению. При высоких температурах сгорает, образуя белый оксид цинка.
Суточная потребность в цинке
В сутки организм взрослого здорового человека должен получать от 9 до 11 мг цинка, дети – чуть меньше, от 2 до 8 мг, женщины в период беременности и кормления грудью – от 11 до 13 мг.
Продукты питания богатые цинком
Основные поставщики цинка – продукты питания, важный для жизнедеятельности организма элемент содержится в зелёных листовых овощах, брокколи, цветной капусте и редисе, моркови и кукурузе, зелёном луке, фасоли, горохе и чечевице, авокадо и ягодах, арахисе, кокосе, грецких и кедровых орехах, кунжуте, пшенице, овсянке и рисе. Присутствует цинк и в продуктах животного происхождения – свинине и баранине, говядине и индейке, мясе утки и говяжьем языке, морепродуктах и рыбе, плавленом сыре и яичном желтке.
Полезные свойства цинка и его влияние на организм
Функции и полезные свойства цинка:
- участие в формировании костных тканей,
- предупреждение диабета,
- препятствие появлению эпилепсии,
- обеспечение быстрого заживления ран,
- пособничество всасыванию витамина А,
- улучшение состояния волос,
- положительное влияние на умственные способности человека,
- профилактика возникновения артрита и ревматизма.
Взаимодействие с другими
Цинк необходим для метаболизма витамина E, витамин А действует только в присутствии цинка. Витамин С и цинк — хорошее средство против катаров и многих вирусных заболеваний.
Признаки нехватки цинка
Нехватка цинка в организме человека характеризуется следующими симптомами:
- расстройства деятельности желудочно-кишечного тракта,
- хрупкость ногтей и появление на них белых пятен,
- истощение и выпадение волос,
- потеря чувства вкуса и аппетита,
- незаживление мелких ран,
- нервозность, быстрая утомляемость,
- снижение памяти.
Признаки избытка цинка
Избыточное содержание цинка в организме человека как правило обусловлено приёмом БАДов и препаратов цинка, характеризуется головными болями, приступами слабости и тошнотой.
Применение цинка в жизни
Цинк в чистом виде используется как восстановитель благородных металлов, как защита стали от коррозии, для производства аккумуляторов, в полиграфической промышленности, в медицине, производстве различных сплавов, резиновых шин и масляных красок.
Автор: Виктория Н. (специально для ) Копирование данной статьи целиком или частично запрещено.
Свойства атома цинка:
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 65,38(2) а.е.м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 |
| 203 | Электронная оболочка | K2 L8 M18 N2 O0 P0 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 142 пм |
| 205 | Эмпирический радиус атома* | 135 пм |
| 206 | Ковалентный радиус* | 122 пм |
| 207 | Радиус иона (кристаллический) | Zn2+ 74 (4) пм, 88 (6) пм, Читайте также: Как отличить электроды постоянного тока от переменного 104 (8) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 139 пм |
| 209 | Электроны, Протоны, Нейтроны | 30 электронов, 30 протонов, 35 нейтронов |
| 210 | Семейство (блок) | элемент d-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 12-ая группа (по старой классификации – побочная подгруппа 2-ой группы) |
| 213 | Эмиссионный спектр излучения |
Атом и молекула цинка. Формула цинка. Строение атома цинка:
Цинк (лат. Zincum, от нем. Zinke – «зубец») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением Zn и атомным номером 30. Расположен в 12-й группе (по старой классификации – побочной подгруппе второй группы), четвертом периоде периодической системы.
Цинк – амфотерный металл. Относится к группе переходных металлов. Относится к цветным металлам.
Цинк обозначается символом Zn.
Как простое вещество цинк при нормальных условиях представляет собой хрупкий металл голубовато-белого цвета (тускнеет на воздухе, покрываясь тонким слоем оксида цинка).
Молекула цинка одноатомна.
Химическая формула цинка Zn.
Электронная конфигурация атома цинка 1s2 2s2 2p6 3s2 3p6 3d10 4s2. Потенциал ионизации (первый электрон) атома цинка равен 906,4 кДж/моль (9,394197(6) эВ).
Строение атома цинка. Атом цинка состоит из положительно заряженного ядра (+30), вокруг которого по четырем оболочкам движутся 30 электронов. При этом 28 электронов находятся на внутреннем уровне, а 2 электрона – на внешнем. Поскольку цинк расположен в четвертом периоде, оболочек всего четыре. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлена s- и р-орбиталями. Третья – внутренняя оболочка представлена s-, р- и d-орбиталями. Четвертая – внешняя оболочка представлена s-орбиталью. На внешнем энергетическом уровне атома цинка – на s-орбитали находится два спаренных электрона. В свою очередь ядро атома цинка состоит из 30 протонов и 35 нейтронов.
Радиус атома цинка (вычисленный) составляет 142 пм.
Атомная масса атома цинка составляет 65,38(2) а. е. м.
Цинк с давних пор широко используется человеком.
Цинк, свойства атома, химические и физические свойства
Химические свойства цинка:
| 300 | Химические свойства | |
| 301 | Степени окисления | -2, 0, +1, +2 |
| 302 | Валентность | II |
| 303 | Электроотрицательность | 1,65 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 906,4 кДж/моль (9,394197(6) эВ) |
| 305 | Электродный потенциал | Zn2+ + 2e— → Zn, Eo = -0,763 В |
| 306 | Энергия сродства атома к электрону | 0 кДж/моль |
Физические свойства цинка:
| 400 | Физические свойства | |
| 401 | Плотность* | 7,14 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 6,57 г/см3 (при температуре плавления 419,53 °C и иных стандартных условиях, состояние вещества – жидкость), 6,4 г/см3 (при 800 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | 419,53 °C (692,68 K, 787,15 °F) |
| 403 | Температура кипения* | 907 °C (1180 K, 1665 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 7,32 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 115 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость* | 25,47Дж/(K·моль) |
| 411 | Молярный объём | 9,2 см³/моль |
| 412 | Теплопроводность | 116 Вт/(м·К) (при стандартных условиях), 116 Вт/(м·К) (при 300 K) |
| 413 | Коэффициент теплового расширения | 30,2 мкм/(М·К) (при 25 °С) |
| 414 | Коэффициент температуропроводности | |
| 415 | Критическая температура | |
| 416 | Критическое давление | |
| 417 | Критическая плотность | |
| 418 | Тройная точка | |
| 419 | Давление паров (мм.рт.ст.) | |
| 420 | Давление паров (Па) | |
| 421 | Стандартная энтальпия образования ΔH | |
| 422 | Стандартная энергия Гиббса образования ΔG | |
| 423 | Стандартная энтропия вещества S | |
| 424 | Стандартная мольная теплоемкость Cp | |
| 425 | Энтальпия диссоциации ΔHдисс | |
| 426 | Диэлектрическая проницаемость | |
| 427 | Магнитный тип | |
| 428 | Точка Кюри | |
| 429 | Объемная магнитная восприимчивость | |
| 430 | Удельная магнитная восприимчивость | |
| 431 | Молярная магнитная восприимчивость | |
| 432 | Электрический тип | |
| 433 | Электропроводность в твердой фазе | |
| 434 | Удельное электрическое сопротивление | |
| 435 | Сверхпроводимость при температуре | |
| 436 | Критическое магнитное поле разрушения сверхпроводимости | |
| 437 | Запрещенная зона | |
| 438 | Концентрация носителей заряда | |
| 439 | Твёрдость по Моосу | |
| 440 | Твёрдость по Бринеллю | |
| 441 | Твёрдость по Виккерсу | |
| 442 | Скорость звука | |
| 443 | Поверхностное натяжение | |
| 444 | Динамическая вязкость газов и жидкостей | |
| 445 | Взрывоопасные концентрации смеси газа с воздухом, % объёмных | |
| 446 | Взрывоопасные концентрации смеси газа с кислородом, % объёмных | |
| 446 | Предел прочности на растяжение | |
| 447 | Предел текучести | |
| 448 | Предел удлинения | |
| 449 | Модуль Юнга | |
| 450 | Модуль сдвига | |
| 451 | Объемный модуль упругости | |
| 452 | Коэффициент Пуассона | |
| 453 | Коэффициент преломления |
Свойства цинка (таблица): температура, плотность, давление и пр.:
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Цинк |
| 102 | Прежнее название | |
| 103 | Латинское название | Zincum |
| 104 | Английское название | Zinc |
| 105 | Символ | Zn |
| 106 | Атомный номер (номер в таблице) | 30 |
| 107 | Тип | Металл |
| 108 | Группа | Амфотерный, переходный, цветной металл |
| 109 | Открыт | Известен с глубокой древности |
| 110 | Год открытия | до 1000 года до н. э. |
| 111 | Внешний вид и пр. | Хрупкий металл голубовато-белого цвета |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,0078 % |
| 120 | Содержание в морях и океанах (по массе) | 5,0·10-7 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,00003 % |
| 122 | Содержание в Солнце (по массе) | 0,0002 % |
| 123 | Содержание в метеоритах (по массе) | 0,018 % |
| 124 | Содержание в организме человека (по массе) | 0,0033 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 65,38(2) а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 |
| 203 | Электронная оболочка | K2 L8 M18 N2 O0 P0 Q0 R0
|
| 204 | Радиус атома (вычисленный) | 142 пм |
| 205 | Эмпирический радиус атома* | 135 пм |
| 206 | Ковалентный радиус* | 122 пм |
| 207 | Радиус иона (кристаллический) | Zn2+ 74 (4) пм, 88 (6) пм, 104 (8) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 139 пм |
| 209 | Электроны, Протоны, Нейтроны | 30 электронов, 30 протонов, 35 нейтронов |
| 210 | Семейство (блок) | элемент d-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 12-ая группа (по старой классификации – побочная подгруппа 2-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | -2, 0, +1, +2 |
| 302 | Валентность | II |
| 303 | Электроотрицательность | 1,65 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 906,4 кДж/моль (9,394197(6) эВ) |
| 305 | Электродный потенциал | Zn2+ + 2e– → Zn, Eo = -0,763 В |
| 306 | Энергия сродства атома к электрону | 0 кДж/моль |
| 400 | Физические свойства | |
| 401 | Плотность* | 7,14 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело), 6,57 г/см3 (при температуре плавления 419,53 °C и иных стандартных условиях, состояние вещества – жидкость), 6,4 г/см3 (при 800 °C и иных стандартных условиях, состояние вещества – жидкость) |
| 402 | Температура плавления* | 419,53 °C (692,68 K, 787,15 °F) |
| 403 | Температура кипения* | 907 °C (1180 K, 1665 °F) |
| 404 | Температура сублимации | |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл)* | 7,32 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 115 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость* | 25,47Дж/(K·моль) |
| 411 | Молярный объём | 9,2 см³/моль |
| 412 | Теплопроводность | 116 Вт/(м·К) (при стандартных условиях), 116 Вт/(м·К) (при 300 K) |
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Гексагональная плотноупакованная
|
| 513 | Параметры решётки | a = 2,6648 Å, c = 4,9468 Å |
| 514 | Отношение c/a | 1,856 |
| 515 | Температура Дебая | 234 K |
| 516 | Название пространственной группы симметрии | P63/mmc |
| 517 | Номер пространственной группы симметрии | 194 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7440-66-6 |
Примечание:
205* Эмпирический радиус атома цинка согласно [1] и [3] составляет 134 пм и 138 пм соответственно.
206* Ковалентный радиус цинка согласно [1] и [3] составляет 122±4 пм и 125 пм соответственно.
401* Плотность цинка согласно [3] и [4] составляет 7,133 г/см3 (при 0 °C/20 °C и иных стандартных условиях, состояние вещества – твердое тело), согласно [4] составляет 6,59 г/см3 (при 500 °C и иных стандартных условиях, состояние вещества – жидкость).
402* Температура плавления цинка согласно [3] и [4] составляет 419,6 °С (692,75 K, 787,28 °F) и 419,5 °С (692,65 K, 787,1 °F).
403* Температура кипения цинка согласно [3] и [4] составляет 906,2 °С (1179,35 K, 1663,16 °F) и 906 °C (1179,15 К, 1662,8 °F) соответственно.
407* Удельная теплота плавления (энтальпия плавления ΔHпл) цинка согласно [3] и [4] составляет 7,28 кДж/моль и 7,24 кДж/моль соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) цинка согласно [3] и [4] составляет 114,8 кДж/моль и 115,3 кДж/моль соответственно.
410* Молярная теплоёмкость цинка согласно [3] составляет 25,4 Дж/(K·моль).
Кристаллическая решётка цинка:
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Гексагональная плотноупакованная |
| 513 | Параметры решётки | a = 2,6648 Å, c = 4,9468 Å |
| 514 | Отношение c/a | 1,856 |
| 515 | Температура Дебая | 234 K |
| 516 | Название пространственной группы симметрии | P63/mmc |
| 517 | Номер пространственной группы симметрии | 194 |
( 1 оценка, среднее 5 из 5 )
ЦИНК (Zincum) Zn – химический элемент 12-й (IIb) группы Периодической системы. Атомный номер 30, относительная атомная масса 65,39. Природный цинк состоит из трех стабильных изотопов 64Zn (48,6%), 66Zn (26,9%) и 67Zn (4,1%). Известно несколько радиоактивных изотопов, важнейший из них – 65Zn с периодом полураспада 244 сут. Степень окисления +2.
История открытия.
Цинк (как и золото, серебро, медь, ртуть, свинец, олово и железо) относится к металлам древности, дата открытия которых теряется в веках.
Восстановление оксида цинка древесным углем требует температуры не менее 1000° С. Так как металл при этой температуре находится в парообразном состоянии и легко окисляется, выделение цинка требует умения конденсировать металлический пар, причем делать это надо в отсутствие воздуха, иначе металл превратится в оксид.
Получение сплавов цинка из смешанных руд не требует выделения самого цинка и достигается проще. Небольшие количества цинка, присутствующие в образцах древнеегипетской меди отражают состав местных руд, однако для выплавки палестинской латуни, датируемой 1400–1000 до н.э. и содержащей около 23% цинка, уже должны были преднамеренно смешивать медную руду с цинковой. Латунь получали и на Кипре и, позднее, в районе Кельна (Германия). Китайские мастера овладели искусством выплавки цинка в средние века. Цинковые монеты использовались в годы правления династии Минь (1368–1644).
В средневековой Европе не было специального производства цинка, хотя его небольшие количества получались при производстве свинца, серебра и латуни. Начиная примерно с 1605, его импортировала из Китая Восточно-Индийская Компания. Английская цинковая промышленность появилась в районе Бристоля в начале 18 в., и ее продукция быстро проникла в Силезию и Бельгию.
Происхождение названия элемента неясно, однако кажется правдоподобным, что оно произведено от Zinke (по-немецки «острие», или «зуб»), благодаря внешнему виду металла.
Распространение цинка в природе и его промышленное извлечение. Содержание цинка в земной коре составляет 7,6·10–3%, он распространен примерно так же, как рубидий (7,8·10–3%), и чуть больше, чем медь (6,8·10–3%).
Основными минералами цинка являются сульфид цинка ZnS (известный как цинковая обманка или сфалерит) и карбонат цинка ZnCO3 (каламин в Европе, смитсонит в США). Свое название этот минерал получил в честь Джеймса Смитсона, основателя Смитсонианского Института в Вашингтоне. Менее важными минералами являются гемиморфит Zn4Si2O7(OH)2·H2O и франклинит (Zn,Fe)O·Fe2O3.
Первое место в мире по добыче (16,5% мировой добычи, 1113 тыс. т, 1995) и запасам цинка занимает Канада. Кроме того, богатые месторождения цинка сосредоточены в Китае (13,5%), Австралии (13%), Перу (10%), США (10%), Ирландии (около 3%).
Добыча цинка ведется в 50 странах. В России цинк извлекается из медноколчеданных месторождений Урала, а также из полиметаллических месторождений в горах Южной Сибири и Приморья. Крупные запасы цинка сосредоточены в Рудном Алтае (Восточный Казахстан), на долю которого приходится более 50% добычи цинка в странах СНГ. Цинк добывают также в Азербайджане, Узбекистане (месторождение Алмалык) и Таджикистане.
Характеристика простого вещества и промышленное получение металлического цинка. Металлический цинк обладает характерным голубоватым блеском на свежей поверхности, который он быстро теряет во влажном воздухе. Температура плавления 419,58° С, температура кипения 906,2° С, плотность 7,133 г/см3. При комнатной температуре цинк хрупок, при 100–150° С становится пластичным и легко прокатывается в тонкие листы и проволоку, а при 200–250° С вновь становится очень хрупким и его можно быть истолочь в порошок.
При нагревании цинк взаимодействуют с неметаллами (кроме водорода, углерода и азота). Активно реагирует с кислотами:
Zn + H2SO4(разб.) = ZnSO4 + H2
Цинк – единственный элемент группы, который растворяется в водных растворах щелочей с образованием ионов [Zn(OH)4]2– (гидроксоцинкатов):
Zn + 2OH– + 2H2O = [Zn(OH)4]2– + H2
При растворении металлического цинка в растворе аммиака образуется аммиачный комплекс:
Zn + 4NH3·H2O = [Zn(NH3)4](OH)2 + 2H2O + H2
Исходное сырье для получения металлического цинка – сульфидные цинковые и полиметаллические руды. Выделение цинка начинается с концентрирования руды методами седиментации или флотации, затем ее обжигают до образования оксидов:
2ZnS + 3O2 = 2ZnO + SO2
Образующийся диоксид серы используют в производстве серной кислоты, а оксид цинка перерабатывают электролитическим методом или выплавляют с коксом.
В первом случае цинк выщелачивают из сырого оксида разбавленным раствором серной кислоты. При этом цинковой пылью осаждают кадмий:
Zn + Cd2+ = Zn2+ + Cd
Затем раствор сульфата цинка подвергают электролизу. Металл 99,95%-ной чистоты осаждается на алюминиевых катодах.
Восстановление оксида цинка коксом описывается уравнением:
2ZnO + C = 2Zn + CO2
Для выплавки цинка ранее использовались ряды сильно нагретых горизонтальных реторт периодического действия, затем они были заменены непрерывно действующими вертикальными ретортами (в некоторых случаях, с электрическим подогревом). Эти процессы не были так термически эффективны, как доменный процесс, в котором сжигание топлива для нагрева проводится в той же камере, что и восстановление оксида, однако неизбежная проблема в случае цинка в том, что восстановление оксида цинка углеродом не протекает ниже температуры кипения цинка (этой проблемы нет для железа, меди или свинца), поэтому для конденсации паров нужно последующее охлаждение. Кроме того, в присутствии продуктов сгорания металл повторно окисляется.
Эту проблему можно решить, опрыскивая выходящие из печи пары цинка расплавленным свинцом. Это приводит к быстрому охлаждению и растворению цинка, так что повторное окисление цинка сводится к минимуму. Затем цинк почти 99%-й чистоты выделяют в виде жидкости и дополнительно очищают вакуумной дистилляцией до чистоты 99,99%. Весь присутствующий кадмий в ходе дистилляции восстанавливается. Преимущество доменной печи в том, что состав шихты не имеет принципиального значения, поэтому можно использовать смешанные руды цинка и свинца (ZnS и PbS часто находят вместе) для непрерывного производства обоих металлов. Свинец при этом выпускают со дна печи.
По данным экспертов, в 2004 производство цинка составило 9,9 млн тонн, а его потребление – около 10,2 млн тонн. Таким образом, дефицит цинка на мировом рынке равен 250–300 тыс. тонн.
В 2004 в Китае выпуск рафинированного цинка достиг 2,46 млн т. Примерно по 1 млн. т производят Канада и Австралия. Цена на цинк в конце 2004 составила более 1100 долл. за тонну.
Спрос на металл остается высоким, благодаря бурному росту производства антикоррозионных покрытий. Для получения таких покрытий используют различные способы: погружение в расплавленный цинк (цинкование горячим способом), электролитическое осаждение, опрыскивание жидким металлом, нагревание с порошком цинка и использование красок, содержащих цинковый порошок. Оцинкованная жесть широко применяется как кровельный материал. Металлический цинк в виде брусков используют для защиты от коррозии стальных изделий, соприкасающихся с морской водой. Большое практическое значение имеют сплавы цинка – латуни (медь плюс 20–50% цинка). Для литья под давлением, помимо латуней, используется быстро растущее число специальных сплавов цинка. Еще одна область применения – производство сухих батарей, хотя в последние годы оно существенно сократилось.
Примерно половина всего производимого цинка используется для производства оцинкованной стали, одна треть – в горячем цинковании готовых изделий, остальное – для полосы и проволоки. За последние 20 лет мировой рынок этой продукции вырос более чем в 2 раза, в среднем прибавляя по 3,7 % в год, причем в странах Запада производство металла ежегодно увеличивается на 4,8 %. В настоящее время для цинкования 1 т стального листа нужно в среднем 35 кг цинка.
По предварительным оценкам, в 2005 потребление цинка в России может составить порядка 168,5 тыс. т в год, в том числе 90 тыс. т пойдет на цинкование, 24 тыс. т – на полуфабрикаты (латунный, цинковый прокат и др.), 29 тыс. т – в химическую промышленность (лакокрасочные материалы, резинотехнические изделия), 24,2 тыс. т – на литейные цинковые сплавы.
Соединения цинка.
Цинк образует многочисленные бинарные соединения с неметаллами, некоторые из них обладают полупроводниковыми свойствами.
Соли цинка бесцветны (если не содержат окрашенных анионов), их растворы имеют кислотную среду вследствие гидролиза. При действии растворов щелочей и аммиака (начиная с pH ~ 5) основные соли осаждаются и переходят в гидроксид, который растворяется в избытке осадителя.
Оксид цинка ZnO является самым важным промышленным цинксодержащим соединением. Будучи побочным продуктом производства латуни, он стал известен раньше, чем сам металл. Оксид цинка получают, сжигая на воздухе пары цинка, образующиеся при плавке руды. Более чистый и белый продукт производят сжиганием паров, полученных из предварительно очищенного цинка.
Обычно оксид цинка – это белый тонкий порошок. При нагревании его окраска меняется на желтую в результате удаления кислорода из кристаллической решетки и образованиея нестехиометрической фазы Zn1+xO(x Ј 7,10–5). Избыточное количество атомов цинка приводит к появлению дефектов решетки, захватывающих электроны, которые впоследствии возбуждаются при поглощении видимого света. Добавляя в оксид цинка 0,02–0,03%-ный избыток металлического цинка, можно получить целый спектр цветов – желтый, зеленый, коричневый, красный, однако красноватые оттенки природной формы оксида цинка – цинкита – появляются по другой причине: за счет присутствия марганца или железа. Оксид цинка ZnO амфотерен; он растворяется в кислотах с образованием солей цинка и в щелочах с образованием гидроксоцинкатов, таких как [Zn(OH)3]– и [Zn(OH)4]2–:
ZnO + 2OH– + H2O = [Zn(OH)4]2–
Основное промышленное применение оксида цинка – производство резины, в котором он сокращает время вулканизации исходного каучука.
В качестве пигмента при производстве красок оксид цинка имеет преимущества по сравнению с традиционными свинцовыми белилами (основной карбонат свинца), благодаря отсутствию токсичности и потемнения под действием соединений серы, однако уступает оксиду титана по показателю преломления и кроющей способности.
Оксид цинка увеличивает срок жизни стекла и поэтому используется в производстве специальных стекол, эмалей и глазурей. Еще одна важная область применения – в составе нейтрализующих косметических паст и фармацевтических препаратов.
В химической промышленности оксид цинка обычно является исходным веществом для получения других соединений цинка, в которых наиболее важными являются мыла (т.е. соединения жирных кислот, такие как стеарат, пальмитат и другие соли цинка). Их используют в качестве отвердителей красок, стабилизаторов пластмасс и фунгицидов.
Небольшая, но важная область применения оксида цинка – производство цинковых ферритов. Это шпинели типа ZnIIxMII1–xFeIII2O4, содержащие еще один двухзарядный катион (обычно MnII или NiII). При х = 0 они имеют структуру обращенной шпинели. Если х = 1, то структура соответствует нормальной шпинели. Понижение количества ионов FeIII в тетраэдрических позициях приводит к понижению температуры Кюри. Таким образом, изменяя содержание цинка, можно влиять на магнитные свойства ферритов.
Гидроксид цинка Zn(OH)2 образуется в виде студенистого белого осадок при добавлении щелочи к водным растворам солей цинка. Гидроксид цинка, так же как и оксид, амфотерен:
Zn(OH)2 + 2OH– = [Zn(OH)4]2–
Применяется для синтеза различных соединений цинка.
Сульфид цинка ZnS выделяется в виде белого осадка при взаимодействии растворимых сульфидов и солей цинка в водном растворе. В кислотной среде осадок сульфида цинка не выпадает в кислотной среде. Сероводородная вода осаждает сульфид цинка лишь в присутствии анионов слабых кислот, например, ацетат-ионов, которые понижают кислотность среды, что приводит к повышению концентрации сульфид-ионов в растворе.
Сфалерит ZnS является наиболее распространенным минералом цинка и главным источником металла, однако известна и вторая природная, хотя и намного более редкая форма вюрцит, более устойчивая при высокой температуре. Названия этих минералов используются для обозначения кристаллических структур, которые являются важными структурными типами, найденными для многих других соединений АВ. В обеих структурах атом цинка тетраэдрически координирован четырьмя атомами серы, а каждый атом серы тетраэдрически координирован четырьмя атомами цинка. Структуры существенно различаются только типом плотнейшей упаковки: в вюрците она кубическая, а в сфалерите – гексагональная.
Чистый сульфид цинка – белый и, подобно оксиду цинка, применяется как пигмент, для этого его часто получают (как литопон) вместе с сульфатом бария при взаимодействии водных растворов сульфата цинка и сульфида бария.
Свежеосажденный сульфид цинка легко растворяется в минеральных кислотах с выделением сероводорода:
ZnS + 2H3O+ = Zn2+ + H2S + 2H2O
Однако прокаливание делает его менее реакционноспособным, и поэтому он является подходящим пигментом в красках для детских игрушек, так как безвреден при проглатывании. Кроме того, у сульфида цинка интересные оптические свойства. Он становится серым при действии ультрафиолетового излучения (возможно, за счет диссоциации). Однако этот процесс можно замедлить, например, добавлением следов солей кобальта. Катодное, рентгеновское и радиоактивное излучение вызывает появление флуоресценции или люминесценции различных цветов, которую можно усилить добавлением следов различных металлов или замещением цинка кадмием, а серы селеном. Это широко используется для производства электроннолучевых трубок и экранов радаров.
Селенид цинка ZnSe может быть осажден из раствора в виде лимонно-желтого, плохо фильтрующегося осадка. Влажный селенид цинка очень чувствителен к действию воздуха. Высушенный или полученный сухим путем устойчив на воздухе.
Монокристаллы селенида цинка выращивают направленной кристаллизацией расплава под давлением или осаждением из газовой фазы. Сульфид цинка используется в качестве лазерного материала и компонента люминофоров (вместе с сульфидом цинка).
Теллурид цинка ZnTe, в зависимости от способа получения, – серый порошок, краснеющий при растирании, или красные кристаллы, используется как материал для фоторезисторов, приемников инфракрасного излучения, дозиметров и счетчиков радиоактивного излучения. Кроме того, он служит люминофором и полупроводниковым материалом, в том числе в лазерах.
Хлорид цинка ZnCl2 является одним из важных соединений цинка в промышленности. Его получают действием соляной кислоты на вторичное сырье или обожженную руду.
Концентрированные водные растворы хлорида цинка растворяют крахмал, целлюлозу (поэтому их нельзя фильтровать через бумагу) и шелк. Его применяют в производстве текстиля, кроме того, он используется как антисептик для древесины и при изготовлении пергамента.
Поскольку в расплаве хлорид цинка легко растворяет оксиды других металлов, его используют в ряде металлургических флюсов. С помощью раствора хлорида цинка очищают металлы перед пайкой.
Хлорид цинка применяется и в магнезиальном цементе для зубных пломб, как компонент электролитов для гальванических покрытий и в сухих элементах.
Ацетат цинка Zn(CH3COO)2 хорошо растворим в воде (28,5% по массе при 20° С) и многих органических растворителях. Его используют как фиксатор при крашении тканей, консервант древесины, противогрибковое средство в медицине, катализатор в органическом синтезе. Ацетат цинка входит в состав зубных цементов, используется при производстве глазурей и фарфора.
При перегонке ацетата цинка при пониженном давлении образуется основный ацетат [Zn4O(OCOMe)6], его молекулярная структура включает атом кислорода, окруженный тетраэдром из атомов цинка, связанных по ребрам ацетатными мостиками. Он изоморфен основному ацетату бериллия, но в отличие от него, быстро гидролизуется в воде, это обусловлено способностью катиона цинка иметь координационное число выше четырех.
Цинкорганические соединения. Открытие в 1849 английским химиком-органиком Эдуардом Франклендом (Frankland Edward) (1825–1899) алкилов цинка, хотя и не первых из синтезированных металлоорганических соединений (соль Цейзе была получена в 1827), можно считать началом металлоорганической химии. Исследования Франкленда положили начало применению цинкорганических соединений в качестве промежуточных веществ при органическом синтезе, а измерения плотности паров привело его к предположению (важнейшему в развитии теории валентности), что каждый элемент имеет ограниченную, но определенную силу сродства. Реактивы Гриньяра, открытые в 1900, сильно потеснили алкилы цинка в органическом синтезе, однако многие реакции, в которых они теперь используются, были сначала разработаны для соединений цинка.
Алкилы типа RZnX и ZnR2 (где Х – галоген, R – алкил) можно получить, нагревая цинк в кипящем RX в инертной атмосфере (диоксид углерода или азот). Ковалентные ZnR2 представляют собой неполярные жидкости или низкоплавкие твердые вещества. Они всегда мономерны в растворе и характеризуются линейной координацией атома цинка
C–Zn–C. Цинкорганические соединения очень чувствительны к действию воздуха. Соединения с малой молекулярной массой самовоспламеняются, образуя дым из оксида цинка. Их реакции с водой, спиртами, аммиаком и другими веществами протекают подобно реакциям Гриньяра, однако менее энергично. Важным отличием является то, что они не взаимодействуют с диоксидом углерода.
Биологическая роль цинка.
Цинк – одно из наиболее важных биологически активных элементов и необходим для всех форм жизни.
Тело взрослого человека содержит около 2 г цинка. Хотя цинксодержащие ферменты присутствуют в большинстве клеток, его концентрация очень мала и поэтому довольно поздно стало понятно, насколько важен этот элемент. Необходимость и незаменимость цинка для человека была установлена 100 лет тому назад.
Роль цинка в жизнедеятельности организма обусловлена, в основном, тем, что он входит в состав более 40 важных ферментов. Они катализируют гидролиз пептидов, белков, некоторых эфиров и альдегидов. Наибольшее внимание привлекают два цинксодержащих фермента: карбоксипептидаза А и карбоангидраза.
Карбоксипептидаза А катализирует гидролиз концевой пептидной связи в белках в процессе пищеварения. Она имеет относительную молекулярную массу около 34000 и содержит атом цинка, тетраэдрически координированный с двумя гистидиновыми атомами азота, карбоксильным атомом кислорода глутаматного остатка (см. БЕЛКИ) и молекулой воды. Точный механизм ее действия до конца не ясен, несмотря на интенсивное изучение модельных систем, однако принято считать, что первой стадией является координация концевого пептида к атому цинка.
Карбоангидраза была первым из открытых цинксодержащих ферментов (1940), она катализирует обратимую реакцию превращения диоксида углерода в угольную кислоту. В эритроцитах млекопитающих прямая реакция (гидратация) протекает при поглощении диоксида углерода кровью в тканях, а обратная реакция (дегидратация) идет, когда диоксид углерода затем высвобождается в легких. Фермент увеличивает скорости этих реакций примерно в миллион раз.
Относительная молекулярная масса фермента составляет около 30 000. Почти сферическая молекула содержит один атом цинка, расположенный в глубоком «кармане» белка, где есть и несколько молекул воды, расположенных в таком же порядке, как во льде. Атом цинка координирован тетраэдрически с тремя имидазольными атомами азота и молекулой воды. Точные детали действия фермента не установлены, однако кажется вероятным, что координированная молекула Н2О ионизируется с образованием Zn–OH–, а нуклеофил ОН– затем реагирует с атомом углерода в СО2 (который может удерживаться в правильном положении водородными связями двух его атомов кислорода) с образованием НСО3–.
В отсутствие фермента данная реакция требует высокого рН. Роль фермента заключается в создании подходящего окружения внутри белкового «кармана», которое способствует диссоциации координированной молекулы воды при рН 7.
Позднее была установлена функция цинка в белках, отвечающих за распознавание последовательности оснований в ДНК и, следовательно, регулирующих перенос генетической информации в ходе репликации ДНК. Эти белки с так называемыми «цинковыми пальцами» содержат 9 или 10 ионов Zn2+, каждый из которых, координируясь с 4 аминокислотами, стабилизирует выступающую складку («палец») белка. Белок обертывается вокруг двойной спирали ДНК, при этом каждый из «пальцев» связывается с ДНК. Их расположение совпадает с последовательностью оснований в ДНК, что обеспечивает точное распознавание.
Цинк участвует в углеводном обмене с помощью цинксодержащего гормона – инсулина. Только в присутствии цинка действует витамин А. Этот элемент необходим для формирования костей. Кроме того, он проявляет антивирусное и антитоксическое действие.
Цинк влияет на вкус и обоняние. Из-за нехватки цинка, необходимого для полноценного развития плода, многие женщины в первые 3 месяца беременности жалуются на капризы вкуса и обоняния.
Считается, что существует определенная связь между умственными и физическими способностями человека и содержанием цинка в его организме. Так, у хорошо успевающих студентов в волосах содержится больше цинка, чем у студентов отстающих. У больных ревматизмом и артритом наблюдается понижение уровня цинка в крови.
Дефицит цинка может быть вызван нарушением деятельности щитовидной железы, болезнями печени, плохим усвоением, недостатком цинка в воде и пище, а также слишком большим количеством фитина в продуктах питания (фитин связывает цинк, затрудняя его усвоение). Алкоголь также понижает уровень цинка в организме, особенно в мышцах и плазме крови.
Цинк необходим организму в количестве 10–20 мг в день, однако лекарствами восполнить недостаток цинка очень трудно. В естественных сочетаниях цинк содержится только в пище, что и определяет его усвояемость. Наиболее богаты цинком мясо, печень, молоко, яйца.
В организме существует конкуренция между цинком и медью, а также железом. Поэтому, употребляя богатую цинком пищу, следует дополнить диету пищей, богатой медью и железом. Нельзя применять цинк вместе с селеном, так как два этих элемента взаимодействуют друг с другом и выводятся из организма.
Елена Савинкина

СТРУКТУРА
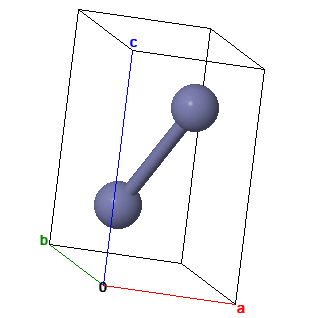
СВОЙСТВА

ЗАПАСЫ И ДОБЫЧА

Месторождения цинка известны в Иране, Австралии, Боливии, Казахстане. В России крупнейшим производителем свинцово-цинковых концентратов является ОАО «ГМК Дальполиметалл»
Цинк добывают из полиметаллических руд, содержащих 1—4% Zn в виде сульфида, а также Cu, Pb, Ag, Au, Cd, Bi. Руды обогащают селективной флотацией, получая цинковые концентраты (50—60% Zn) и одновременно свинцовые, медные, а иногда также пиритные концентраты.
Основной способ получения цинка — электролитический (гидрометаллургический). Обожжённые концентраты обрабатывают серной кислотой; получаемый сульфатный раствор очищают от примесей (осаждением их цинковой пылью) и подвергают электролизу в ваннах, плотно выложенных внутри свинцом или винипластом. Цинк осаждается на алюминиевых катодах, с которых его ежесуточно удаляют (сдирают) и плавят в индукционных печах.
ПРОИСХОЖДЕНИЕ

ПРИМЕНЕНИЕ

Применяется для защиты стали от коррозии (оцинковка поверхностей, не подверженных механическим воздействиям, или металлизация — для мостов, емкостей, металлоконструкций).
Цинк используется в качестве материала для отрицательного электрода в химических источниках тока, то есть в батарейках и аккумуляторах.
Пластины цинка широко используются в полиграфии, в частности, для печати иллюстраций в многотиражных изданиях. Для этого с XIX века применяется цинкография — изготовление клише на цинковой пластине при помощи вытравливания кислотой рисунка в ней. Примеси, за исключением небольшого количества свинца, ухудшают процесс травления. Перед травлением цинковую пластину подвергают отжигу и прокатывают в нагретом состоянии.
Цинк вводится в состав многих твёрдых припоев для снижения их температуры плавления.
Окись цинка широко используется в медицине как антисептическое и противовоспалительное средство. Также окись цинка используется для производства краски — цинковых белил.
Цинк — важный компонент латуни. Сплавы цинка с алюминием и магнием (ЦАМ, ZAMAK) благодаря сравнительно высоким механическим и очень высоким литейным качествам очень широко используются в машиностроении для точного литья. В частности, в оружейном деле из сплава ZAMAK (-3, −5) иногда отливают затворы пистолетов, особенно рассчитанных на использование слабых или травматических патронов. Также из цинковых сплавов отливают всевозможную техническую фурнитуру, вроде автомобильных ручек, корпусы карбюраторов, масштабные модели и всевозможные миниатюры, а также любые другие изделия, требующие точного литья при приемлемой прочности.
Хлорид цинка — важный флюс для пайки металлов и компонент при производстве фибры.
Теллурид, селенид, фосфид, сульфид цинка — широко применяемые полупроводники. Сульфид цинка — составная часть многих люминофоров. Фосфид цинка используется в качестве отравы для грызунов.
Селенид цинка используется для изготовления оптических стёкол с очень низким коэффициентом поглощения в среднем инфракрасном диапазоне, например, в углекислотных лазерах.
Цинк (англ. Zinc) — Zn
| Молекулярный вес | 65.39 г/моль |
| Происхождение названия | Слово «цинк» впервые встречается в трудах Парацельса, который назвал этот металл словом «zincum» или «zinken» в книге Liber Mineralium II |
| IMA статус | действителен, описан впервые до 1959 (до IMA) |
КЛАССИФИКАЦИЯ
| Strunz (8-ое издание) | 1/A.04-10 |
| Nickel-Strunz (10-ое издание) | 1.AB.05 |
| Dana (7-ое издание) | 1.1.8.1 |
| Dana (8-ое издание) | 1.1.5.1 | Hey’s CIM Ref | 1.8 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | белый металлический |
| Цвет черты | белый и слегка сероватый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | весьма совершенная по 0001 |
| Твердость (шкала Мооса) | 2 |
| Прочность | хрупкий |
| Излом | зазубренный |
| Плотность (измеренная) | 6.9 — 7.2 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | диамагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | 6/mmm (6/m 2/m 2/m) — дигексагональная дипирамидальная |
| Пространственная группа | P63/mmc |
| Сингония | гексагональная |
| Параметры ячейки | a = 2.665Å, c = 4.947Å |
mineralpro.ru
13.07.2016
Цинк (лат. Zincum), Zn (читается «цинк»), химический элемент с атомным номером 30, атомная масса 65, 39. Природный цинк состоит из смеси пяти стабильных нуклидов: 64Zn (48, 6% по массе), 66Zn (27, 9%), 67Zn (4, 1%), 68Zn (18, 8%) и 70Zn (0, 6%). Расположен в четвертом периоде в группе IIВ периодической системы. Конфигурация двух внешних электронных слоев 3s2p6d104s2. В соединениях проявляет степень окисления +2 (валентность II).
Радиус атома Zn 0, 139 нм, радиус иона Zn2+0, 060 нм (координационное число 4), 0, 0740 нм (координационное число 6) и 0, 090 нм (координационное число 8). Энергии последовательной ионизации атома соответствуют 9, 394, 17, 964, 39, 7, 61, 6 и 86, 3 эВ. Электроотрицательность по Полингу 1, 66.
Сплавы цинка с медью — латуни — были известны еще древним грекам и египтянам. Цинк получали в 5 в. до н. э. в Индии. Римский историк Страбон в 60-20 годах до н. э. писал о получении металлического цинка, или «фальшивого серебра». В дальнейшем секрет получения цинка в Европе был утерян, так как образующийся при термическом восстановлении цинковых руд цинк при 900°C переходит в пар. Пары цинка реагируют с кислородом воздуха, образуя рыхлый оксид цинка, который алхимики называли «белой шерстью».
В 1743 в Бристоле открылся первый завод по получению металлического цинка, где цинковую руду восстанавливали в ретортах без доступа воздуха. В 1746 А. С. Маргграф разработал способ получения металла прокаливанием смеси его окиси с углем без доступа воздуха в ретортах с последующей конденсацией паров цинка в холодильниках.
Слово «цинк» встречается в трудах Парацельса и других исследователей 16-17 вв. и восходит, возможно, к древнегерманскому «цинко» — налет, бельмо на глазу. Название этого металла за его историю несколько раз менялось. Общеупотребительным название «цинк» стало только в 1920-х гг.
Содержание цинка в земной коре 8, 3·10–3% по массе, в воде Мирового океана 0, 01 мг/л. Известно 66 минералов цинка, важнейшие из них: сфалерит, клейофан, марматит, вюртцит, смитсонит ZnCO3, каламин Zn4(OH)4Si2O7·H2O, цинкит ZnO, виллемит. Цинк входит в состав полиметаллических руд, которые содержат также медь, свинец, кадмий, индий, галлий, таллий и другие. Цинк — важный биогенный элемент: в живом веществе содержится 5·10–4% по массе.
Цинк добывают из полиметаллических руд, содержащих 1-4% Zn в виде сульфида. Руду обогащают, получая цинковый концентрат (50-60%). Цинковые концентраты обжигают в печах в кипящем слое, переводя сульфид цинка в ZnO. От ZnO к Zn идут двумя путями. По пирометаллургическому методу концентрат спекают, а затем восстанавливают углем или коксом при 1200-1300°C. Затем испарившиеся из печи пары цинка конденсируют.
ZnO + C = Zn + CO.
Основной способ получения цинка гидрометаллургический. Обожженные концентраты обрабатывают серной кислотой. Из полученного сульфатного раствора удаляют примеси, осаждая их цинковой пылью. Очищенный раствор подвергают электролизу. Цинк осаждается на алюминиевых катодах. Чистота электролитного цинка 99, 95%.
Для получения цинка высокой чистоты применяют зонную плавку.
Цинк — голубовато-белый металл.
Обладает гексагональной решеткой с параметрами а = 0, 26649 нм, с = 0, 49468 нм. Температура плавления 419, 58°C, температура кипения 906, 2°C, плотность 7, 133 кг/дм3. При комнатной температуре хрупок. При 100-150°C пластичен. Стандартный электродный потенциал –0, 76 В, в ряду стандартных потенциалов расположен до железа Fe.
На воздухе цинк покрывается тонкой пленкой оксида ZnO. При сильном нагревании сгорает с образованием амфотерного белого оксида ZnO.
2Zn + O2 = 2ZnO
Оксид цинка реагирует как с растворами кислот:
ZnO + 2HNO3 = Zn(NO3)2 + H2O
так и щелочами:
ZnO + 2NaOH (сплавление)= Na2ZnO2 + Н2О
В этой реакции образуется цинкат натрия Na2ZnO2.
Цинк обычной чистоты активно реагирует с растворами кислот:
Zn + 2HCl = ZnCl2 + H2
Zn + H2SO4 = ZnSO4 + H2
и растворами щелочей:
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2,
образуя гидроксоцинкаты. С растворами кислот и щелочей очень чистый цинк не реагирует. Взаимодействие начинается при добавлении нескольких капель раствора сульфата меди CuSO4.
При нагревании цинк реагирует с галогенами с образованием галогенидов ZnHal2. С фосфором цинк образует фосфиды Zn3P2 и ZnP2.С серой и ее аналогами — селеном и теллуром — различные халькогениды, ZnS, ZnSe, ZnSe2и ZnTe.
В водных растворах ионы цинка Zn2+ образуют аквакомплексы [Zn(H2O)4]2+ и [Zn(H2O)6]2+.
Основная часть производимого цинка расходуется на изготовление антикоррозионных покрытий железа и стали. Цинк применяют в аккумуляторах и сухих элементах питания. Листовой цинк используют в типографском деле. Сплавы цинка (латунь, нейзильбер и другие) применяются в технике. ZnO служит пигментом в цинковых белилах. Соединения цинка являются полупроводниками. Раствором хлорида цинка ZnCl2 пропитывают железнодорожные шпалы, предохраняя их от гниения.
Цинк входит в состав более 40 металлоферментов, катализирующих в организме человека гидролиз пептидов, белков и других соединений. Цинк входит в состав гормона инсулина. В организм человека цинк поступает с мясом, молоком, яйцами.
Растения при недостатке цинка в почве заболевают.
Металлический цинк мало токсичен. Фосфид и оксид цинка ядовиты. Попадание в организм растворимых солей цинка приводит к расстройству пищеварения, раздражению слизистых оболочек. ПДК для цинка в воде 1, 0 мг/л.
- Живописцев В. П., Селезнева Е. А. Аналитическая химия цинка. М., 1975.
- Зайцев В. Я., Маргулис Е. В. Металлургия свинца и цинка. М., 1985.
- Карлов В. И. Технологические расчеты по металлургии цинка. — Владикавказ: Изд-во СКГТУ, 2002.
- Рудные ресурсы и их размещение по геоэпохам. Цветные металлы. — М.: Недра, 1994.
- Цинк и кадмий в окружающей среде. — М.: Наука, 1992.



























